La cérémonie annuelle des Prix Inserm de la recherche médicale se tiendra le 3 décembre 2014 au Collège de France en présence de Marisol Touraine, ministre des Affaires sociales et de la Santé, Geneviève Fioraso, secrétaire d’Etat à l’Enseignement supérieur et à la Recherche et Yves Lévy, Président-directeur général de l’Inserm. Huit prix seront décernés aux personnalités scientifiques qui contribuent, par leurs travaux, aux progrès de la recherche et à l’excellence de l’Institut. La cérémonie clôturera une année exceptionnelle, rythmée par plus d’une centaine de manifestations célébrant le 50ème anniversaire de l’Inserm.
L’événement sera retransmis en direct sur le site de l’Inserm.
Le Grand Prix Inserm est attribué à Anne Dejean-Assémat, directrice de l’Unité mixte Inserm/Institut Pasteur 993 « Organisation nucléaire et oncogenèse », pour l’ensemble de ses recherches sur les mécanismes moléculaires et cellulaires impliqués dans le développement des cancers chez l’Homme. Anne Dejean-Assémat ©Inserm
Anne Dejean-Assémat ©Inserm
Cette chercheuse a établi le rôle mutagène du virus de l’hépatite B dans le cancer du foie. Elle a identifié l’un des premiers récepteurs de l’acide rétinoïque (RAR), la forme active de la vitamine A, puis démontré son rôle dans certains cancers humains.
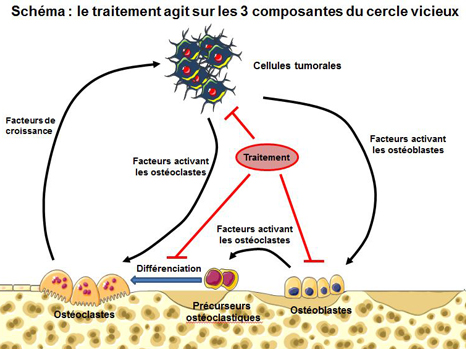
En découvrant l’altération systématique du récepteur de cet acide chez les patients atteints de leucémies aiguës promyélocytaires et l’altération cellulaire associée, Anne Dejean-Assémat a, avec ses collègues, clarifié les bases moléculaires et cellulaires de la leucémogénèse et permis de mettre au jour les mécanismes impliqués dans l’efficacité du traitement de ce type de leucémie. Ces observations constituent l’un des exemples les plus illustratifs de thérapie ciblée du cancer.
Les autres lauréats :
Depuis 2004, un Prix d’Honneur et un Prix International sont décernés, témoignant de la carrière de personnalités scientifiques particulièrement éminentes. Le Prix d’Honneur 2014 sera décerné à William Vainchenker (Unité 1009 Inserm/ Institut Gustave-Roussy/Université Paris-Sud), le Prix International à Sir Leszek Borysiewicz (Université de Cambridge, Royaume-Uni).
Les Prix Recherche distinguent des chercheurs, enseignants-chercheurs et cliniciens-chercheurs, dont les travaux ont particulièrement marqué le champ de la recherche fondamentale, de la recherche clinique et thérapeutique et de la recherche en santé publique. Les lauréats 2014 sont Nadine Cerf-Bensussan (Unité 1163 Institut Imagine/Université Paris-Descartes) et Hélène Dollfus (Unité 1112 Inserm/Université de Strasbourg).
Les Prix Innovation récompensent des ingénieurs, techniciens ou administratifs pour des réalisations originales au service de l’accompagnement de la recherche. Les lauréats 2014 sont Frédéric De Bock (Unité 661 Inserm/CNRS/Universités de Montpellier 1et 2) et Mathieu Ducros (Unité 1128 Inserm/ Université Paris-Descartes).
Depuis 2013, un Prix Opecst-Inserm est remis conjointement par l’Office parlementaire d’évaluation des choix scientifiques et technologiques et l’Inserm. Il vise à récompenser un chercheur pour son implication dans la valorisation des résultats de la recherche. Le lauréat 2014 est Mickaël Tanter (Unité 979 Inserm/CNRS/ESPCI de Paris).
La biographie détaillée d’Anne Dejean-Assémat est consultable sur le site de l’Académie des sciences
Des photos des lauréats sont disponibles en téléchargement sur Serimedis, la banque d’images de l’Inserm
Des films consacrés aux travaux des lauréats seront disponibles dès le 4 décembre sur Serimedis