L’insuffisance cardiaque concerne plus d’un million de personnes en France. Si le réseau sanguin est le premier à avoir été exploré en vue d’améliorer la fonction cardiaque, une étude de l’Inserm dévoile le potentiel d’un réseau secondaire jusque-là peu étudié. Les chercheurs[1] ont analysé chez l’animal le réseau lymphatique du cœur. Ils ont révélé que ce réseau était fortement altéré après un infarctus du myocarde. A l’aide d’une biothérapie basée sur l’injection de microparticules innovantes, ils sont parvenus à régénérer des vaisseaux lymphatiques de manière ciblée. Ce traitement favorise le drainage lymphatique, limitant ainsi l’œdème et l’inflammation post infarctus. Le fonctionnement du cœur est ainsi amélioré.
Ces résultats sont publiés dans la revue Circulation.
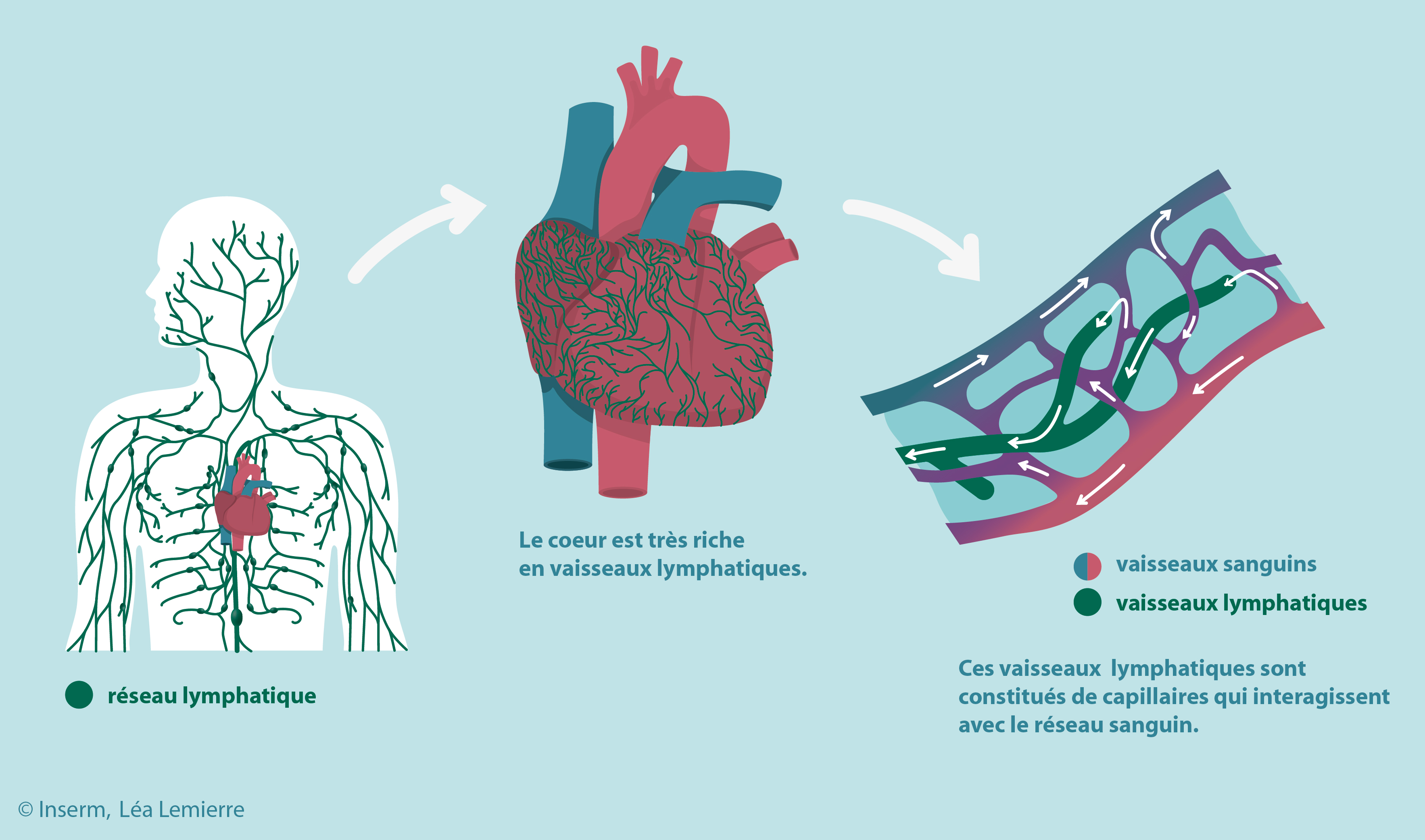
Lorsque le cœur n’est plus capable d’assurer un apport sanguin suffisant aux besoins du corps, on parle d’insuffisance cardiaque (IC). Celle-ci est due à une anomalie du muscle cardiaque qui peut être associés à des lésions, un défaut de remplissage associé à une maladie du poumon, la déformation des valves cardiaques… Fatigue, essoufflement et œdèmes en sont les principaux symptômes. Pendant que le réseau sanguin participe à l’alimentation des organes en sang et leur assure un apport en oxygène et en nutriments, le réseau lymphatique (voir illustration ci-dessous), transporte des fluides ainsi que des cellules immunitaires et draine des déchets cellulaires.

Le réseau lymphatique chez l’Homme © Inserm, Léa Lemierre
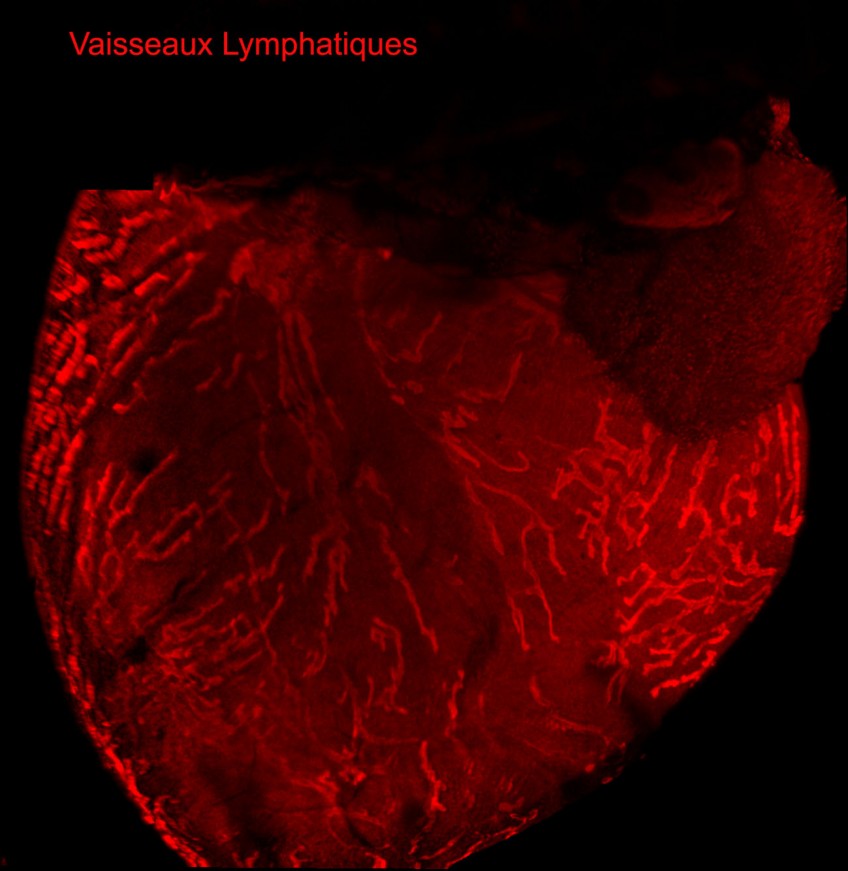
Le réseau lymphatique du cœur est particulièrement développé (voir photo ci-dessous) mais son rôle dans les maladies cardiovasculaires n’avait reçu jusqu’à ce jour très peu d’attention.
Vaisseaux lymphatiques du cœur chez le rat visibles en rouge par immunofluorescence © Inserm, Ebba Brakenhielm
Après un infarctus du myocarde, le réseau lymphatique du cœur subit de fortes modifications. Dans cette étude, les chercheurs de l’Inserm à Rouen montrent, en plus de cette anomalie structurelle, une altération du fonctionnement de ce réseau qui conduit à la formation d’un œdème et d’une inflammation cardiaque chronique. Pour résorber l’œdème, ils ont eu l’idée de stimuler la création de nouveaux vaisseaux lymphatiques du cœur de manière ciblée.
L’équipe de recherche a utilisé des microcapsules innovantes biodégradables, contenant des facteurs de croissance, précédemment mises au point lors de travaux sur la création de vaisseaux sanguins[2]. Les chercheurs ont procédé à l’injection d’une nouvelle biothérapie chez le rat, basée sur la libération d’un facteur de croissance encapsulé spécifique des lymphatiques (VEGF-C).
« Le traitement administré aux rats accélère la réponse lymphangiogénique cardiaque post infarctus et améliore le drainage lymphatique du cœur en 3 semaines. Il a comme effet direct une diminution de l’œdème, de l’inflammation et de la fibrose cardiaques. » explique Ebba Brakenhielm, chargée de recherche à l’Inserm.
« Ces travaux, issus de 4 années de recherches, montrent l’implication importante de ce réseau dans les maladies cardiovasculaires. En effet, les recherches sur ces vaisseaux lymphatiques auparavant invisibles ne se sont développés que depuis 10 ans à peine, et leur rôle dans la physiopathologique est souvent ignoré » conclut Vincent Richard, directeur du laboratoire Inserm à Rouen.
La lymphangiogénese (processus qui guide la formation de vaisseaux lymphatiques) représente ainsi une nouvelle approche thérapeutique non négligeable à explorer dans le cas de l’insuffisance cardiaque et de l’infarctus du myocarde.
[1] Unité 1096 « Nouvelles cibles pharmacologiques de la protection endothéliale et de l’insuffisance cardiaque » (Inserm/Université de Rouen)
[2] 2011: Des microcapsules innovantes pour prévenir les maladies du cœur développées en collaboration avec une équipe CNRS de Reims