Cherchant à mieux comprendre les causes de la schizophrénie, Marie Odile Krebs, de l’Unité 894 Inserm – Université Paris Descartes « Centre de psychiatrie et neurosciences », à l’hôpital Sainte-Anneet Guy A. Rouleau de l’Université de Montréal (Canada) ont utilisé une nouvelle approche pour séquencer l’ADN d’individus atteints de schizophrénie. Le but des chercheurs était d’identifier des variations génétiques susceptibles d’être impliquées dans la schizophrénie. Se démarquant d’une approche « gène candidat », les analyses génétiques ont été faites en examinant l’ensemble de l’exome (1) d’individus atteints de schizophrénie et dont les parents ne montraient aucun signe de la maladie. Premiers résultats de « whole exome » dans la schizophrénie, ces travaux ont été publiés dans la revue Nature Genetics.

© Fotolia
La schizophrénie est une maladie chronique caractérisée par une vaste gamme de symptômes pouvant comprendre des hallucinations et idées délirantes, un retrait social et des troubles cognitifs. Elle touche, selon l’Organisation mondiale de la santé (OMS), 24 millions d’individus à travers le monde.
Afin d’identifier des mutations génétiques associées à la schizophrénie, l’étude menée en partie par les chercheurs de l’Inserm a consisté à analyser l’ensemble de l’exome, environ 20,000 gènes, chez chacun des 42 participants (individus affectés et parents respectifs) en se focalisant sur l’identification de mutations dites« de novo », c’est-à-dire présentes dans le matériel génétique des patients mais absentes chez leurs parents.
Les résultats obtenus démontrent que les mutations de novo sont plus fréquentes chez les individus atteints de schizophrénie que dans la population générale. La fréquence des mutations de novo observée expliquerait en partie le taux élevé de schizophrénie à l’échelle mondiale.
La plupart des gènes identifiés n’ont jamais été auparavant impliqués dans la schizophrénie et représentent donc de nouvelles cibles thérapeutiques potentielles dans une maladie pour laquelle 30 % des personnes atteintes résistent au traitement.
La stratégie clinique développée par les chercheurs est nouvelle. Elle s’intéresse aux cas sans antécédents familiaux, souvent délaissés des études génétiques. Les mutations identifiées apparaissent dans de nombreux gènes différents et permettront de commencer à établir de nouveaux réseaux génétiques pour comprendre comment ces mutations prédisposent à la schizophrénie. « Nos résultats confortent l’idée qu’il n’existerait pas « une » mais « des » schizophrénies, hétérogénéité à laquelle les cliniciens sont quotidiennement confrontés » précise Marie Odile Krebs.
Ces travaux permettront de mieux comprendre cette maladie et apportent un regard nouveau sur la nature des anomalies génétiques pouvant causer la schizophrénie.
Note :
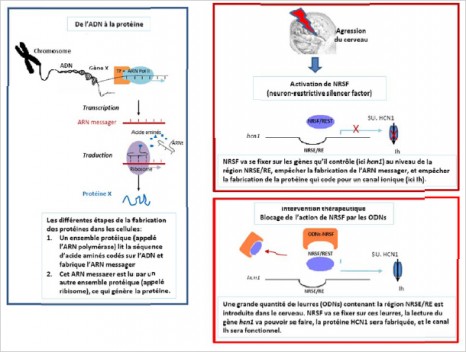
(1) L’exome correspond à l’intégralité des séquences exoniques du génome. Ces séquences sont transcrites en ARN messager puis traduites en protéines pour assurer le bon fonctionnement de l’organisme.