Avec l’augmentation de la longévité des populations humaines, le nombre de patients atteints de maladie d’Alzheimer tend à augmenter en France et dans le monde. Première cause de troubles de la mémoire et des fonctions intellectuelles chez la personne âgée, cette affection constitue donc un enjeu majeur de santé publique. Pour lutter plus vite et plus efficacement contre cette maladie, les chercheurs européens unissent leurs forces. Ainsi, un consortium de 108 laboratoires européens animé par une équipe française (UMR 744 Inserm-Lille2-Institut Pasteur de Lille « Santé publique et épidémiologie moléculaire des maladies liées au vieillissement ») et une équipe britannique (centre de neuropsychiatrie génétique et de génomique, Université de Cardiff) viennent d’identifier cinq nouveaux facteurs de prédisposition génétique impliqués dans le développement de la maladie.
© Fotolia
Ces recherches ont été menées par l’Inserm en collaboration étroite avec le CEA (Centre national de génotypage, CEA-IG-CNG), la Fondation Jean Dausset-CEPH, et un consortium européen regroupant 25 équipes. Ces découvertes ont été obtenues grâce au soutien de la Fondation Plan Alzheimer, qui coordonne le volet recherche du Plan de lutte contre la maladie d’Alzheimer et des maladies apparentées, lancé en février 2008.
Les travaux de ces équipes françaises et anglaises avaient permis en septembre 2009 de découvrir trois nouveaux facteurs de susceptibilité génétique à la maladie d’Alzheimer (CLU, CR1, PICALM) en plus de l’allèle ε4 du gène codant pour l’apolipoprotéine E (APOE) connus depuis plus de 15 ans.
Dans cette nouvelle étude, les chercheurs ont analysé les génomes de 59 176 individus dont 19 870 étaient atteints de la maladie d’Alzheimer et ont ainsi découvert cinq nouveaux gènes de prédisposition : ABCA7, MS4A, EPHA1, CD2AP et CD33. Ils ont également confirmé l’importance du gène BIN1. Ces résultats sont publiés dans la version en ligne de la revue Nature Genetics, du 3 avril 2011.
Ces résultats ont deux intérêts majeurs. Tout d’abord, l’identification de nouveaux gènes associés à la maladie d’Alzheimer va permettre d’élargir le nombre des hypothèses de recherche sur les causes de cette affection. Cette étape est essentielle pour pouvoir identifier de nouvelles pistes de traitements curatifs dans la mesure où les médicaments actuels n’ont que des effets symptomatiques. Par ailleurs, les gènes ainsi identifiés vont aider à mieux cerner le terrain individuel favorisant la survenue de la maladie d’Alzheimer et seront une aide précieuse lorsque des traitements préventifs seront disponibles. La connaissance de ces gènes aidera les chercheurs du monde entier à mieux appréhender les événements conduisant à la destruction des cellules nerveuses et à la perte des fonctions intellectuelles qui caractérisent cette affection.
Dans le même numéro de Nature Genetics, un consortium américain animé par l’Université de Pennsylvanie a également identifié quatre de ces gènes dans une population comparant plus de 11 000 patients et un nombre équivalent de sujets sains. L’ensemble des chercheurs européens et américains ayant contribué à ces découvertes se sont réunis pour la première fois à Paris en Novembre 2010 pour créer le consortium mondial IGAP (International Genomics Alzheimer Project) soutenu par la Fondation Plan Alzheimer en France et l’Alzheimer’s Association aux Etats-Unis. « Cette initiative unique au monde va permettre d’accélérer la lutte contre la maladie, et témoigne de l’importance de ces études collaboratives internationales pour aborder la complexité d’une telle affection », indique Philippe Amouyel, son coordinateur pour la France et le consortium international.
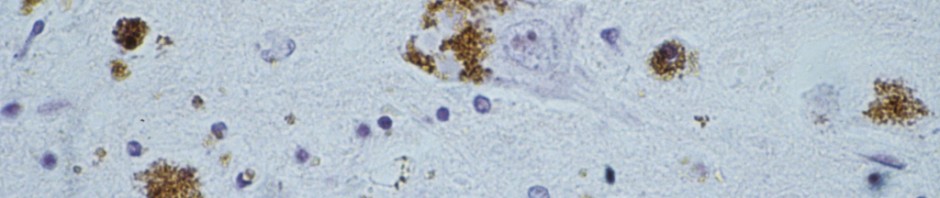
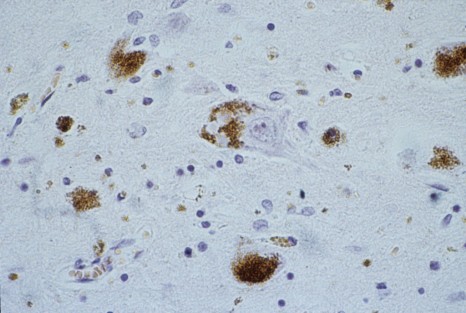
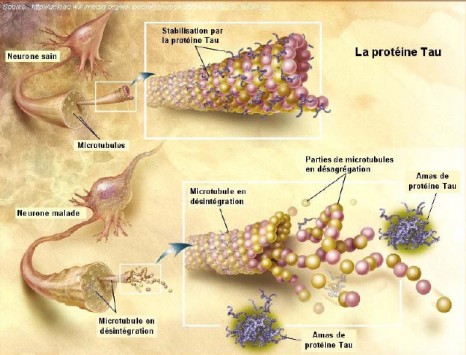
La maladie d’Alzheimer est caractérisée par le développement dans le cerveau de deux types de lésions : les plaques amyloïdes et les dégénérescences neurofibrillaires. Les plaques amyloïdes proviennent de l’accumulation extracellulaire d’un peptide, le peptide β amyloïde (Aβ), dans des zones particulières du cerveau. Les dégénérescences neurofibrillaires sont des lésions intraneuronales provenant de l’agrégation anormale, sous forme de filaments, d’une protéine appelée protéine Tau.
L’identification des gènes qui participent à la survenue de la maladie d’Alzheimer et à son évolution permettra d’aborder plus rapidement les mécanismes physiopathologiques à l’origine de cette affection, d’identifier des protéines et des voies métaboliques cibles de nouveaux traitements et d’offrir des moyens d’identifier les sujets les plus à risque lorsque des traitements préventifs efficaces seront disponibles.