A Toulouse, des chercheurs de l’Inserm dirigés par François Chollet (Unité Inserm 825 « Imagerie cérébrale et handicaps neurologiques » viennent de faire une nouvelle avancée dans le traitement des accidents vasculaires cérébraux. Selon l’essai thérapeutique FLAME (Fluoxetine for motor recovery after acute ischaemic stroke), prescrire l’antidépresseur fluoxétine (Prozac) précocement après un accident vasculaire cérébral peut améliorer la récupération de la motricité et augmenter l’indépendance des patients souvent lourdement touchés. Les résultats de ces travaux sont publiés le 10 janvier 2011 dans The Lancet Neurology.
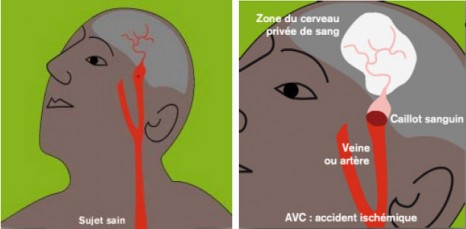
L’accident vasculaire cérébral ischémique (AVC) est consécutif à l’obstruction d’un vaisseau transportant le sang dans le cerveau. Il représente la troisième cause de mortalité et la deuxième cause de handicap de l’adulte en France et touche chaque année environ 130 000 nouveaux patients. Il fait l’objet d’un plan national porté par le ministre de la santé.
L’AVC provoque des dommages parfois irréversibles au cerveau, car les cellules nerveuses ne se renouvellent pas (ou très peu) et leur mort par privation d’oxygène entraîne des pertes fonctionnelles. L’hémiplégie (paralysie de la moitié du corps) et l’hémiparésie (faiblesse de la moitié du corps) constituent les handicaps les plus fréquents après un accident vasculaire cérébral.
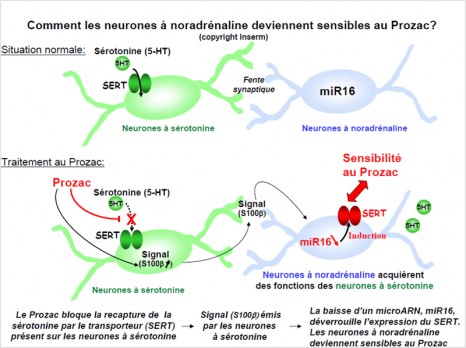
Quelques études préliminaires avaient suggéré que les inhibiteurs de la recapture de la sérotonine pouvaient améliorer la motricité après accident vasculaire cérébral. La même équipe avait montré en 2001(1), sur un petit nombre de patients, que ce médicament était susceptible d’améliorer la motricité en augmentant l’activation et l’excitabilité des neurones des aires motrices cérébrales. Cette première étude a conduit à la réalisation de l’essai clinique dont les résultats sont publiés aujourd’hui.
L’objectif de L’essai FLAME (Fluoxetine for motor recovery after acute ischaemic stroke) était de déterminer si la fluoxétine pouvait augmenter la récupération de la motricité dans un groupe de patients plus important.
© Inserm, F. Koulikoff
Entre mars 2005 et juin 2009, 118 patients hospitalisés pour hémiplégie au sein de neuf unités neurovasculaires en France ont pris 20mg de fluoxétine par jour (59 patients) ou un placebo (59 patients) pendant trois mois après la survenue d’un accident vasculaire cérébral ischémique. Tous les patients ont bénéficié d’une rééducation. Des tests moteurs ont été effectués au début puis au bout de trois mois de traitement. Cette évaluation de la motricité incluait à la fois la réalisation de mouvements simples du membre supérieur et du membre inférieur (flexion extension des doigts, du poignet, du pied…) ainsi que des gestes plus complexes (mettre la main dans le dos, attraper un objet…) inclus dans une échelle d’évaluation motrice validée par la communauté scientifique.
Une récupération motrice avérée
Dans les jours et les mois qui suivent l’accident, tous les patients récupèrent une partie de leurs capacités de manière spontanée. Toutefois l’ampleur de la récupération fonctionnelle reste imprévisible.
Or, une amélioration plus importante de la motricité a été observée chez les patients sous fluoxétine par rapport à ceux sous placebo. Ce gain était présent à la fois au niveau de la récupération motrice des bras et des jambes. De manière générale, la régression de la paralysie est supérieure chez les patients sous fluoxétine par rapport aux personnes sous placebo.
Parallèlement après trois mois de traitement le nombre de patients indépendants dans la vie quotidienne (marche, toilette, gestes courants, déplacements…) était plus important sous fluoxétine que sous placebo.
Globalement le traitement a été bien toléré et les effets secondaires limités. Des troubles digestifs transitoires ont été observés plus fréquemment sous fluoxétine mais la survenue d’une dépression nerveuse s’est avérée plus fréquente sous placebo suggérant que la fluoxétine peut prévenir les syndromes dépressifs post AVC.
Pour François Chollet et ses collaborateurs : « L’effet positif du médicament sur la récupération de la motricité de ces patients suggère que l’action de la Fluoxétine, sur plasticité des neurones et non pas sur les vaisseaux constitue une nouvelle voie thérapeutique au moment de la phase aiguë des accidents vasculaires cérébraux ». Ils ajoutent : « la fluoxétine est un médicament relativement bien toléré, dans le domaine public et dont le coût est raisonnable. »
Des développements sont à prévoir dans un futur proche. Il faut évaluer l’effet à plus long terme, la durée de prescription optimale, l’effet sur les fonctions neurologiques autres que la motricité, l’opportunité de traiter les accidents vasculaires hémorragiques notamment. La question de l’autorisation de mise sur le marché dans cette indication se posera à court ou moyen terme.
Cet essai a reçu la promotion du CHU de Toulouse dans le cadre d’un financement public par le PHRC national.
(1) Le prozac et consorts au service des attaques cérébrales-janvier 2002