Les chercheurs de l’Inserm ont réussi à filmer des molécules biologiques d’à peine 5 nanomètres (1) en mouvement. Cette prouesse technique encore inenvisageable il y a quelques années a été réalisée par l’équipe de chercheurs dirigée par Simon Scheuring (Unité Inserm 1006 « Structure et assemblage des protéines membranaires dans la membrane native par microscopie à force atomique ») et s’appuie sur une méthode totalement inédite basée sur la microscopie à force atomique. Grâce à cette technique, les chercheurs peuvent maintenant visualiser non seulement des molécules infiniment petites mais surtout leurs interactions avec leur environnement. Les champs d’applications sont nombreux puisque le dysfonctionnement des protéines de la membrane cellulaire est impliqué dans de nombreuses pathologies. Ces travaux sont parus dans la revue Nature Nanotechnology
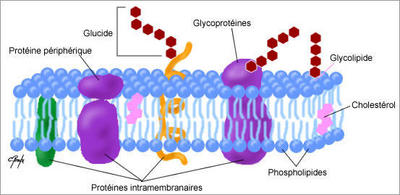
La membrane plasmique contrôle les échanges de la cellule avec son environnement. Pour fonctionner correctement et permettre le passage d’eau, de sucres, de substances nutritives ou encore l’évacuation des déchets par exemple, des protéines tapissent toute la surface des membranes cellulaires. La fonction de ces protéines membranaires dépend de leur position et des interactions avec les autres molécules présentes dans leur environnement.
Cependant, jusqu’à présent, il n’a pas été possible d’étudier simultanément la structure et la dynamique des membranes biologiques. Du fait de son épaisseur (environ 5 nanomètres), la membrane des cellules n’est pas visible via les techniques classiques de microscopie. L’astuce utilisée depuis longtemps par les chercheurs est d’utiliser des marqueurs fluorescents pour suivre ces molécules quasi invisibles. « Mais, même si l’on peut suivre la molécule d’intérêt, on ne peut pas voir son environnement. Et, la protéine de fluorescence parfois assez « grosse » peut parfois modifier la fonction de la molécule que l’on observe » explique Simon Scheuring.
Grâce à cette nouvelle technique de microscopie à force atomique à haute vitesse, les chercheurs de l’Inserm ont caractérisé le mouvement de protéines membranaires et étudié leur diffusion, leur dynamique et leur organisation. Les chercheurs ont pu acquérir des films qui montrent avec une résolution sans précédent la dynamique de ces protéines dans leur environnement. Et, là où seuls les acteurs figés avaient des chances d’apparaître sur la photo, les protéines mobiles peuvent finalement être visualisées au cours de leur déplacement.
Puis, ils ont réalisé une carte des interactions potentielles et le déplacement pour une protéine membranaire « Si les molécules ont de l’espace autour d’elles, elles se déplacent vite. En revanche, si l’espace qui l’entoure est dense, la probabilité de rencontrer d’autres molécules est plus forte, s’ensuivent alors des interactions. Ces partenariats sont parfois indispensables au fonctionnement correct des protéines » explique Simon Scheuring. C’est ce qui explique qu’avec seulement environ 20 000 gènes (donc environ 20 000 protéines), un grand nombre de fonctions cellulaires peuvent être assurées.
Cette première étape fondamentale pourrait trouver de nombreuses applications médicales dès lors que les chercheurs s’intéresseront à des protéines impliquées dans certaines pathologies. Les protéines membranaires représentent près de 60 % des cibles des médicaments. Aussi, connaître les mécanismes en œuvre dans ces interactions permettra à terme d’interférer avec eux et pouvoir moduler les fonctions biologiques correspondantes pour mieux les étudier ou les contrôler. A ce jour, une étude sur les interactions des aquaporines dans la membrane du cristallin de l’œil par microscopie à force atomique à haute vitesse est en cours d’évaluation scientifique.