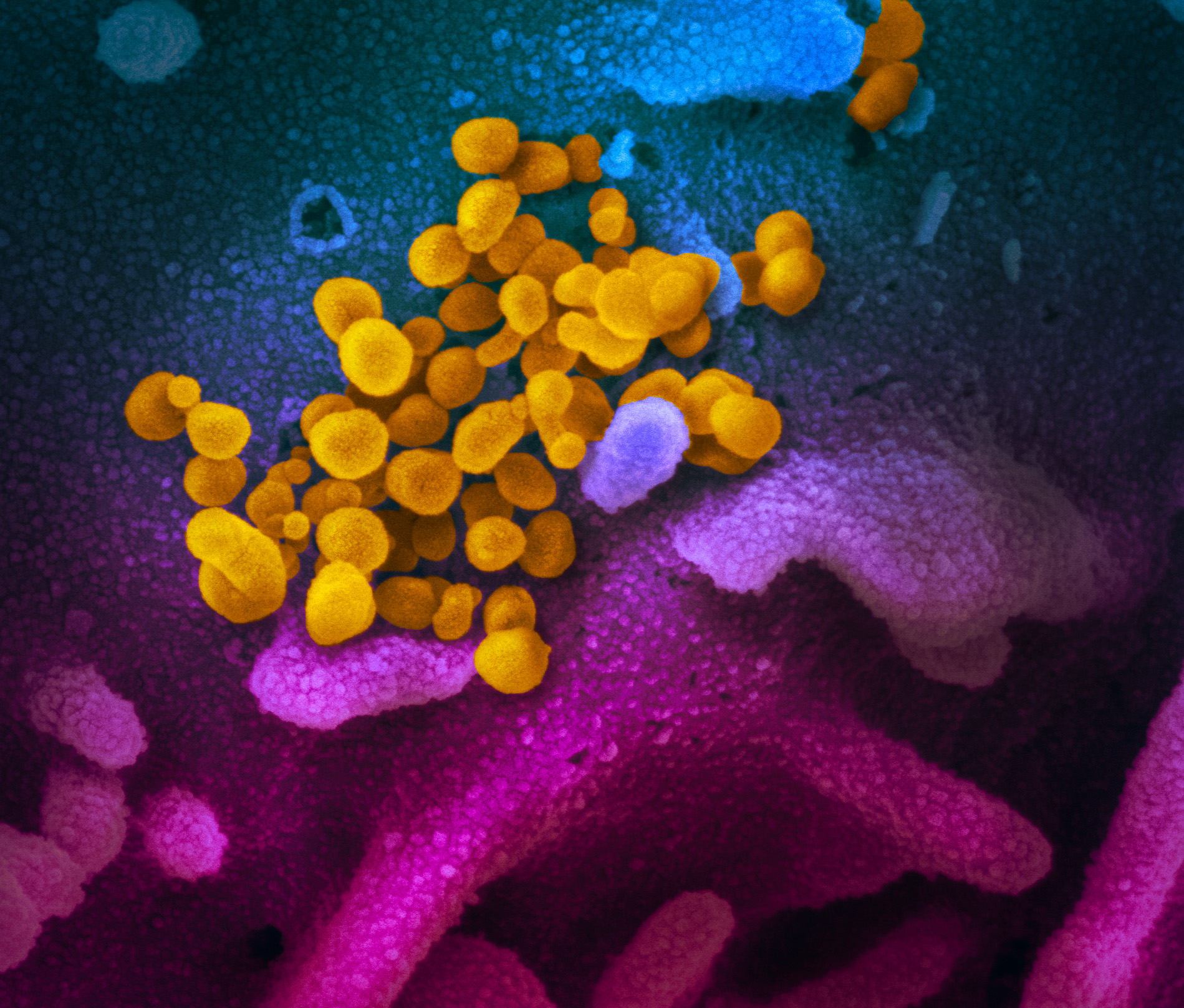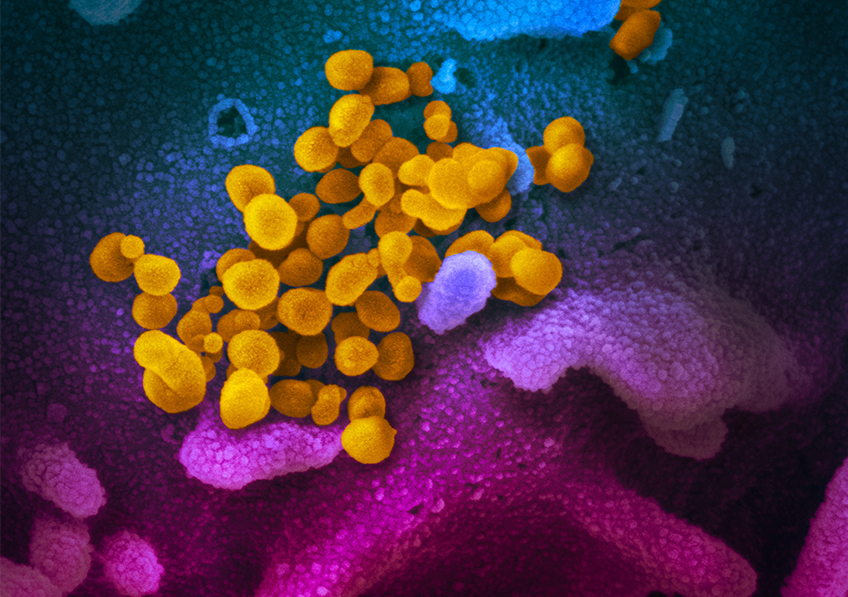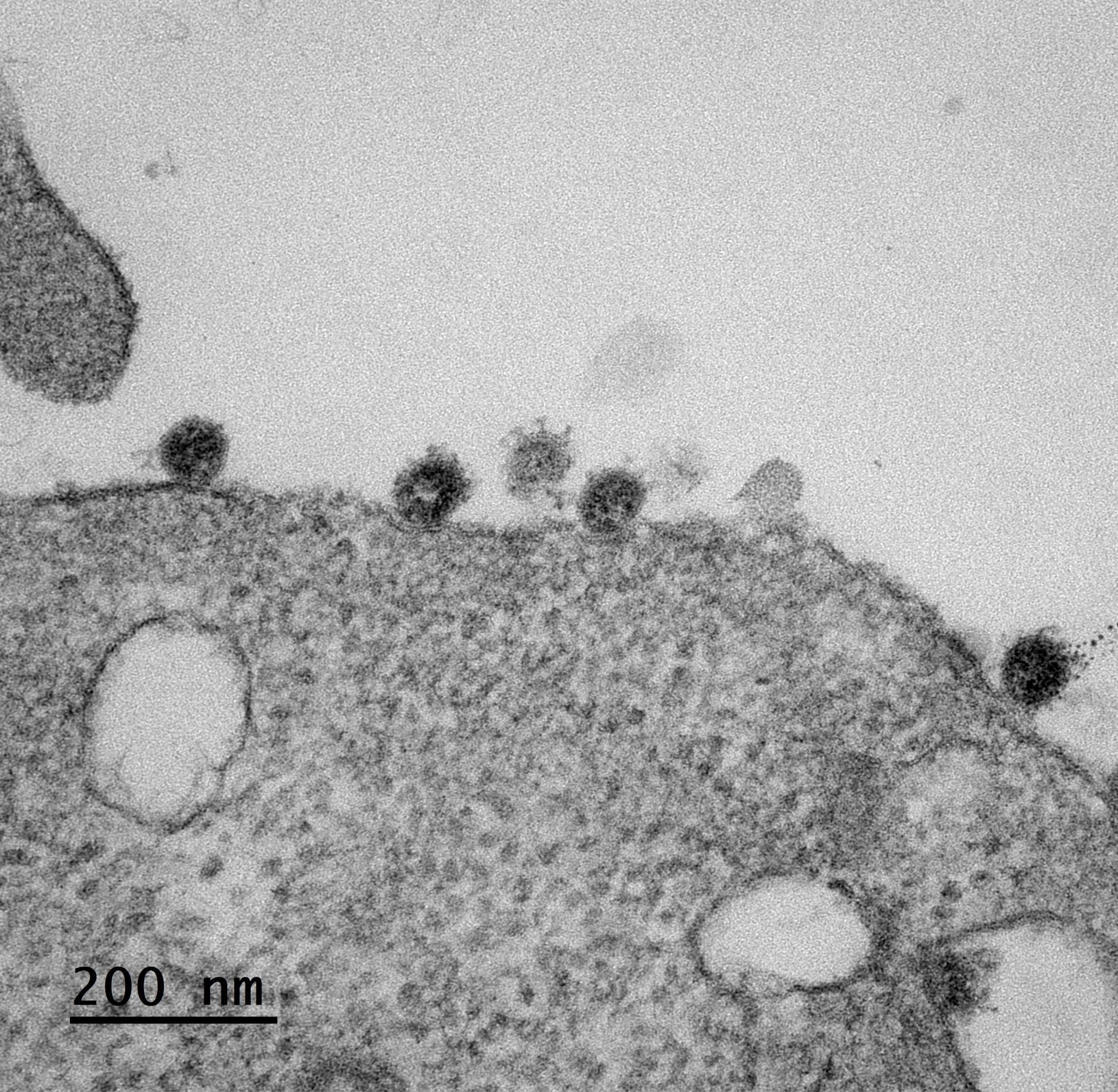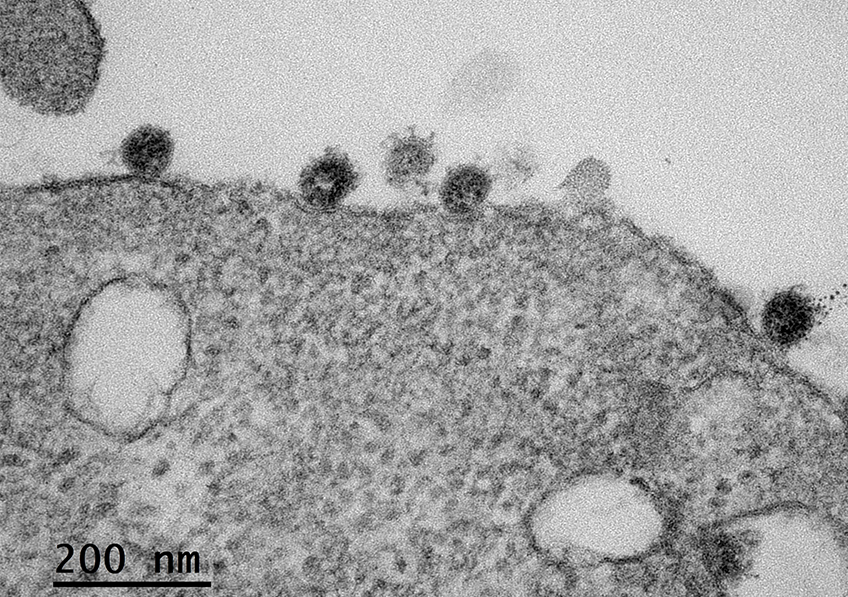
Des chercheurs de Sorbonne Université, de l’hôpital de la Pitié-Salpêtrière AP-HP, de l’Inserm et de l’Institut Pasteur ont mené des travaux dans le but d’étudier la persistance des anticorps neutralisants le SARS-CoV-2 chez des professionnels de santé ayant fait une forme modérée de COVID-19. Ces travaux qui seront publiés le 8 février 2021 dans Nature Communications, montrent que la réponse humorale[1] neutralisant le SARS-CoV-2 est associée aux anticorps dirigés contre le récepteur de la protéine S du virus et que ce caractère neutralisant diminue au cours du temps, pouvant même disparaître dès deux mois après l’infection naturelle.
A l’heure de la vaccination, les corrélats de protection[2] contre le SARS-CoV-2 ne sont pas encore clairement définis et posent la question du taux minimal d’anticorps nécessaire afin d’être protégé de l’infection par le SARS-CoV-2 ou des formes sévères de COVID-19. Ces corrélats sont très souvent associés aux anticorps neutralisants, des anticorps particuliers permettant de prévenir l’infection en bloquant l’entrée du virus dans ses cellules cibles.
Il apparaissait donc important aux chercheurs et biologistes du service de virologie de l’hôpital de la Pitié-Salpêtrière AP-HP et de l’équipe THERAVIR[3] de l’Institut Pierre Louis d’Epidémiologie et de Santé Publique (IPLESP-Sorbonne Université/Inserm), en collaboration avec plusieurs services du groupe hospitalo-universitaire AP-HP-Sorbonne Université et de l’Institut Pasteur[4], d’étudier au cours du temps l’apparition et la persistance de différents type d’anticorps (IgG, IgA et IgM) ainsi que leur caractère neutralisant chez des professionnels de santé ayant fait une forme modérée de COVID-19.
Les résultats de cette étude montrent que l’ensemble de ces professionnels a développé des anticorps entre 2 et 4 semaines après le début des symptômes ainsi qu’une réponse neutralisante au SARS-CoV-2.
Cette réponse neutralisante était associée aux anticorps de type IgG et IgA dirigés contre la protéine S du virus et plus particulièrement, le receptor binding domain, (RBD) responsable de l’interaction avec l’angiotensin converting enzyme 2 (ACE2), le récepteur cellulaire du virus (qui lui permet de s’arrimer aux cellules pour les infecter).Les chercheurs ont montré que les anticorps IgA systémiques, essentiels à la protection des muqueuses, étaient les anticorps principalement responsables de la réponse neutralisante précoce. Cependant, cette réponse neutralisante déclinait rapidement dès 2 mois après le début des symptômes et pouvait même disparaître chez 15% des professionnels, associés au déclin et à la disparition des anticorps IgA dans le sérum.
Malgré cette diminution de la réponse neutralisante, le taux des anticorps IgG, habituellement considérés comme protecteurs et à longue durée de vie se maintenait entre 2 et 3 mois après le début des signes.
En conclusion, cette étude met en évidence l’importance de la protection précoce médiée par les anticorps IgA et pose la question de la persistance à long terme des anticorps neutralisants le SARS-CoV-2 et donc de l’immunité protectrice au cours du temps chez les professionnels de santé ayant fait une forme modérée de COVID-19. Les résultats portant exclusivement sur l’immunité humorale, ils ne prennent pas en compte l’immunité cellulaire générée en réponse à l’infection par le SARS-CoV-2. Par la suite, il serait donc intéressant d’évaluer la persistance d’une réponse cellulaire mémoire chez ces professionnels ainsi que la réponse anticorps IgA au niveau des muqueuses respiratoires.
Ces travaux sont en faveur d’un maintien des mesures de protection et des gestes barrières et de l’intérêt de la vaccination des professionnels de santé ayant fait un COVID-19.
[1] En opposition à l’immunité cellulaire, la réponse humorale est l’immunité adaptative par production d’anticorps.
[2] Un corrélat de protection est une preuve indirecte, le plus souvent sérologique, de l’existence d’une protection contre une maladie donnée.
[3] Equipe THERAVIR : Stratégies thérapeutiques contre l’infection VIH et les maladies virales associées
[4] Unité virus et immunité