Le projet de recherche HOMAGE (Heart OMics in AGEing), coordonné par l’Inserm, vient d’obtenir un financement de la Commission Européenne pour une durée de 6 ans. L’objectif étant d’identifier et de valider les biomarqueurs spécifiques de l’insuffisance cardiaque en vue de prévenir le développement de la maladie chez des patients âgés présentant un risque cardiovasculaire élevé. Dix-sept équipes de recherche venant de 10 pays vont joindre leurs efforts dans le but de proposer de nouvelles voies thérapeutiques ciblées pour traiter les patients à risque. Le projet repose sur une approche innovante dite « omique » qui vise à étudier simultanément un grand nombre de gènes, protéines ou métabolites.
Les 17 partenaires seront réunis à Nancy le 22 février pour le lancement du projet HOMAGE.
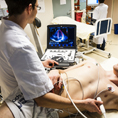
Faiez Zannad, chercheur de l’unité Inserm U1116, Centre d’Investigation Clinique P. Drouin Inserm 9501 à Nancy, coordinateur du projet HOMAGE se réjouit de l’obtention des 12 millions d’euros qui seront consacrés à combattre l’insuffisance cardiaque, maladie grave affectant les capacités du myocarde et qui touche plus de 6.5 millions de personnes en Europe. En effet, l’incidence de l’insuffisance cardiaque prend une part de plus en plus importante dans les pays industrialisés du fait du vieillissement de la population et de l’explosion des facteurs de risque cardiovasculaires tels que le diabète, l’obésité et l’hypertension artérielle.
L’insuffisance cardiaque est une des causes majeures de mortalité et de morbidité dans le monde et reste la cause d’hospitalisation la plus fréquente chez les patients âgés de plus de 65 ans.
On estime le coût socio-économique de sa prise en charge à près de 1,5 milliards d’euros par an en France[1].
Photo : ©Serimedis/Inserm
Malgré des progrès importants dans le traitement, le développement de dispositifs médicaux et la prise en charge des patients, le diagnostic de l’insuffisance cardiaque est souvent difficile notamment chez les patients atteints de pathologies multiples. Des stratégies de dépistage fondées sur la mesure de la pression artérielle, de la glycémie ou du cholestérol sanguin ont une certaine utilité pour dépister les patients à risque mais elles sont limitées car peu sensibles et spécifiques. Au cours de cette dernière décennie, plusieurs biomarqueurs diagnostiques de l’insuffisance cardiaque tels que les peptides natriurétiques ont été identifiés mais leur potentiel prédictif reste faible.
L’objectif à terme du projet HOMAGE est de proposer des marqueurs plus spécifiques et plus sensibles qui pourraient permettre un dépistage plus précoce de la maladie chez les patients à risque.
Pour y parvenir, les chercheurs ont opté pour une approche « omique ». Celle-ci repose sur la validation de candidats biomarqueurs prometteurs et fiables, identifiés par de multiples approches croisées sur de très grandes quantités de données (génomiques, protéomiques, transcriptomiques et métabolomiques). Elles permettront par la suite de connaître de nouveaux mécanismes physiopathologiques, voies de régulations et nouvelles cibles thérapeutiques dans la prévention et/ou le diagnostic de l’insuffisance cardiaque chez les personnes âgées.
Pour cette étude le consortium HOMAGE aura accès à plusieurs cohortes rassemblant plus de 30 000 patients. Les chercheurs européens identifieront dans un premier temps les candidats biomarqueurs sanguins. Ils étudieront également leur valeur prédictive pour les co-morbidités caractéristiques de l’insuffisance cardiaque et du vieillissement (insuffisance rénale, troubles cognitifs…). Dans un deuxième temps, ils étudieront au cours d’un essai thérapeutique l’individualisation d’un traitement préventif de l’insuffisance cardiaque.
Cet essai permettra ainsi d’identifier les malades ayant la plus grande probabilité de répondre au traitement avec le meilleur rapport bénéfice/risque et de définir de nouvelles cibles thérapeutiques.
Les 17 partenaires du projet HOMAGE : www.homage-hf.eu (en ligne le 21 février)
Inserm, France : https://www.inserm.fr/
Inserm U942/ Biomarqueurs et maladies cardiaques, France
Inserm UMR 1048/ Equipe 7, France
Inserm U744/ Recherche des Déterminants Moléculaires des Maladies Cardiovasculaires, France
Inserm Transfert, France : https://www.inserm-transfert.fr/
European Drug Development Hub, France : https://www.fondationtransplantation.org
ACS Biomarker, Pays-Bas : https://acsbiomarker.com/
Randox Testing Service, Royaume-Uni : https://www.randoxtestingservices.com/
Medical University of Graz, Autriche : https://www.meduni-graz.at/en/
University of Manchester, Royaume-Uni : www.manchester.ac.uk
Fundación para la Investigación Médica Aplicada, Espagne : www.cima.es
University College Dublin, Irlande : www.ucd.ie
University of Hull, Royaume-Uni : www.hull.ac.uk
Maastricht University, Pays-Bas : https://www.maastrichtuniversity.nl/
Istituto di Ricerche Farmacologiche ‘Mario Negri’, Italie : https://www.marionegri.it/mn/en/
Hannover Medical School, Allemagne : https://www.mh-hannover.de
University of Leuven, Belgique : www.kuleuven.be/english/
London School of Hygiene, Royaume-Uni : https://www.lshtm.ac.uk/
Emory University, Etats Unis : https://www.emory.edu
University of Glasgow, Royaume-Uni : https://www.gla.ac.uk/
Institutions collaboratrices:
The Trustees of Boston University, National Heart, Lung, and Blood Institute’s Framingham Heart Study, Etats Unis
Imperial College, Royaume-Uni
Steno Diabetes Center (Novo Nordisk), Danemark
[1] Fédération Française de Cardiologie