Malgré les progrès de la médecine régénérative, avec l’âge, la peau perd ses propriétés de manière irréversible. L’équipe ATIP-Avenir « Homéostasie et tumorigenèse épidermiques » dirigée par Chloé Féral, chargée de recherche à l’Inserm à l’Institut de recherche sur le cancer et le vieillissement (Inserm/CNRS/Université Sophia Antipolis), vient de définir les mécanismes cellulaires et moléculaires impliqués dans le maintien des cellules de la peau et la cicatrisation cutanée au cours du vieillissement. Ces mécanismes, décrits in vivo chez la souris, font intervenir la molécule CD98hc, un acteur du renouvellement de l’épiderme qui pourrait constituer un indicateur de la capacité de la peau à se régénérer.
Ces travaux sont publiés dans la revue The Journal of Experimental Medicine.
L’épiderme, la couche superficielle de la peau, est composée en majorité de cellules appelées kératinocytes qui se renouvellent continuellement selon un cycle de 21 jours chez l’Homme. Ces cellules reposent sur une membrane constituée de composants de la matrice extracellulaire qui assurent la jonction avec le derme, la couche profonde de la peau (cf. schéma plus bas). Le renouvellement de l’épiderme est assuré par la prolifération et la différenciation cellulaires qui maintiennent l’équilibre des tissus adultes. L’altération de cet équilibre, indispensable au bon fonctionnement des tissus et que l’on appelle « homéostasie », est responsable des changements physiques associés au vieillissement : flétrissement de la peau dû à la réduction de la prolifération des cellules épidermiques, défaut de cicatrisation en cas de plaies, perte de poils…
L’équipe ATIP-Avenir « Homéostasie et tumorigenèse épidermiques » dirigée par Chloé Féral, chargée de recherche à l’Inserm, a étudié les nombreux facteurs cellulaires impliqués dans le maintien de cet équilibre, en particulier CD98hc, une molécule connue pour son interaction avec des récepteurs en cause dans le vieillissement cutané. Avec l’âge, l’activité du transporteur CD98hc et des intégrines, ces récepteurs liés aux composants de la matrice extra cellulaire, est perturbée. Cependant, les mécanismes impliqués n’avaient jusqu’à présent pas été élucidés.
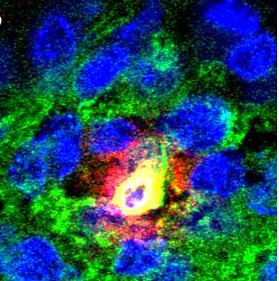
Dans ce travail, les chercheurs ont montré in vivo chez la souris, que la délétion du gène CD98hc (qui code pour le transporteur CD98hc), perturbe l’équilibre cutané et le processus de cicatrisation. En modifiant la prolifération et la migration des cellules, la délétion de ce gène induit également un défaut du cycle du follicule pileux. Les chercheurs ont décrypté l’ensemble des mécanismes complexes associés à CD98hc, en particulier la dérégulation des intégrines induite par l’absence de cette molécule in vivo. Ils confirment notamment ce qui avait été décrit in vitro : le transporteur d’acides aminés CD98hc module le signal intégrine, essentiel au renouvellement de la peau. Par ce biais, CD98hc participerait activement au renouvellement cutané via le recrutement efficace et massif des cellules épidermiques en cas de besoin (cicatrisation d’une plaie par exemple).
« CD98hc apparait nécessaire au renouvellement rapide et efficace de l’épiderme. La baisse de son expression, constatée in vivo chez la souris âgée, confirme son rôle dans le maintien des tissus, le cycle du follicule pileux et la cicatrisation, perturbés avec l’âge » affirme Chloé Féral. Le statut du transporteur CD98hc in vivo pourrait être un indicateur de la capacité de la peau à se régénérer », conclut la chercheuse.
© I-STEM
Le renouvellement de l’épiderme est assuré par les kératinocytes souches.- Ces derniers possèdent deux propriétés : celle de se diviser activement et celle de se différencier. Chaque kératinocyte donne naissance à deux cellules filles identiques. L’une reste sur place pour se diviser à nouveau tandis que l’autre migre vers la couche supérieure, la couche de différenciation, où elle va donner les différents types de cellules épidermiques.