Le cancer du poumon est un cancer dont le taux de survie 5 ans après le diagnostic est très faible. La mise en place du traitement le plus adéquat est rendue difficile par le caractère très hétérogène des tumeurs et de leur pronostic, au sein d’un même stade de développement. Un groupe de chercheurs dirigé par Patricia Forgez du centre de recherche Saint-Antoine, Inserm-UPMC « Laboratoire de signalisation cellulaire et carcinogénèse » vient de mettre en évidence, en collaboration avec le service de chirurgie thoracique de l’Hôtel-Dieu à Paris (AP-HP), un nouveau biomarqueur, pronostic de l’évolution de la tumeur. Cette protéine et son récepteur, dont la présence favorise la progression de la tumeur et l’apparition de métastases, ont fait l’objet d’un dépôt de brevet Inserm/AP-HP et pourraient être détectés de manière simple en laboratoire d’analyse. Ces travaux sont publiés dans l’édition du 1er septembre de Clinical Cancer Research.
Première cause de mortalité par cancer dans les pays occidentaux, le cancer du poumon est en légère diminution chez les hommes mais augmente fortement chez les femmes (+ 4 % par an). Principale cause, le tabagisme, loin derrière l’exposition professionnelle aux carcinogènes, le tabagisme passif et les polluants issus de l’environnement.
Le cancer bronchique est silencieux et de très mauvais pronostic avec un taux de survie de 15 % à 5 ans. Seuls un tiers des cas, les moins avancés, sont éligibles à la chirurgie ; les autres cas, souvent plus avancés au moment où ils se présentent au clinicien, répondent mal aux traitements, y compris les plus récents.
Les tumeurs du poumon sont très hétérogènes, y compris dans les sous-types biologiques. En conséquence, à l’intérieur d’un même stade tumoral, le pronostic varie fortement d’un patient à l’autre en raison de facteurs génétiques et environnementaux propres à l’individu, mais également de facteurs intrinsèques à la tumeur qui lui confèrent un caractère plus ou moins agressif.
Comprendre les facteurs responsables de la progression d’une tumeur et découvrir de nouveaux marqueurs pronostics de son évolution constitue un réel enjeu pour les médecins et les patients dans la mesure où les traitements pourraient ainsi être mieux adaptés à chaque cas.
Le Dr Forgez et son groupe avaient préalablement mis en évidence que le récepteur principal d’une protéine d’origine gastro-intestinale, la neurotensine, retrouvé dans une forte proportion de tumeurs, favorisait dans certaines conditions la progression tumorale.
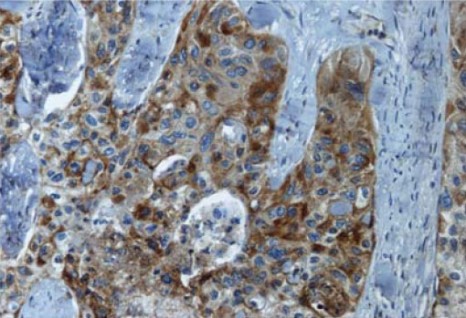
Les chercheurs montrent aujourd’hui dans une série de 136 patients présentant un adénocarcinome pulmonaire de stade 1, que ceux dont les tumeurs expriment le récepteur principal à la neurotensine, ont un moins bon pronostic en termes de survie à 5 ans. L’activation de ce récepteur favorise en effet fortement la croissance des tumeurs et l’émergence de métastases. A stade égal de développement tumoral, la présence ou non de ce récepteur constitue donc un biomarqueur pronostic d’une évolution plus ou moins favorable.
La procédure de détection de ce récepteur est simple et peu coûteuse ; après la confirmation de ces résultats sur une série plus importante de patients, (étude actuellement menée par le même groupe) elle pourrait être utilisée en routine dans les laboratoires d’analyse biologique pour l’identification des patients à haut risque de récidive. Il s’agit de définir pour ceux-ci une prise en charge plus adaptée en termes de stratégie thérapeutique postopératoire et de surveillance.
Deux brevets ont été déposés conjointement par l’Inserm et l’AP-HP sur ce biomarqueur ; ils permettront d’intéresser d’éventuels investisseurs des industries pharmaceutiques et des biotechnologies, tant sur le plan du développement d’un kit de détection que celui du développement des thérapies innovantes visant à diminuer l’agressivité tumorale.
« Comme pour d’autres cancers tels que le cancer du côlon, les leucémies et lymphomes, pour lesquels des marqueurs génétiques spécifiques débouchent sur des décisions thérapeutiques adaptées, les cancers du poumon commencent à être démembrés en plusieurs maladies de pronostics et de traitements différents » précise Fabien Calvo, directeur de l’Institut Cancer de l’Inserm.
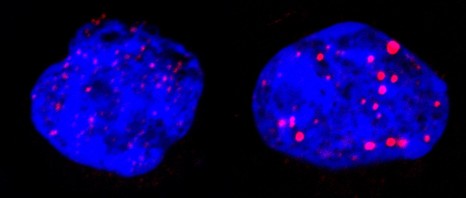
Adénocarcinome bronchique. Marquage du récepteur de la neurotensine © Inserm, U938