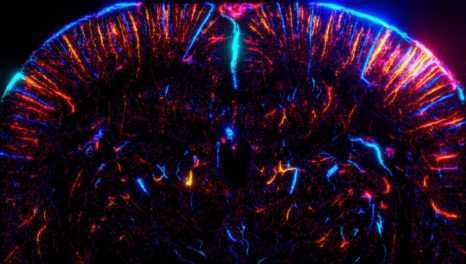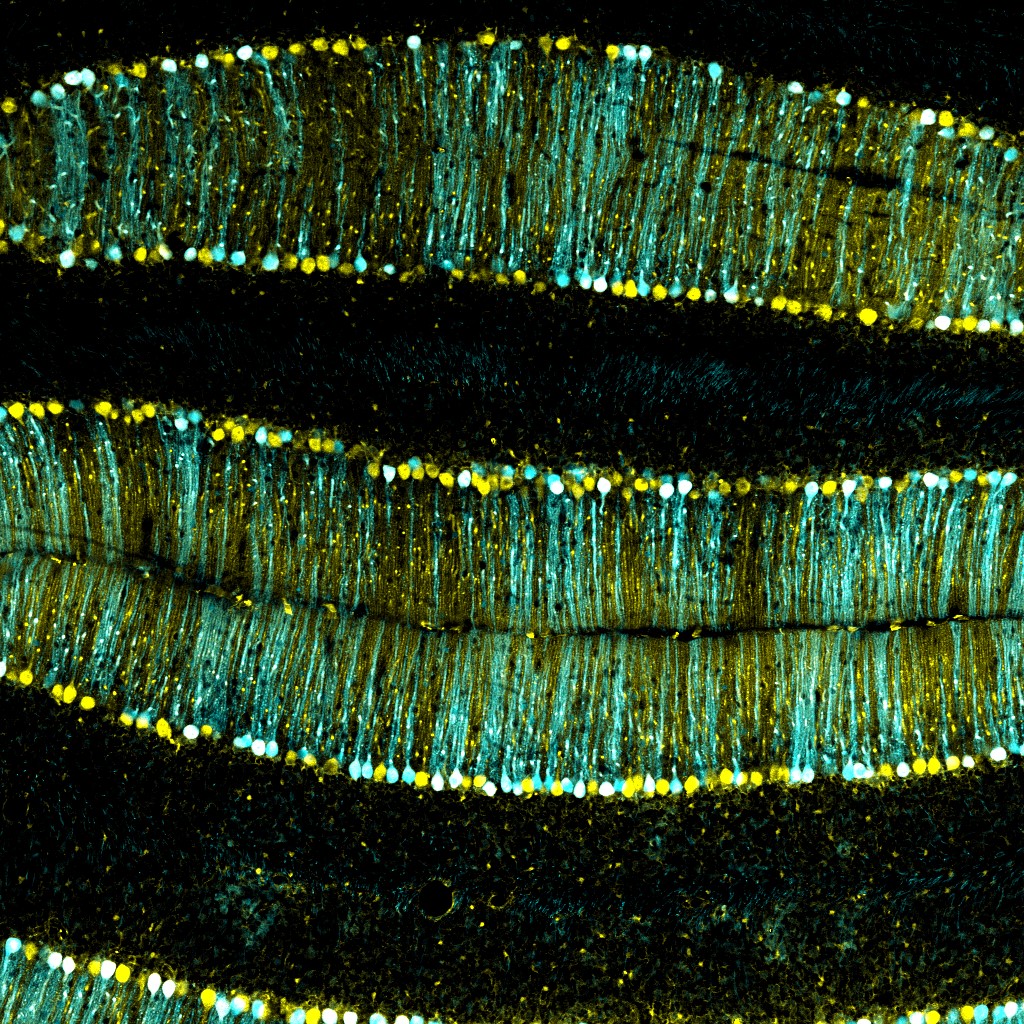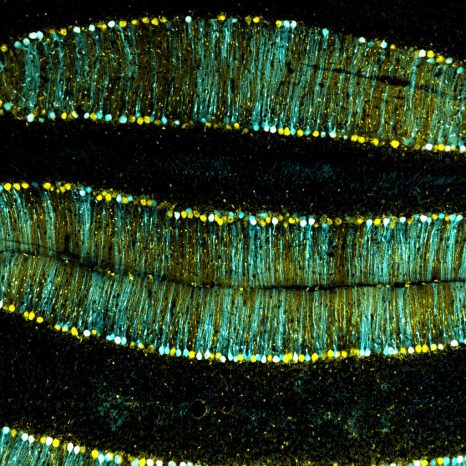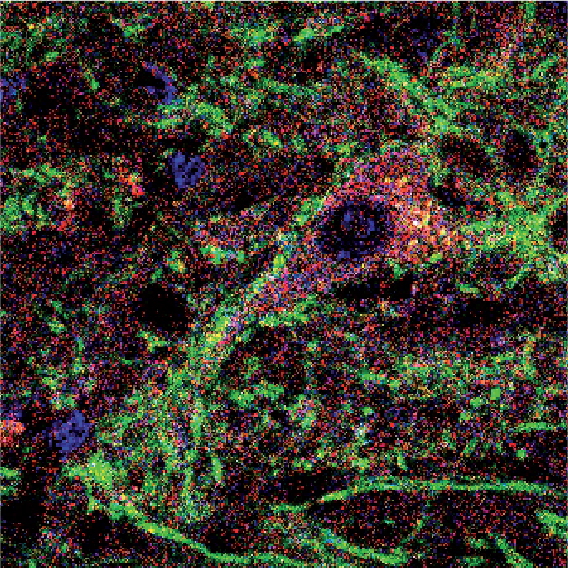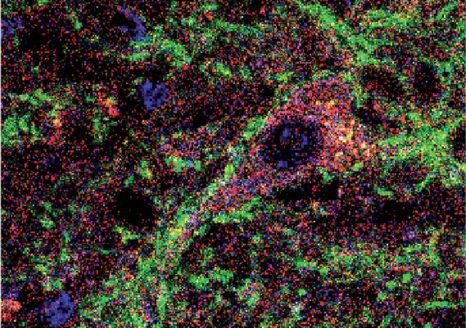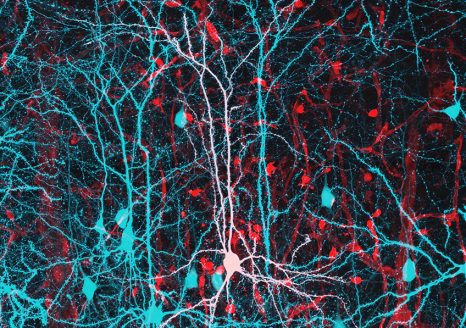
Neurones pyramidaux du cortex à 21 jours après la naissance dont l’activité et la morphologie sont similaires chez les souris contrôles et modèles de la maladie de Huntington alors qu’une semaine après la naissance des altérations sont observées. © Barbara Yal Braz (BY Braz)
Si les symptômes de la maladie de Huntington se manifestent généralement entre 30 et 50 ans, des travaux ont montré que la maladie impactait le développement cérébral dès le stade embryonnaire. Une équipe de chercheuses et chercheurs de l’Inserm et de l’Université Grenoble Alpes, au sein du Grenoble Institut des Neurosciences, a mis en évidence, chez la souris, un impact de la maladie sur la qualité de la transmission nerveuse dans certains neurones très tôt après la naissance avec des conséquences anatomiques et comportementales. Ces travaux à paraître dans Science montrent aussi l’intérêt d’un traitement précoce avec une molécule favorisant la transmission nerveuse, qui restaure les défauts néonataux observés et retarde l’apparition de la maladie à l’âge adulte. Ils ouvrent ainsi de nouvelles pistes de recherche sur la prise en charge thérapeutique de la maladie de Huntington chez l’humain.
La maladie de Huntington est une maladie génétique rare et héréditaire du système nerveux central qui se manifeste par des troubles psychiatriques, cognitifs et moteurs qui s’aggravent progressivement. Elle est due à la mutation du gène codant pour une protéine nommée « huntingtine », essentielle au bon fonctionnement des neurones. La maladie se déclenchant tardivement – habituellement entre les âges de 30 et 50 ans, l’impact de la mutation de la huntingtine sur le neurodéveloppement pré- et postnatal a été jusqu’à présent peu étudié.
En 2020, Sandrine Humbert, directrice de recherche Inserm, a codirigé des travaux mettant en évidence des anomalies cérébrales dans des cerveaux d’embryons humains porteurs de la mutation responsable de la maladie de Huntington. Plusieurs fonctions régulées par l’activité neuronale apparaissaient impactées, suggérant une altération de la transmission nerveuse.
Forte de ces observations, l’équipe de Sandrine Humbert au Grenoble Institut des Neurosciences (Inserm/Université Grenoble-Alpes) s’est intéressée à la mise en place des circuits neuronaux et aux comportements cognitifs et sensori-moteurs chez des souriceaux modèles de la maladie de Huntington.
Les chercheuses et chercheurs ont observé différentes altérations chez les souriceaux Huntington : les neurones pyramidaux (voir encadré) de leur cortex cérébral présentaient des défauts morphologiques et de transmission synaptique, associés à des altérations du comportement. Toutefois, après 21 jours de vie, ils retrouvaient une physiologie et une morphologie apparemment similaires à celle des souris saines.
« Ces observations témoignent, dans la maladie de Huntington, de l’altération précoce de la transmission excitatrice des neurones pyramidaux, précise Sandrine Humbert, mais cette déficience temporaire est corrigée pendant le premier mois de vie. »
Pour autant ces compensations ne fonctionneraient qu’un temps puisqu’à partir de 4 à 5 semaines les souris Huntington développent certains signes de la maladie.
À propos des neurones pyramidaux
Ces neurones jouent un rôle majeur dans le contrôle des mouvements volontaires. Ils tiennent leur nom de leur corps triangulaire d’où partent de longues et nombreuses ramifications (appelées « dendrites ») leur donnant une forme rappelant un arbre (d’où l’expression « arbre dendritique ») et qui leur permet de recevoir des signaux excitateurs. À leur base, un long prolongement appelé « axone », permet de transmettre l’information nerveuse à d’autres neurones par son extrémité appelée « synapse ».
Les scientifiques ont ensuite émis l’hypothèse qu’une restauration des défauts transitoires observés au cours de la première semaine de vie pourrait influencer l’apparition de la maladie à l’âge adulte. Pour vérifier cette supposition, ils ont utilisé une molécule thérapeutique de la classe des ampakines, le CX516, connue pour faciliter la transmission nerveuse. Ce traitement néonatal a permis de restaurer l’activité neuronale et les capacités cognitives et sensori-motrices des souriceaux Huntington, et surtout, il les a empêchés de développer les signes caractéristiques de la maladie à l’âge adulte.
« Ces travaux montrent une altération précoce de la transmission nerveuse et de la morphologie des neurones du cortex cérébral dans la maladie de Huntington, associée à des altérations de comportements cognitif et moteur, précise Sandrine Humbert. Contrecarrer ces déficits temporaires par traitement avec une ampakine au cours de la première semaine postnatale exerce des effets bénéfiques durables chez la souris, puisque les adultes ne développent pas la maladie », ajoute-t-elle.
Si ces résultats obtenus chez l’animal plaident en faveur d’un traitement précoce des personnes portant le gène de la maladie de Huntington pour modifier l’évolution de la maladie à l’âge adulte, ils invitent également à approfondir la compréhension du développement cérébral dans le contexte de cette pathologie. Ils appellent aussi à découvrir les liens entre les anomalies causées par la maladie et les mécanismes compensatoires mis en place par l’organisme avant l’apparition des symptômes.