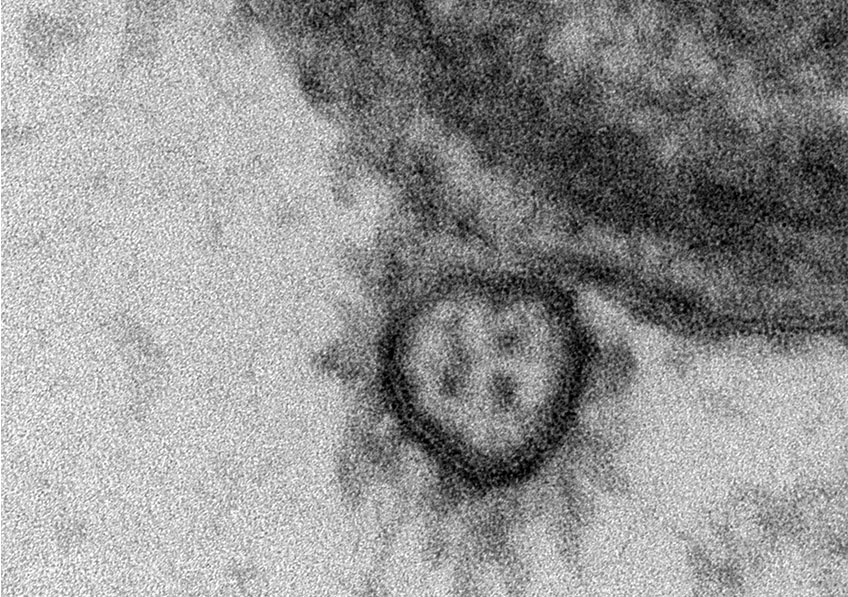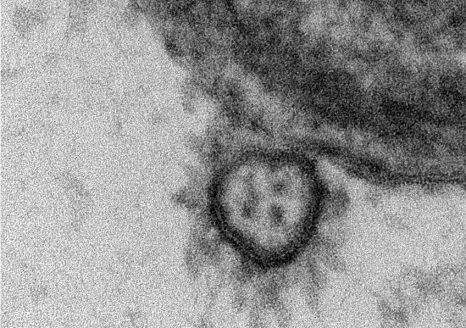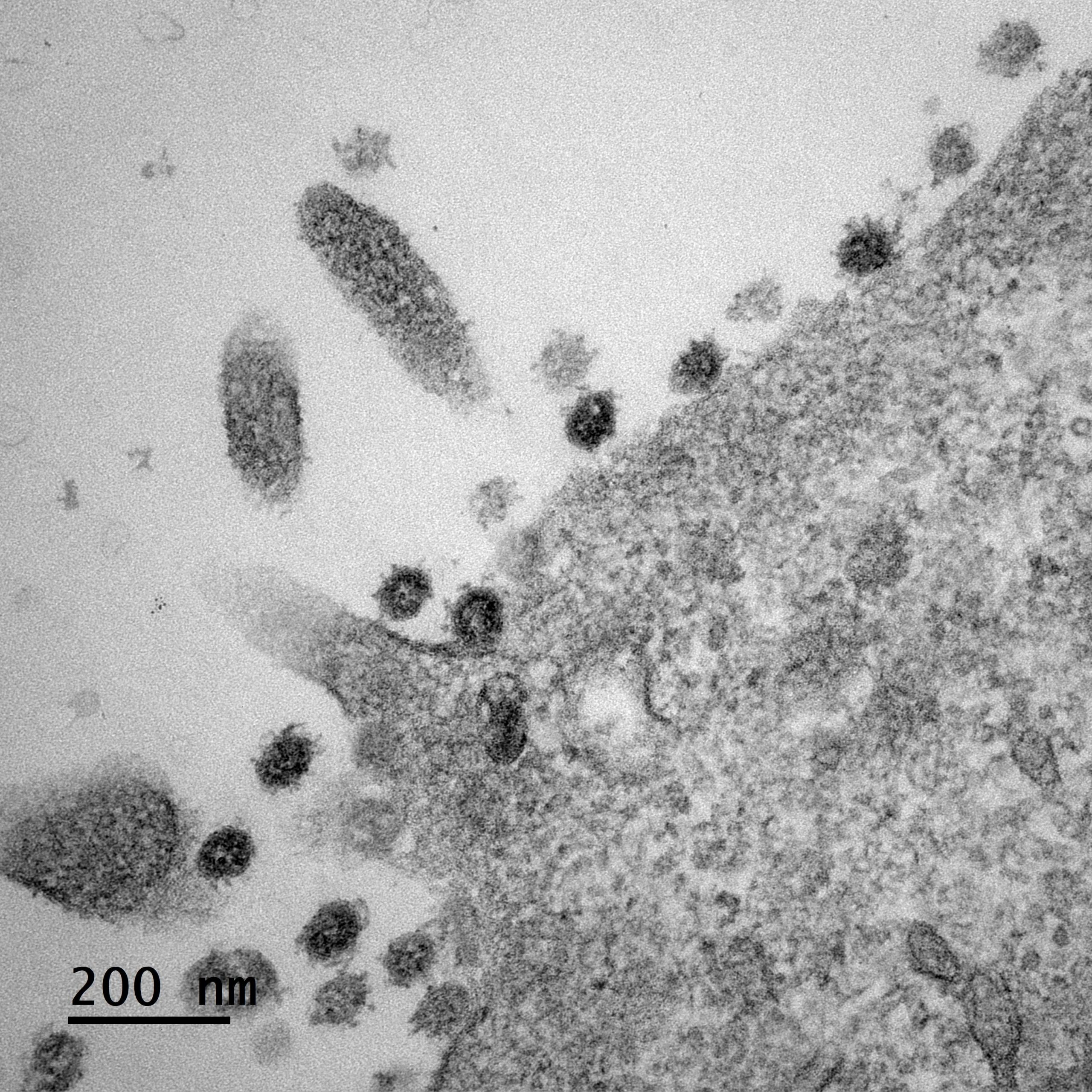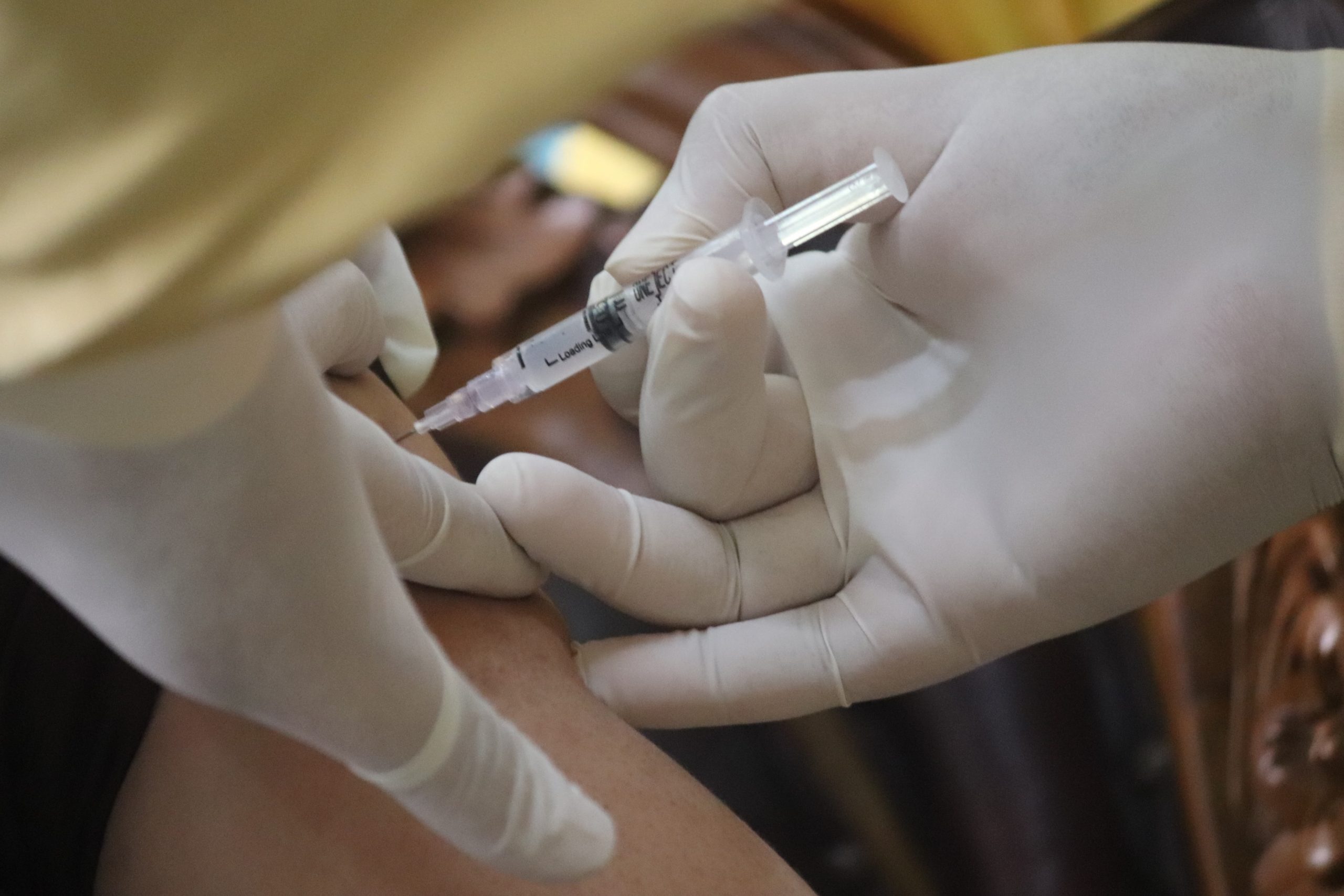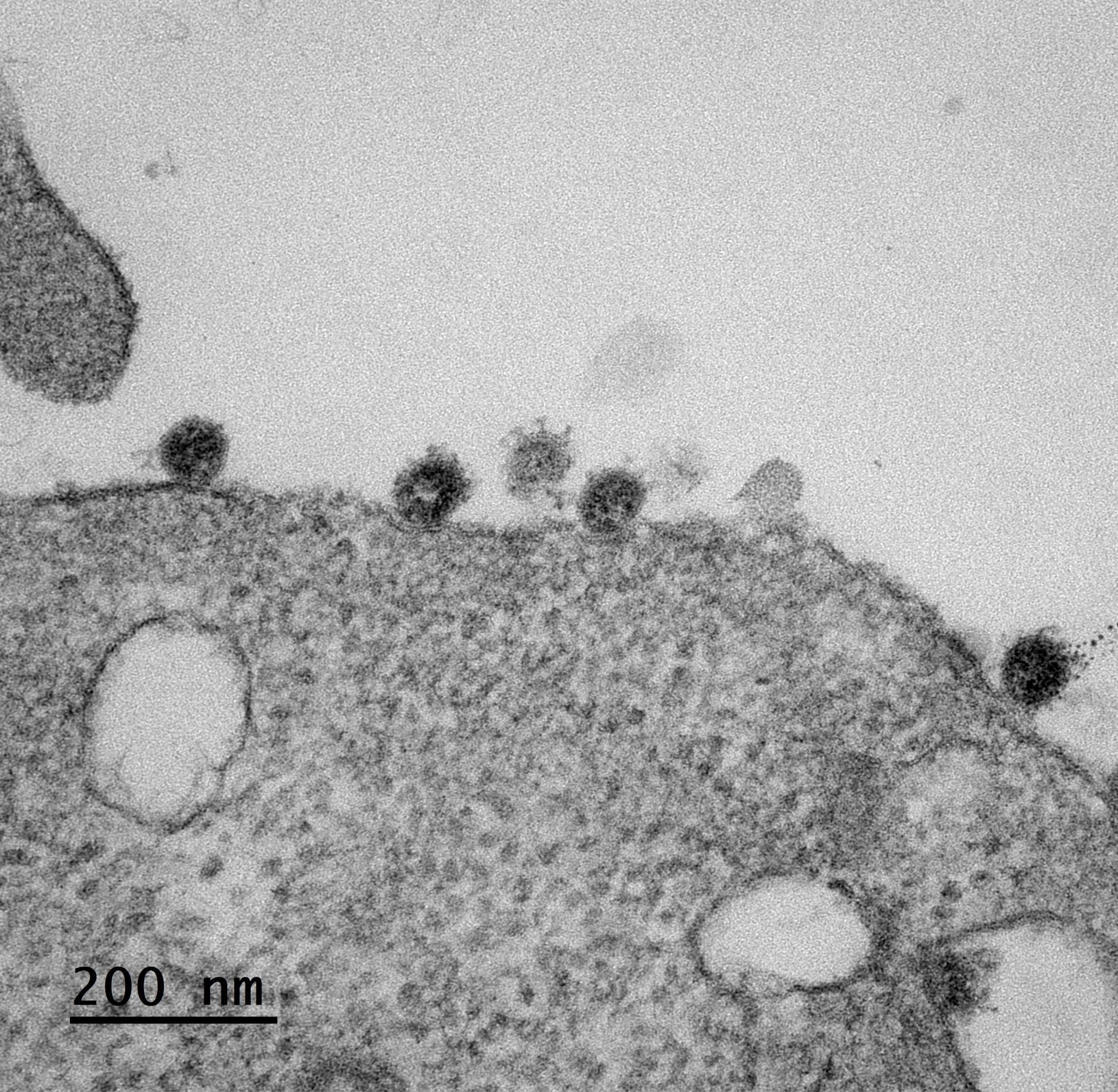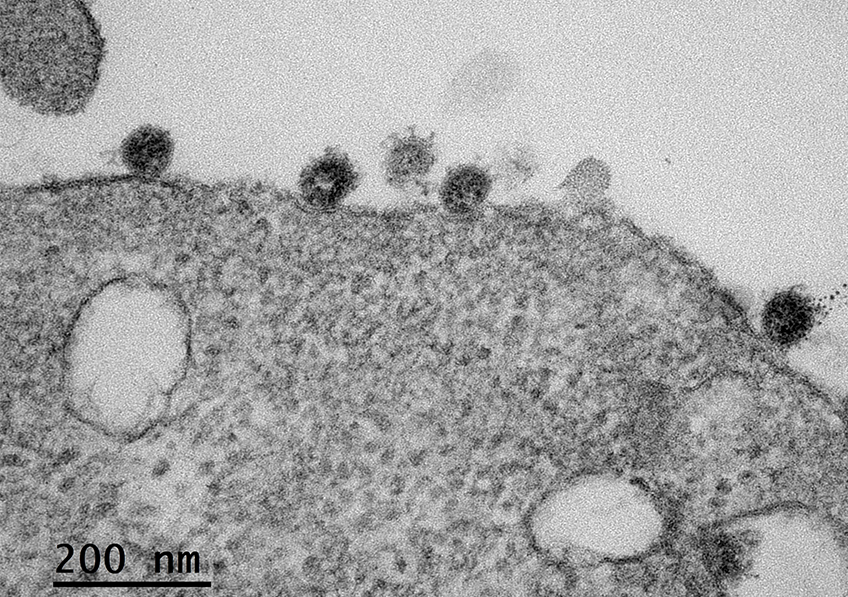
Modélisation 3D d’anticorps « attaquant » un virus. ©Adobe Stock
Le 11 octobre 2021, l’Organisation mondiale de la santé (OMS) a annoncé qu’elle recommandait une troisième dose de vaccin contre la Covid-19 pour les personnes immunodéprimées, tout en insistant sur le fait que cette décision ne concerne pas le reste de la population. Une annonce qui intervient alors que l’organisation s’opposait depuis plusieurs mois au principe d’une troisième dose, préférant plutôt insister sur l’importance de rendre la vaccination accessible à tous les pays.
En France, une troisième dose de rappel avait déjà proposée aux personnes les plus fragiles et à celles âgées de plus de 65 ans depuis septembre. La reprise épidémique a conduit les autorités à généraliser cette troisième dose à toute la population adulte.
En creux, la question qui se pose est celle de la durée de la réponse immunitaire suite à la vaccination. Est-on toujours protégé contre l’infection par le SARS-CoV-2, et surtout contre le risque de développer une forme grave de la maladie, plusieurs mois après avoir été vacciné ? Chez quelles personnes l’immunité est-elle particulièrement affaiblie ? Et pour qui une troisième dose s’avère-t-elle vraiment nécessaire ?
Depuis le début de la pandémie, de nombreuses équipes de recherche se sont penchées sur la réponse immunitaire induite par l’infection ou par la vaccination, ainsi que sur sa durée. Si des interrogations demeurent, des données solides ont déjà émergé, permettant d’y voir un peu plus clair. Canal Détox fait le point.
Texte mis à jour le 9 décembre 2021 pour refléter les données disponibles les plus récentes. Cet article reflète l’état des connaissances scientifiques en date de décembre 2021. Les connaissances scientifiques évoluant rapidement, il est possible que de nouvelles données viennent modifier une partie des conclusions mises en avant dans cet article.
La réponse immunitaire ne se résume pas aux anticorps
Avant toute chose, bien que les quantités d’anticorps dans le sang constituent un marqueur important de l’immunité, il est important de rappeler que la réponse immunitaire ne se résume pas seulement à cela.
Après avoir été infecté par un virus ou après vaccination, l’organisme garde en mémoire sa rencontre avec le pathogène. Le système immunitaire peut alors reconnaitre ce dernier et l’éliminer en cas d’une nouvelle exposition, protégeant la personne contre la maladie. Cette réponse immunitaire fait intervenir différents éléments, dont les anticorps neutralisants produits lors de la première exposition au pathogène qui subsistent encore dans l’organisme, mais aussi les lymphocytes T ou encore les lymphocytes B qui coordonnent la production de nouveaux anticorps (voir encadré).
Quelques rappels sur la réponse immunitaire
L’immunité innée est une réponse immédiate qui survient chez tout individu en l’absence d’immunisation préalable. Il s’agit de la première barrière de défense vis-à-vis des agents pathogènes. Elle fait principalement intervenir des anticorps préformés (naturels) et des lymphocytes qui ne présentent pas de récepteurs spécifiques à l’antigène.
L’immunité adaptative se met en place au bout de quelques jours après le contact avec l’agent pathogène et constitue la deuxième ligne de défense de l’organisme. Contrairement à l’immunité innée, l’immunité adaptative est spécifique d’un antigène donné.
On peut distinguer deux grandes catégories de réponse immunitaire adaptative. Les réponses dites humorales sont fondées sur la production d’anticorps par les lymphocytes B. Ces anticorps reconnaissent le pathogène et le neutralisent pour l’empêcher d’infecter les cellules cibles. Les réponses dites cellulaires sont fondées sur la reconnaissance et la destruction par les lymphocytes T des cellules infectées.
Les anticorps produits lors de l’infection ou de la vaccination diminuent au cours du temps, mais nous conservons des lymphocytes T et des lymphocyte B dits « mémoires », capables de générer de nouveaux anticorps en cas de nouveau contact avec le pathogène.
Il est cependant plus difficile d’étudier ces cellules mémoires et de s’assurer qu’elles sont bien présentes dans l’organisme. En effet, pour voir si un individu en dispose, il convient de réaliser une ponction au niveau des ganglions lymphatiques. Une procédure bien plus invasive que la prise de sang effectuée pour déterminer nos taux d’anticorps.
Une quantité réduite d’anticorps dans le sang, plusieurs mois après avoir été infecté ou vacciné, ne signifie donc pas que l’on n’est plus du tout protégé contre le virus. Les lymphocytes B et T qui restent en mémoire sont en mesure de prendre le relais.
Quelle immunité après l’infection ?
Plusieurs études soulignent que six à douze mois après l’infection, la plupart des anciens malades de la Covid-19 sont encore partiellement immunisés contre le virus.
Ainsi dans une étude publiée dans le journal Science, menée auprès de 200 patients convalescents, les scientifiques ont montré que 95 % d’entre eux présentaient encore une réponse immunitaire durable contre le virus dans les huit mois suivant l’infection. Les niveaux d’anticorps demeuraient stables, déclinant seulement légèrement six à huit mois après l’infection. La quantité de lymphocytes B spécifiques du virus augmentait quant à elle progressivement pour atteindre un pic six mois après infection, puis elle se stabilisait.
Enfin, les niveaux de lymphocytes T spécifiques du virus demeuraient aussi élevés. Six mois après l’infection, 92 % des individus présentaient des lymphocytes T CD4+ impliqués dans la coordination de la réponse immunitaire, tandis que la moitié d’entre eux présentaient des lymphocytes T CD8+, qui tuent les cellules infectées par le virus. La quantité de ces cellules variait beaucoup d’un individu à l’autre sans qu’aucun facteur explicatif (sexe ou âge des personnes par exemple) ne se détache particulièrement.
Ces données sont corroborées par des publications plus récentes dans le journal Nature, qui montrent que six à douze mois après infection, des patients convalescents présentent des niveaux d’anticorps stables mais également des lymphocytes B qui restent en mémoire au niveau de la moelle osseuse et peuvent réactiver la réponse immunitaire en cas de nouvelle infection.
Et après la vaccination ?
Les scientifiques ont aussi étudié la durée de l’immunité chez des milliers de patients vaccinés. Si nous avons un peu moins de recul sur ce sujet, les campagnes de vaccination ayant commencé il y a moins d’un an, on peut toutefois déjà souligner que les données disponibles suggèrent une efficacité toujours élevée des vaccins au cours du temps.
Une étude parue en septembre 2021 dans le New England Journal of Medicine rapporte le suivi d’environ 40 000 personnes vaccinées par le vaccin à ARN Pfizer (BNT162b2) aux États-Unis, en Amérique du Sud, en Afrique et en Europe, et montre que six mois après vaccination, une protection contre l’infection atteignant 91,3 %, est toujours constatée.
Plus récemment, deux études publiées dans la même revue sont venues compléter le tableau. La première, portant sur plus de 900 000 personnes vaccinées au Qatar, s’est intéressée à l’efficacité du même vaccin à ARN pour prévenir l’infection, mais également pour éviter les formes sévères de la maladie et les décès, dans un contexte où le variant delta était devenu dominant. Les données suggèrent là aussi un haut niveau de protection contre les formes graves de la maladie induites par le variant delta, atteignant 96 % d’efficacité deux mois après la seconde dose, et se maintenant à ce niveau jusqu’à six mois après. Toutefois, l’efficacité du vaccin pour prévenir l’infection et les formes asymptomatiques était plus faible, atteignant 77,5 % d’efficacité un mois après la première dose, mais déclinant après.
La seconde étude a été menée en Israël sur 4 868 soignants, testés mensuellement au moyen d’un test sérologique sur une durée de six mois, afin de déterminer leur taux d’anticorps neutralisants dans le sang. L’étude montre que ce taux diminue rapidement au bout de trois mois, mais qu’il reste ensuite relativement stable jusqu’au sixième mois. Des différences notables ont cependant été identifiées entre les individus. Ainsi, les personnes âgées avaient un taux d’anticorps plus faible que les plus jeunes, et les hommes un taux plus faible que les femmes. De manière générale, les personnes immunodéprimées étaient également plus susceptibles de présenter des taux réduits d’anticorps. À noter encore une fois que la diminution des anticorps dans le sang ne signifiait pas absence d’immunité. Les auteurs de cette publication n’ont pas étudié ici les autres paramètres de la réponse immunitaire, comme les lymphocytes.
Un risque d’émergence de nouveaux variants
À ce jour, les données disponibles concordent donc pour montrer que si la réponse immunitaire diminue au cours du temps, les individus continuent à être partiellement immunisés. D’autres cellules que les anticorps neutralisants peuvent prendre le relais en cas de nouvelle rencontre avec le virus. Par ailleurs, les vaccins continuent à être efficaces pour lutter contre les formes graves de Covid-19 et les décès, jusqu’à six mois après avoir reçu un schéma vaccinal complet. Le risque d’être infecté existe néanmoins, surtout suite à l’émergence de variants plus contagieux, comme le variant delta.
Par principe de précaution, notamment pour protéger les personnes ayant un système immunitaire plus fragile (en particulier les personnes âgées et immunodéprimées), qui ont potentiellement développé une réponse immunitaire moins forte suite aux premières doses de vaccins, certains pays ont donc introduit le principe d’une dose de rappel.
Avant de généraliser cette pratique, de nombreux scientifiques estiment cependant que la priorité reste de rendre la vaccination accessible à toutes les populations, dans tous les pays. Ne pas le faire implique de prendre le risque de laisser le virus circuler activement dans certaines régions du monde, ce qui pourrait aboutir à l’émergence de nouveaux variants potentiellement résistants aux vaccins.
Efficacité de la 3e dose, vaccination contre le variant omicron : les premières données disponibles
Une troisième dose de vaccin (dose de rappel ou ‘booster’) est privilégiée par les autorités sanitaires de nombreux pays pour compléter le schéma vaccinal des individus et lutter contre la reprise épidémique. Des données solides concernant l’efficacité de cette mesure sont désormais disponibles. Ainsi une large étude a été publiée le 8 décembre 2021 dans le New England Journal of Medicine portant sur plus de 850 000 personnes âgées de plus de 50 ans en Israël. La grande majorité (760 000 d’entre elles) avait reçu une troisième dose au moins cinq mois après leur deuxième dose. Les chercheurs se sont intéressés à l’efficacité de cette dose de rappel sur le risque de mortalité. Ils montrent que cette efficacité est de 90 % pour prévenir la mortalité liée au variant delta (65 décès dans le groupe ayant reçu la 3e dose vs 137 dans le groupe ne l’ayant pas reçu). Les facteurs de risque de mortalité étaient toujours l’âge ou le fait d’être atteint d’une pathologie affectant la réponse immunitaire. Ces données viennent confirmer que la dose booster renforce la qualité et l’intensité de la réponse immunitaire.
Face à l’émergence du variant omicron, la question de l’échappement immunitaire et de l’efficacité des vaccins disponibles s’est aussi très rapidement posée. Les premières données transmises par les laboratoires et issues de préprints, qui sont donc très préliminaires, suggèrent que les vaccins dont nous disposons seraient moins efficaces contre ce variant. Une perte du pouvoir neutralisant des anticorps induits par la vaccination est constatée face à omicron. Toutefois, la troisième dose de vaccin permettrait aux anticorps de regagner une capacité de neutralisation du virus plus importante. A long terme, adapter les vaccins au variant omicron est une stratégie envisagée.