Pierre Gressens est directeur de l’Unité mixte de recherche 676 Inserm-Université Paris Diderot, au sein du centre « neurosciences et neuropédiatrie » de l’Hôpital Robert- Debré (AP-HP). Il est également professeur de neurologie périnatale à l’hôpital Hammersmith, Imperial College, à Londres. Il est lauréat cette année du prix « ROGER DE SPOELBERCH », qui récompense un projet de recherche réalisé dans des hôpitaux universitaires européens par des chercheurs ayant contribué de manière significative à la recherche médicale et scientifique.
Pierre Gressens, directeur de l’unité de recherche U676. © Inserm, E. Begouen
Pierre Gressens a obtenu le diplôme de docteur en médecine à l’Université de Louvain en 1989. Jusqu’en 1991, il travaille dans le laboratoire de neurobiologie du développement dirigé par le Pr Philippe Evrard puis part aux Etats-Unis. Lorsque Philippe Evrard fut invité à créer et diriger à l’Hôpital Robert-Debré un service de neurologie pédiatrique et des maladies métaboliques, auquel il rattacha immédiatement une équipe de recherche Inserm en neurosciences translationnelles, Pierre Gressens le rejoint. Il dirige actuellement toujours cette unité mixte de recherche Inserm-Université Paris Diderot, étroitement liée au centre « neurosciences et neuropédiatrie », un programme très prioritaire de l’Hôpital Universitaire Robert-Debré (AP-HP). Il est également depuis 2009 professeur de neurologie périnatale à l’hôpital Hammersmith, Imperial College, à Londres.
Grâce au Prix Roger de Spoelberch, Pierre Gressens va bénéficier d’un soutien financier très substantiel pour poursuivre ses travaux particulièrement utiles dans la lutte contre les maladies neuro-dégénératives. Ses recherches visent à mieux comprendre les mécanismes et les conséquences fonctionnelles des atteintes cérébrales du nouveau-né pour développer des stratégies pour protéger le cerveau des tout-petits.
Des contributions scientifiques au service des tout-petits
Pierre Gressens a permis l’avancée des recherches sur le cerveau en développement. Il a notamment mis en évidence :
- le rôle neurotrophique du peptide vasoactif intestinal (VIP) qui est un facteur d’origine maternel clé pour le contrôle de la prolifération des cellules souches neurales. Ses travaux récents ont également montré que le VIP stimule la prolifération des cellules souches neurales en modulant les programmes génétiques contrôlant le cycle mitotique, établissant pour la première fois un lien entre un facteur environnemental d’origine maternelle et un processus génétique conservé tout au long de l’évolution.
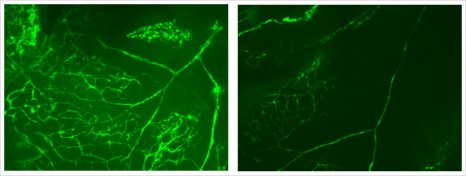
- le rôle sensibilisant des cytokines inflammatoires pour les lésions cérébrales périnatales et le rôle central de la microglie cérébrale dans la physiopathologie des lésions cérébrales du prématuré, ouvrant ainsi des perspectives originales de neuroprotection.
- l’effet protecteur de la mélatonine dans différents modèles animaux de lésions cérébrales mimant les lésions du prématuré humain. Ces travaux ont conduit à la mise sur pied d’un essai thérapeutique utilisant la mélatonine pour limiter les lésions cérébrales du prématuré.
Ses principaux projets de recherche ont aujourd’hui pour objectif de :
- réaliser l’essai thérapeutique “mélatonine” chez les enfants prématurés
- évaluer le potentiel neuroprotecteur des cellules souches dans les lésions cérébrales périnatales et leur capacité à limiter la neurodégénérescence au cours du développement
- comprendre les liens entre inflammation périnatale et neurodégénérescence à moyen et long terme.