Comment le souvenir traumatique des attentats du 13 novembre 2015 évolue-t-il dans les mémoires individuelles et la mémoire collective ? Comment ces mémoires individuelles se nourrissent-elles de la mémoire collective, et inversement ? Peut-on prédire, par l’étude des marqueurs cérébraux, quelles victimes développeront un état de stress post-traumatique, et lesquelles se remettront plus facilement ? Ce sont quelques-unes des questions auxquelles tentera de répondre l’ambitieux programme « 13-Novembre », porté par le CNRS, l’Inserm et héSam Université, avec la collaboration de nombreux partenaires. Codirigé par l’historien Denis Peschanski et le neuropsychologue Francis Eustache, ce programme de recherche transdisciplinaire est fondé sur le recueil et l’analyse de témoignages de 1000 personnes volontaires interrogées à quatre reprises en dix ans. Mobilisant plusieurs centaines de professionnels, ce programme est une première mondiale par son ampleur, le nombre de disciplines associées et le protocole établi. Des retombées sont attendues dans les domaines socio-historique et biomédical, mais aussi du droit et des politiques publiques ou de la santé publique.
Suite à l’appel lancé par Alain Fuchs, président du CNRS[1] en novembre dernier, la communauté des chercheurs se mobilise pour répondre aux questions posées à nos sociétés par les attentats et leurs conséquences. Elaboré dans la foulée de cet appel à projets, « 13-Novembre » est un programme transdisciplinaire qui se déroulera sur 12 ans. Porté par le CNRS et l’Inserm, en lien avec héSam Université, il a pour objectif d’étudier la construction et l’évolution de la mémoire après les attentats du 13 novembre 2015, mais aussi l’articulation entre mémoire individuelle et mémoire collective. « La vocation du CNRS s’exprime pleinement dans le projet 13 novembre : soutenir deux scientifiques qui vont eux-mêmes orchestrer des études mobilisant 150 chercheur-e-s issues de disciplines différentes dans un programme de long terme et d’une ambition inégalée », estime Alain Fuchs, président du CNRS. « L’Inserm s’est engagé dès le début pour faire aboutir le projet. Il associe les sciences humaines et sociales et les avancées les plus récentes des neurosciences. Il s’agit d’un projet interdisciplinaire, ambitieux qui répondra à des questions que nous nous posons tous. J’ai considéré que cela relevait des missions de deux organismes comme l’Inserm et le CNRS », indique Yves Lévy, PDG de l’Inserm.
1000 personnes suivies pendant dix ans
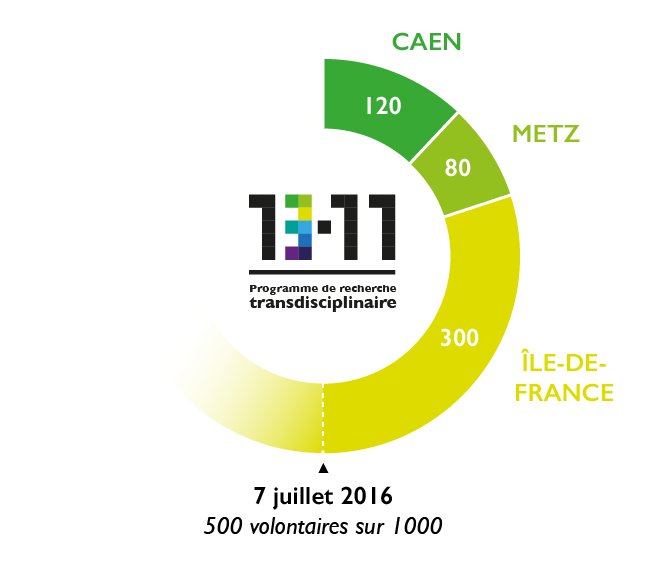
Les témoignages de 1000 personnes volontaires seront recueillis et analysés. Certaines ont vécu le drame au plus près – des survivants, leur entourage, des policiers, militaires, pompiers, médecins et aidants qui sont intervenus. D’autres ont été touchées indirectement : des habitants et usagers des quartiers touchés ; des personnes vivant aux abords de Paris ; et enfin, des habitants de plusieurs villes de France, dont Caen et Metz.
Cette étude est inédite par son ampleur : les 1000 participants seront suivis pendant 10 ans au cours de quatre campagnes d’entretiens filmés (en 2016, 2018, 2021 et 2026), grâce au concours de l’INA (chargé des captations parisiennes) et de l’ECPAD[2] (pour les entretiens en région). Sa conception est également sans précédent : les guides d’entretiens ont été construits en commun par des historiens, des sociologues, des psychologues, des psychopathologues et des neuroscientifiques, afin que le matériel recueilli soit utilisable par chacune de ces disciplines. À ce jour, il n’y a pas d’étude équivalente dans le monde.
Les témoignages individuels seront mis en perspective avec la mémoire collective telle qu’elle se construit au fil des années : les journaux télévisés et radiodiffusés, les articles de presse, les réactions sur les réseaux sociaux, les textes et les images des commémorations… autant de documents conservés par l’INA et analysés par ses équipes de recherches, en lien avec d’autres laboratoires. Un partenariat avec le Crédoc[3] permettra en outre de prendre le pouls de l’opinion aux dates des campagnes d’entretiens. Onze questions spécifiques sont ainsi incluses dans le traditionnel questionnaire semestriel du Crédoc en juin et juillet 2016.
Une étude biomédicale, intitulée « Remember », dont l’Inserm est promoteur, portera sur 180 des 1000 personnes : 120 personnes directement touchées par les attentats, souffrant ou non d’un état de stress post-traumatique, et 60 personnes habitant Caen. Grâce à des entretiens et à des IRM cérébrales, passés à la même fréquence que les entretiens filmés, il s’agira de mieux comprendre l’impact des chocs traumatiques sur la mémoire (notamment la résurgence incontrôlable de certaines images et pensées, caractéristique de l’état de stress post-traumatique), et d’identifier des marqueurs cérébraux associés à la résilience au traumatisme. Le tout, bien sûr, sans réexposer les personnes à des images et pensées traumatiques.
En parallèle, l’étude « ESPA » (étude de santé publique post-attentats) est lancée par Santé publique France[4] en collaboration avec le programme « 13-Novembre ». Celle-ci vise à analyser, par le biais d’un web questionnaire, l’impact psychotraumatique des attentats sur les personnes directement exposées, mais également la validité des circuits de soins.
Une étude transdisciplinaire et un engagement citoyen
L’intérêt de ce programme est majeur pour toutes les disciplines scientifiques qui y sont représentées. L’historien ou le sociologue essaieront de comprendre comment se co-construisent témoignage individuel et mémoire collective. Le linguiste mesurera l’évolution du vocabulaire et des constructions syntaxiques. Le neuropsychologue s’intéressera aux mécanismes de consolidation et reconsolidation de la mémoire et à son fonctionnement, différent selon que l’on a vécu l’événement lui-même ou que l’on se remémore les conditions dans lesquelles on a appris l’événement. Le neuroscientifique travaillera quant à lui sur les modifications des représentations mentales, l’état de stress post traumatique ou la possibilité d’évacuer le souvenir douloureux. Le psychopathologue s’attachera aux conséquences des attentats sur les représentations de soi, aux mécanismes de défense ou aux relations à la destructivité. En outre, le programme 13-Novembre aura des retombées dans le domaine des politiques pénales, des politiques de prise en charge des victimes, de gestion de crise et de pratiques mémorielles… Les entretiens filmés auront aussi une valeur patrimoniale : il s’agit également de conserver et de transmettre la mémoire des attentats du 13 novembre. C’est une forme d’engagement citoyen de la part de la communauté scientifique comme des professionnels de l’INA et de l’ECPAD en charge des captations des entretiens, de la description documentaire, de la mise à disposition des chercheurs et de l’archivage pérenne de cette mémoire.
Ce programme transpose au cas des attentats certains des concepts et des méthodologies transdisciplinaires développés par Denis Peschanski et Francis Eustache autour de la mémoire collective de la Seconde Guerre mondiale et du 11-Septembre dans le cadre de l’équipement d’excellence Matrice porté par héSam Université et dont l’INA est déjà partenaire. Pour les deux chercheurs, il est impossible de comprendre pleinement la mémoire collective sans prendre en compte les dynamiques cérébrales de la mémoire ; de même, on ne peut comprendre pleinement ces dynamiques cérébrales sans prendre en compte l’apport des déterminants sociaux. Les chercheurs s’inspirent aussi de l’étude par questionnaires papier menée par le psychologue américain William Hirst, une semaine, quelques mois et quelques années après les attentats du 11 septembre 2001. Il est d’ailleurs prévu une analyse comparée des résultats de ces deux études.
Appel à volontaires
Que vous ayez été témoin ou intervenant lors des attentats, que vous soyez résident ou usager des quartiers touchés, ou simplement habitant de Paris et sa banlieue, les chercheurs ont besoin de vous.
Si vous souhaitez participer et apporter votre témoignage dans le cadre du programme 13-Novembre, contactez l’équipe de médiateurs du programme :
– par téléphone : 06 60 98 53 82 / 06 61 19 10 32
– par email : rf.yromemecirtam@erbmevon31eriomem
Une permanence est déjà tenue dans les locaux de la mairie du 11e arrondissement de Paris (place Léon Blum, 75011 Paris). Horaires : le lundi et le vendredi de 8h30 à 17h (sauf le 3e vendredi du mois de 8h30 à 14h).
Des partenaires et soutiens multiples
L’étude « 13-Novembre » a démarré le 13 mai à Caen et le 2 juin à Bry-sur-Marne pour les entretiens filmés, et l’étude biomédicale Remember a débuté le 7 juin au sein de la plateforme d’imagerie biomédicale « Cyceron » à Caen, et en lien avec Normandie Université. L’appel à volontaires est en cours, relayé notamment par le quotidien Le Parisien-Aujourd’hui en France (via son journal et son site web). Les premiers résultats devraient être livrés à l’automne 2017. Les résultats finaux sont attendus pour 2028, deux ans après les derniers entretiens.
Porté par le CNRS et l’Inserm pour le volet scientifique, par héSam Université pour le volet administratif, le programme « 13-Novembre » est financé par l’Agence nationale de la recherche (ANR) dans le cadre du Programme Investissements d’Avenir (PIA).
Il mobilise plusieurs laboratoires de recherche :
- le Centre de recherche sur les liens sociaux, Cerlis (CNRS/Université Paris Descartes/Université Sorbonne Nouvelle – Paris 3),
- le laboratoire Neuropsychologie et imagerie de la mémoire humaine (Inserm/EPHE/Université de Caen Normandie),
- l’Institut des systèmes complexes – Paris-Île-de-France (CNRS),
- le laboratoire Neuropsychiatrie : recherche épidémiologique et clinique (Inserm/Université de Montpellier),
- le Centre de recherche sur les médiations (Université de Lorraine),
- le laboratoire Bases, corpus, langage (CNRS/Université Nice Sophia Antipolis).
Il associe de nombreux autres partenaires :
- l’INA,
- Santé publique France,
- l’ECPAD,
- l’EPHE,
- les Archives nationales,
- les Archives de France,
- l’Université Paris 1 – Panthéon Sorbonne,
- l’Université de Caen Normandie,
- la plateforme d’imagerie biomédicale Cyceron,
- le CHU de Caen,
- le quotidien Le Parisien- Aujourd’hui en France,
- Universcience,
- le Crédoc.
En outre, il bénéficie du soutien de plusieurs ministères, collectivités territoriales et associations :
- le ministère de l’Education nationale, de l’Enseignement supérieur et de la Recherche,
- le ministère de l’Intérieur,
- le ministère de la Culture et de la Communication,
- le secrétariat d’État à la Défense, chargé des Anciens combattants et de la Mémoire
- la mairie de Paris,
- la mairie du 10e arrondissement de la Ville de Paris,
- la mairie du 11e arrondissement de la Ville de Paris,
- la ville de Saint-Denis,
- la communauté d’agglomération Caen la mer,
- la région Normandie,
- Normandie Université
- l’Institut national d’aide aux victimes et de médiation (Inavem),
- l’association Life for Paris : 13 novembre 2015,
- l’association 13 novembre : Fraternité et Vérité,
- l’association Paris aide aux victimes,
- le groupe paritaire de protection sociale B2V,
- l’Institut mémoires de l’édition contemporaine (IMEC).
[1] Voir : https://intranet.cnrs.fr/intranet/actus/160225-attentats-recherche.html
[2] Établissement de communication et de production audiovisuelle de la Défense.
[3] Centre de recherche pour l’étude et l’observation des conditions de vie.
[4] Santé publique France est la nouvelle agence de santé publique issue de la fusion, le 1er mai 2016, de l’Institut national de prévention et d’éducation pour la santé (Inpes), de l’Institut de veille sanitaire (InVS) et de l’Etablissement de préparation et de réponse aux urgences sanitaires (Eprus).