Le Plan France Médecine Génomique 2025 a été remis au Premier ministre Manuel Valls par Yves Lévy, Président de l’Alliance nationale pour les sciences de la vie et de la santé – Aviesan et Pdg de l’Inserm, ce 22 juin 2016. Le Premier Ministre a adressé une lettre de mission en avril 2015 au Président d’Aviesan afin d’examiner les conditions nécessaires pour permettre l’utilisation du séquençage du génome entier dans la pratique clinique. Ce plan ambitieux, piloté et soutenu par l’Etat, vise à positionner, d’ici dix ans, la France dans le peloton de tête des grands pays engagés dans la médecine génomique. S’il répond à un enjeu de santé publique en termes diagnostiques, pronostiques et thérapeutiques, ce plan ambitionne également de faire émerger une filière médicale et industrielle nationale en médecine génomique et d’exporter ce savoir-faire.
Accéder au Plan
La médecine génomique est une réalité : elle transforme d’ores et déjà la manière dont on prévient, diagnostique, soigne et pronostique l’évolution d’une maladie. C’est un domaine à forte compétitivité internationale, chaque pays souhaitant aujourd’hui introduire la médecine génomique dans le parcours de soin, développer une filière industrielle et attirer les talents scientifiques pour consolider ses avantages. Pour élaborer ce Plan, l’Alliance Aviesan a réuni une année durant des représentants institutionnels et des compétences transversales des domaines de la recherche, de la santé, et de l’industrie, les agences de recherche et sanitaires, les administrations centrales des ministères, les industriels représentés par l’Ariis, la CNAM et l’HAS, le CGI, l’École d’économie de Toulouse.

Remise du Plan France Médecine génomique 2025 le 22 juin 2016 © Jean-Marie Heidinger / Inserm
Plus de 150 personnes se sont ainsi attachées à :
- Définir la place et l’importance du séquençage génomique dans la médecine actuelle et les développements futurs attendus dans 10 ans.
- Établir le positionnement de la France dans le domaine de la recherche sur la génomique, sa place dans les plans santé en cours ainsi que les priorités à mettre en œuvre en cohérence avec les stratégies nationales de santé et de recherche.
- Évaluer les enjeux associés en matière d’innovation, de valorisation et de développement économique, en prenant en compte les aspects technologiques, la gestion des grandes données et les implications éthiques.
Proposer un modèle médico-économique, sur le long terme, intégrant la prise en charge par l’Assurance maladie et le développement d’une filière industrielle pour soutenir une telle initiative.
« La médecine génomique est une révolution dans le domaine du soin et de la prévention, a affirmé Yves Lévy, Président d’Aviesan lors de la remise du Plan. Elle est au cœur de l’innovation en matière de diagnostic, de pronostic, de traitements et d’administration du médicament. La France doit se donner les moyens de réussir cette révolution, d’y prendre sa place, parmi les toutes premières. Nous disposons pour cela des formidables atouts de notre recherche fondamentale, clinique et translationnelle ».
Organisé autour de 14 mesures opérationnelles structurées en 3 grands objectifs, le plan France Médecine Génomique 2025 vise à :
- Déployer les instruments du parcours de soins génomique en
– se dotant des capacités de séquençage avec le déploiement d’un réseau de douze plateformes de séquençage couvrant l’ensemble du territoire,
– mettant en place les outils pour exploiter les volumes de données générées avec l’installation d’un Collecteur analyseur de données (CAD), capable de traiter et d’exploiter le volume considérable de données générées en les appariant avec les données médicales et d’offrir les premiers services dans le cadre du parcours de soin.
- Assurer le déploiement opérationnel et la montée en puissance du dispositif dans un cadre technique et éthique sécurisé afin de permettre un accès à la médecine génomique pour l’ensemble des personnes concernées (malades et leurs familles selon les indications) sur le territoire par :
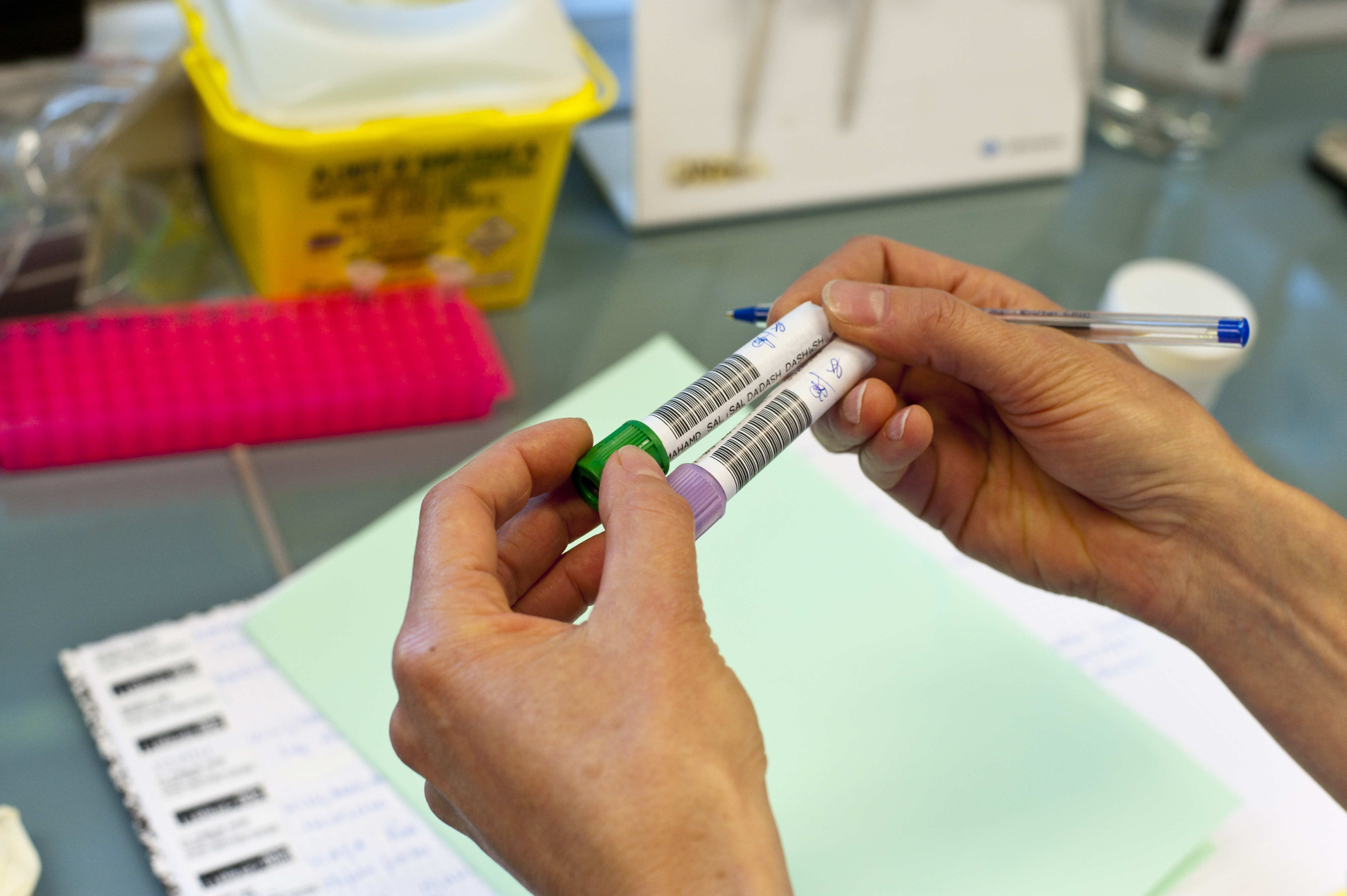
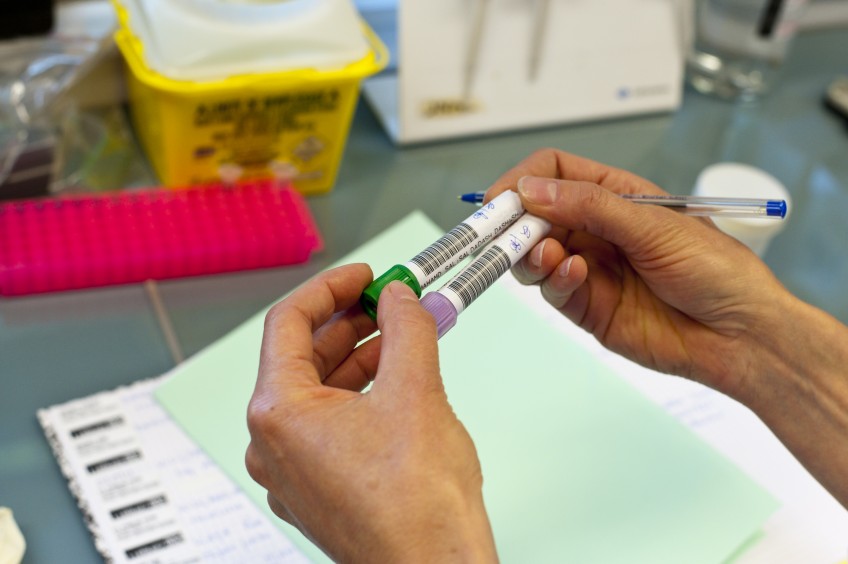
- La mise en œuvre effective du parcours de soin génomique dont les différents maillons seront testés et validés depuis le recueil des consentements, les modalités de prélèvements, de transport et de transfert des échantillons vers les centres de séquençage, jusqu’à la mise en place des personnels susceptibles d’en faire l’analyse et des contrôles qualité jusqu’à l’élaboration et la transmission des comptes rendus,
- La mise en place d’un dispositif d’évaluation et de validation des indications d’accès à la médecine génomique,
- La création d’un centre de référence, d’innovation, d’expertise et de transfert (CRefIX) capable, en partenariats avec les industriels, d’assurer les développements technologiques et informatiques indispensables,
- La mise en place des formations à la santé génomique et digitale au sein des universités et des écoles nécessaires pour relever le défi de l’exploitation et de l’interprétation des données,
- La garantie d’un parcours sécurisé et de qualité.
- Contribuer à l’émergence rapide d’une filière « médecine génomique »
La mise en place d’une filière nationale de médecine génomique, capable d’être un levier d’innovation scientifique et technologique, de valorisation industrielle et de croissance économique, nécessitera l’implication des industriels concernés aux côtés de la recherche académique et des acteurs publics du soin.
Pour accompagner l’émergence de cette filière, le plan prévoit par ailleurs un suivi des évolutions de la médecine génomique à l’échelle internationale ainsi que la mise en œuvre d’un programme de recherche dédié aux aspects médico-économiques.
La dimension éthique est au cœur de ce Plan de médecine génomique. L’accès et l’utilisation de données génomique représentant des populations entières soulèvent de nombreuses questions d’éthique tant au niveau individuel que sociétal. Aussi, le Plan prévoit notamment une saisine du Comité consultatif national d’éthique (CCNE), indispensable afin d’approfondir ces aspects au niveau national, mais également de se doter des moyens pour informer, consulter et impliquer les citoyens dans cette révolution.
Enfin, conscientes des enjeux que représente la médecine génomique, les associations de malades en lien avec l’Inserm se sont particulièrement impliquées, comme en témoigne leur contribution à l’élaboration de ce Plan.
La médecine génomique, une compétition internationale et des enjeux majeurs
Les États-Unis, le Royaume Uni et la Chine ont lancé des plans nationaux ambitieux au cours des deux dernières années, visant à la fois à développer une stratégie nationale et à soutenir leurs acteurs industriels. Avec eux, de nombreux acteurs industriels se mobilisent pour déployer des solutions technologiques dédiées à la médecine génomique et à la gestion des données numériques massives associées. De grandes entreprises internationales ont perçu le fort potentiel de développement de cette santé numérique et investissent ce secteur.
En Europe, plusieurs pays ont commencé à intégrer la médecine génomique dans leur système de santé : Estonie, Pays-Bas, Slovénie. Le risque de voir se développer un tourisme médical vers des pays du Continent offrant ce type de service existe avec lui celui d’une aggravation des inégalités de santé.
C’est dans ce contexte qu’a été élaboré le Plan « France Médecine Génomique 2025 » pour répondre aux différents enjeux que pose la médecine génomique :
Un enjeu de santé publique en permettant à un nombre substantiel de patients de bénéficier grâce séquençage de leur génome d’une prise en charge diagnostic, pronostic et thérapeutique personnalisée.
Un enjeu scientifique et clinique visant à renforcer la chaîne translationnelle allant de l’exploration moléculaire des pathologies jusqu’au bénéfice thérapeutique du patient en passant par la constitution et l’appariement de bases de données hétérogènes et multiples qu’il s‘agisse de données biologiques, cliniques voire environnementales.
Un enjeu technologique à travers la convergence indispensable entre les sciences numériques et les sciences de la vie et de la santé qu’exige cette approche. La capacité à acquérir, stocker, distribuer, interpréter et adresser ces données massives est au cœur de cette convergence qui verra émerger une filière en sciences du calcul et des données en biologie.
Un enjeu économique à la fois en termes d’efficience et de cout pour notre système de soin (diminution du nombre de bilans inadaptés, imprécis et onéreux, réduction des délais d’analyse, suppression ou limitation de médicaments inutiles, élimination de certains effets secondaires handicapants, gain d’années de vie) mais également d’opportunité de développer une nouvelle filière industrielle sources d’innovation en santé, de croissance et d’emplois.