© Inserm
© Inserm
L’Inserm vient de réaliser une expertise collective ciblée dressant un état des lieux actualisé et contextualisé des usages de cocaïne en France. Le rapport, commandé par la Mission interministérielle de lutte contre les drogues et les conduites addictives (Mildeca) et le ministère de la Santé se fonde sur l’analyse de la littérature scientifique internationale (plus de 2 600 références examinées) par un groupe pluridisciplinaire d’experts couvrant les domaines de l’épidémiologie, de la sociologie, de l’économie, de l’addictologie, de la prévention, de la réduction des risques et des dommages, et des trafics. L’expertise analyse les conséquences sanitaires et sociales actuelles de la consommation de cocaïne sous ses différentes formes en France. Elle identifie les stratégies et les actions les plus efficaces, ou les plus prometteuses en matière de prévention, de réduction des risques et des dommages, de prise en charge sanitaire et médico-sociale des personnes qui consomment et/ou souffrent de troubles de l’usage, ainsi que de politiques publiques de santé.
La cocaïne ou chlorhydrate de cocaïne, alcaloïde extrait de la feuille de coca, est un produit psychoactif de la classe des stimulants du système nerveux central, se présentant sous forme de poudre blanche, forme sous laquelle elle est principalement consommée par voie nasale (en « sniff »). L’ajout d’une base (ammoniac ou bicarbonate de soude) à sa forme poudre permet de la cristalliser sous forme de petits cailloux et de la rendre fumable avec une pipe : on parle alors de cocaïne basée, aussi appelée « crack » et/ou « free base »[1]. Elle se consomme également par injection dans une forme ou dans l’autre : selon les données 2022 du réseau français d’addictovigilance, la cocaïne est la première substance psychoactive injectée en France, principalement sous forme poudre.
Mode d’action et effets psychotropes de la cocaïne
La cocaïne agit sur le cerveau en bloquant la recapture de certains neurotransmetteurs, des molécules sécrétées par les neurones, qui permettent la transmission d’information vers les neurones adjacents. C’est-à-dire qu’elle empêche les neurones de recapturer eux-mêmes les neurotransmetteurs qu’ils ont libérés et qui finissent par s’accumuler. Or, dans le cas de la cocaïne, les neurotransmetteurs concernés sont la dopamine, la sérotonine et la noradrénaline, des neurotransmetteurs liés au bien-être, au plaisir et à la motivation. Par conséquent, la cocaïne provoque une désinhibition induisant des sensations de toute-puissance, une hypervigilance et une hyperactivité. Parmi les effets recherchés : une exacerbation des émotions, de l’excitation et un sentiment d’euphorie.
Les troubles de l’usage associés à la consommation de cocaïne incluent craving[2], développement d’une tolérance au produit, symptômes de sevrage, consommation incontrôlée en fréquence et/ou dosage, usages dans des situations physiquement dangereuses pour soi ou les autres… Ils sont majorés pour le crack en raison de sa rapidité d’action.
I. Un état des lieux de la consommation de la cocaïne en France : qui consomme et comment ?
Une consommation en hausse en France et dans le monde
Si le cannabis reste la substance la plus consommée dans le monde, la cocaïne effectue une percée avec une estimation à 22 millions de personnes qui consomment en 2021, ce qui s’explique notamment par la baisse des prix et l’augmentation de la pureté de la cocaïne. Cette augmentation est particulièrement notable en Europe, devenue un marché comparable au continent américain. La France occupe ainsi la sixième place en Europe avec l’Espagne en matière d’usage dans la population des 15-34 ans.
En France, la consommation de cocaïne a fortement augmenté en population générale, passant de 1,8 % en 2000 à 9,4 % en 2023 pour l’expérimentation au moins une fois au cours de la vie. Les 25-34 ans sont les plus touchés, avec 5,4 % d’usagers récents. La polyconsommation est fréquente, avec 61 % des usagers consommant également de l’alcool ou des opioïdes.
Les motivations de consommation sont multiples : recherche de performance, gestion du stress, ou usage récréatif, notamment en milieu festif où 42 % des festivaliers consomment de la cocaïne. L’expertise relève que les données concernant les usages en lien avec le milieu professionnel sont, à l’heure actuelle, trop lacunaires.
Chez les jeunes, l’expérimentation de la cocaïne a diminué ces dernières années, passant de 2,8 % en 2017 à 1,4 % en 2022 à 17 ans selon l’enquête nationale Escapad[3]. Cependant, cette consommation reste inégalement répartie selon le statut scolaire, avec 4,4 % des jeunes non scolarisés ayant déjà expérimenté la cocaïne, contre seulement 0,9 % en lycée général. Les garçons restent plus concernés que les filles, bien que l’écart se réduise. À l’échelle internationale, la France se situe au-dessus de la moyenne européenne, avec 2,7 % des 15-16 ans ayant déjà consommé de la cocaïne, contre 1,9 % en moyenne dans l’Union européenne.
Les demandes de prise en soins pour des problèmes liés à la cocaïne ont doublé entre 2015 et 2019 avec des délais d’attente de 3 à 6 mois. En 2021, 11 % des patients suivis dans les Centre de soins, d’accompagnement et de prévention en addictologie (CSAPA) consommaient de la cocaïne, souvent en polyconsommation. La durée moyenne entre la première consommation et la première consultation est actuellement de 13 ans pour les usagers présentant des troubles de l’usage.
La consommation de cocaïne basée se diffuse au-delà des populations en extrême précarité
Les scènes ouvertes de consommation (c’est-à-dire réalisée dans l’espace public), particulièrement visibles en Île-de-France révèlent des dynamiques communautaires complexes, où le soutien entre usagers coexiste avec la répression policière.
En parallèle, les données françaises sur les personnes accueillies en CSAPA montrent que l’usage de cocaïne basée (4,9 % des patients en 2021 contre 2,9 % en 2015, soit une augmentation de 70 % en 6 ans) se diffuse au-delà des milieux marginalisés. Initialement concentré dans des populations en grande précarité en raison de son faible coût, il touche désormais des publics insérés.
Facteurs de risques : peu de données sur l’hérédité, mais un effet avéré des troubles psychiatriques
S’agissant de la susceptibilité génétique d’un individu à développer des troubles de l’usage de la cocaïne, les données existantes sont peu robustes car concernent des échantillons trop faibles de personnes et des travaux de recherche fondamentale sur la transmission intergénérationnelle (épigénétique, hérédité et exposition prénatale) sont nécessaires.
La présence chez la personne consommatrice de troubles psychiatriques (stress post-traumatique, trouble de l’humeur, trouble déficitaire de l’attention avec ou sans hyperactivité/TDAH…) est quant à elle associée à l’augmentation du risque de troubles de l’usage.
Le constat de différences entre les femmes et les hommes vis-à-vis des troubles de l’usage a été associé à la fois à des causes physiologiques en lien avec le sexe biologique et à des déterminants sociaux liés au genre.
De manière générale, les experts précisent que l’usage de substances psychoactives et les troubles de l’usage de ces substances sont d’origine multifactorielle, avec un modèle communément admis d’une relation tripartite entre une substance, un individu et un environnement. La compréhension des facteurs de risque de la consommation de cocaïne est un préalable à l’efficacité des campagnes de prévention afin de cibler les publics concernés et de mieux appréhender les dynamiques qui conduisent à l’initiation, à l’installation ou à l’aggravation des consommations.
Approvisionnement et distribution de la cocaïne en France aujourd’hui
Le vecteur maritime étant le principal vecteur d’approvisionnement en cocaïne, la France avec sa façade océanique constitue une cible de choix pour l’approvisionnement portuaire. Le pays est également approvisionné par les pays limitrophes, ainsi que par une filière aérienne spécifique liée au territoire guyanais, zone de transit aujourd’hui responsable d’environ 20 % des entrées de cocaïne en France hexagonale.
Les usages actuels se caractérisent par une disponibilité accrue ainsi qu’une diversification des modes de consommation (64 % par sniff, 25 % par inhalation et 9 % par injection). Aux points de deal traditionnels s’ajoutent de nouvelles modalités de distribution : des doses de petites quantités à des prix très bas, des points de vente mobiles, des centrales d’appel, des ventes en ligne via des applications et messageries téléphoniques, des livraisons à domicile ou sur le lieu de travail. L’offre numérique favorise la diffusion de la consommation à de nouvelles catégories de personnes en matière de classes sociales et de localisation. Elle encourage le retour à l’usage grâce à des stratégies marketing visant à fidéliser les personnes qui consomment avec des offres promotionnelles et personnalisées. La livraison à domicile permet aussi d’irriguer l’ensemble du territoire et donc d’étendre la consommation de cocaïne aux petits centres urbains et à la ruralité, tout en banalisant l’acte d’achat pour la personne qui consomme.
II. Enjeux sanitaires : la santé de la personne qui consomme et au-delà
Une consommation associée à des risques sanitaires graves pour la personne consommatrice, son entourage et la population générale
La consommation de cocaïne peut avoir des conséquences graves, dont les risques augmentent avec le nombre et la régularité des prises : troubles cardiovasculaires, lésions ORL liées à la consommation en sniff, altérations des fonctions cognitives (troubles de l’attention, de la mémoire, de l’apprentissage et de la psychomotricité, impulsivité, dépendance…) voire développement ou aggravation de troubles psychiatriques, dommages rénaux…
La contamination par des maladies infectieuses (hépatite C, VIH, syphilis, papillomavirus…) est principalement liée à la consommation par injection, au partage et/ou à la réutilisation de matériel usagé (seringues, pipes à crack, pailles) ou à des pratiques à risque associées (pratiques sexuelles à risque). Les personnes consommatrices de cocaïne basée sont particulièrement vulnérables face à ce risque et également susceptibles de développer des lésions pulmonaires dues à la combustion des cristaux lors de l’inhalation.
Plus largement, certaines conséquences graves peuvent toucher à la fois la personne consommatrice et son entourage comme l’altération globale de la qualité de vie, les accidents et comportements à risque et/ou violents liés à la consommation, le risque accru de subir des violences sexuelles… Les enfants comptent ainsi parmi les victimes collatérales les plus vulnérables : que ce soit chez l’enfant à naître ou chez les enfants, adolescents, et adultes qu’ils deviendront, les conséquences potentielles sont nombreuses (violences intrafamiliales, troubles du développement…).
Les conséquences sociales sont également multiples, avec une stigmatisation des usagers qui a des conséquences négatives sur l’accès aux soins, le maintien dans le système de soins et la réinsertion socio-professionnelle. Enfin, les publics non-consommateurs sont eux aussi touchés par les tensions liées aux scènes de consommation ouvertes et par les violences collatérales (criminalité, voisinage de lieux de deal, règlements de comptes, corruption, violences sexuelles) et l’impact environnemental liés à la production et au trafic.
La diffusion et l’accroissement de la consommation de cocaïne engendrent une augmentation des dommages liés à son utilisation, avec un coût financier et sociétal direct et indirect. À titre d’exemple, 10 % du budget d’addictologie des hôpitaux marseillais sont consacrés à la cocaïne. S’il existe une littérature riche sur les dommages liés à la consommation de cocaïne, peu d’articles s’intéressent spécifiquement à la cocaïne basée.
Pas encore de traitement mais des pistes intéressantes
Aucun traitement pharmacologique dédié n’a encore obtenu d’autorisation de mise sur le marché (AMM) pour traiter la dépendance à la cocaïne. Cependant, des agents pharmacologiques ayant montré une efficacité dans les essais cliniques peuvent être envisagés. La NAC (N-acétyl-cystéine) a montré un potentiel intéressant pour réduire l’intensité du craving dans plusieurs essais cliniques mais nécessite des études complémentaires incluant de plus grands effectifs de patients et sur un temps plus long. Quant au topiramate, il a montré une efficacité sur le nombre maximal de jours sans consommation de cocaïne et sur la diminution de l’intensité du craving, mais présente une balance bénéfice-risque peu favorable.
Plusieurs pistes thérapeutiques sont en cours d’étude contre les troubles de l’usage et/ou pour réduire ou arrêter la consommation : la kétamine, le méthylphénidate (spécifiquement pour les personnes TDAH qui sont plus susceptibles de développer des troubles de l’usage), les psychédéliques (en particulier la psilocybine), ou le bupropion (un anti-dépresseur) font partie des pistes médicamenteuses explorées. D’autres approches sont également considérées comme la stimulation cérébrale ou le vaccin « anti-cocaïne », à l’étude depuis plus de 30 ans. En complément des traitements médicamenteux, les approches psychothérapeutiques, telles que les thérapies cognitivo-comportementales et les entretiens motivationnels, restent essentielles.
L’efficacité de l’incitation motivationnelle – qui vise à « récompenser » une modification de comportement pour la renforcer – a déjà été montrée dans des études au Brésil et aux États-Unis, avec un effet positif corrélé à la valeur de la « récompense » (ou « renforçateur »). En France, elle a été étudiée à travers l’expérience Tapaj (Travail alternatif payé à la journée)[4] qui a montré à la fois une efficacité significative dans l’amélioration de l’accès aux soins de personnes qui utilisent des drogues vivant en situation de précarité et une diminution de 30 % de la délinquance. De telles approches peuvent être couplées aux programmes de type « chez soi d’abord » (Housing First) qui, en proposant des hébergements adaptés aux personnes en situation de sans-abrisme et qui consomment de la cocaïne, permettraient de réduire les hospitalisations de moitié.
III. Prévenir et réduire les risques et les dommages : ce qui fonctionne, ce qui ne fonctionne pas
Des leviers concrets dont l’efficacité est montrée par les données disponibles
D’une façon générale, il ressort des études que les approches de santé publique sur les substances illicites, dont la cocaïne, comprennent la prévention et l’éducation du public cible, la réduction des risques et des dommages – RdRD (voir encadré), la prise en soins des troubles de l’usage et une dimension apparue plus récemment de mesure d’efficacité fondée sur les preuves.
Pour répondre de façon plus efficace et plus humaine à l’urgence sanitaire et sociale posée par la consommation de cocaïne, plusieurs pistes d’action sont identifiées par les experts : le renforcement des politiques de prévention et la RdRD constituent notamment une première ligne d’actions essentielles, visant à limiter l’initiation de la consommation et à freiner l’expansion des usages problématiques.
En savoir plus sur la Réduction des risques et des dommages (RdRD)
La RdRD est une approche qui a émergé pour répondre aux enjeux liés à la consommation de drogues, en particulier en matière de santé publique. De manière pragmatique, elle s’est focalisée sur la prévention des risques sanitaires, notamment lors de l’épidémie de VIH, avec la distribution de matériel stérile et l’accès aux traitements de substitution aux opiacés, mais elle s’intéresse également aux droits des personnes qui consomment et à la justice sociale.
Ce modèle repose sur un accompagnement adapté afin de permettre aux personnes de réduire les risques et les dommages auxquels elles sont confrontées, si on leur en offre les moyens et sans conditionner l’accompagnement à l’arrêt de la consommation. Il inclut des actions spécifiques telles que l’accueil inconditionnel, un travail de proximité sans jugement, la reconnaissance de l’expertise de la personne usagère de drogue, l’accompagnement vers l’emploi, le logement et la parentalité, ainsi que des interventions en milieu festif. Il permet de travailler avec la personne et de la soutenir où qu’elle soit et quels que soient ses perceptions, ses capacités et ses choix quant à une diminution, une modification, une régulation ou l’arrêt des consommations.
Sur l’aspect éducatif et préventif, les experts recommandent ainsi le développement de campagnes ciblées, de prévention par les pairs[5] (particulièrement efficaces auprès des jeunes personnes consommatrices) et les stratégies auto-préventives[6]. Ils pointent l’intérêt de l’usage de services numériques via Internet afin d’atteindre les populations plus insérées de façon large et à moindre coût et d’offrir un premier niveau d’aide, de psychoéducation et de soutien.
Autre levier majeur : le développement et le renforcement des dispositifs de réduction des risques, tels que les salles de consommation supervisées (« haltes soins addictions » – HSA en France, voir encadré) avec des systèmes de ventilation adaptés aux consommations par inhalation, le drug checking[7] et la distribution de matériel stérile (seringues pour l’injection et « pipes à crack » pour l’inhalation) qui ont montré leur efficacité, mais dont le déploiement reste limité.
« Haltes soins addictions » : un dispositif au cœur des politiques de prévention et de RdRD
Les salles de consommation supervisées (ou « à moindre risques ») – aujourd’hui dénommées « haltes soins addictions » (HSA) en France – permettent aux usagers de pouvoir consommer dans de bonnes conditions d’hygiène et de sécurité, avec un accès facilité à du matériel d’injection stérile à usage unique, sous la supervision d’un personnel formé. En plus d’offrir un lieu de consommation contrôlée, elles permettent d’accéder aux usagers et de les orienter vers les services sociaux et médicaux adaptés.
Ces stratégies de RdRD permettent d’attirer les personnes le plus marginalisées et améliorent leur accès aux soins primaires. De précédentes études ont montré dans plusieurs pays que ces salles se présentaient comme un moyen efficace de réduire les pratiques à risque des consommateurs de substances injectables, de diminuer les injections réalisées dans l’espace public (et par extension, les tensions et violences qui leurs sont associées) et le nombre de seringues retrouvées sur la voie publique, de casser les chaînes de transmissions infectieuses et de prévenir les overdoses.
Dans le cadre de la lutte contre l’épidémie d’hépatite C, le gouvernement a mis en place en 2016 pour une durée test de 6 ans, deux HSA ouvertes aux plus de 18 ans, à Paris et à Strasbourg. La Mildeca a confié à l’Inserm l’évaluation de leur efficacité en matière de santé et tranquillité publiques avec notamment des résultats positifs sur la diminution des risques infectieux[8]. La mise en place de la HSA à Strasbourg a également permis une diminution de 40 % des injections en public.
Cependant, le dialogue avec les riverains est compliqué, et les projets d’implantation de HSA ou d’ouverture d’espaces d’accueil pour les usagers sont mal acceptés, notamment dans des quartiers situés hors des scènes de consommation.
À la suite des différentes évaluations positives émises par l’Inserm, l’Inspection générale des affaires sociales (IGAS), l’Inspection générale de l’administration (IGA) et la Mildeca, confirmant leur efficacité et leur utilité comme « maillons essentiels » pour la santé publique et la réduction des nuisances dans l’espace public, la fin de l’expérimentation des HSA en France – initialement programmée pour le 31 décembre 2025 –, est repoussée au 31 décembre 2027.
Concernant la prise en soins, l’expertise insiste sur l’importance de l’investissement dans la recherche sur les traitements innovants et la formation des professionnels afin d’améliorer l’accompagnement sanitaire et social des personnes consommatrices.
La stigmatisation plurielle des personnes qui consomment limite la recherche de soins par les usagers et leur efficacité
La stigmatisation des personnes consommatrices de drogues se manifeste sous différentes formes : la stigmatisation sociale (discrimination par l’entourage et la société), la stigmatisation structurelle (discrimination par l’organisation des soins, pratiques discriminatoires au sein des services de santé) et l’auto-stigmatisation (baisse de l’estime de soi, intériorisation et anticipation de la stigmatisation sociale réduisant la capacité à demander de l’aide ou à répondre à ses propres besoins sociaux).
La stigmatisation structurelle a un impact profond sur l’accès aux soins des personnes concernées et certains travaux la considèrent comme un déterminant social de santé majeur. Elle est perpétuée par les conditions de prise en soins : contraintes de temps, manque de ressources, représentations négatives des personnels de santé…
En outre, les stigmatisations sociales et structurelles s’entrelacent souvent avec d’autres formes de discrimination, notamment liées à la classe sociale, au genre et à la couleur de peau. Ainsi, l’accès aux dispositifs de RdRD reste très inégal avec des sous-groupes identifiés comme particulièrement vulnérables à la consommation de substances et aux troubles liés à la consommation et présentant des besoins spécifiques : les personnes sans-abri, travailleuses du sexe, qui présentent des comorbidités psychiques, qui sont incarcérées ou qui l’ont été, les populations minorisées (femmes, personnes racisées, minorités sexuelles et de genre) et populations déplacées forcées (réfugiés, demandeurs d’asile…) n’ont que très peu accès aux services socio-sanitaires pour des raisons multiples, d’ordre structurel, social et individuel.
L’expertise pointe que des efforts supplémentaires sont nécessaires pour concevoir et mettre en œuvre des politiques et des programmes répondant aux besoins particuliers de ces groupes, avec une attention portée sur l’intersectionnalité[9] et la prise en compte des discriminations multiples. Elle insiste sur l’importance d’aller à la rencontre de ces personnes et de communiquer avec elles, mais aussi de mettre en place de nouveaux lieux d’accueil et de consommation dédiés – par exemple en non-mixité (en particulier pour les mineurs, les femmes et les minorités de genre) – pour réduire la stigmatisation, offrir un accueil plus approprié et renforcer l’accès aux soins.
Le langage utilisé pour désigner les personnes qui consomment des drogues est également crucial : des termes péjoratifs et connotés (toxicomanes, drogués…) renforcent les stéréotypes. Selon les experts, l’utilisation de mots neutres et appropriés pourrait ainsi contribuer à lutter contre cette stigmatisation. Ils recommandent dans le débat public par exemple, de parler de la cocaïne avec rigueur en se fondant sur la science, dans toutes ses dimensions (notamment, d’intégrer systématiquement les dimensions sanitaire et sociale) et sans sensationnalisme.
IV. Politique pénale : penser la régulation autrement pour une meilleure efficacité
Une répression qui renforce les effets de la stigmatisation et de la précarité des personnes consommatrices ayant des troubles de l’usage
Sur le plan législatif, la décriminalisation de l’usage de drogues est au cœur des débats européens. La législation française en matière d’infractions à la loi sur les stupéfiants est considérée comme l’une des plus répressives en Europe. N’établissant aucune distinction entre les drogues, la répression actuelle se concentre principalement sur les usagers qui représentent 90 % des interpellations, avec des amendes forfaitaires dont le montant vient d’augmenter.
Pourtant, cette approche semble peu efficace : malgré les saisies record et les coûts importants de police et de justice engagés, l’offre et la demande de cocaïne continuent d’augmenter. Certaines données suggèrent même que la répression policière aggraverait les problèmes sociaux, sanitaires et judiciaires des personnes présentant des troubles de l’usage. La criminalisation engendrerait aussi une incertitude concernant la composition des produits, exposant davantage les personnes qui consomment à des risques. Selon l’analyse de la littérature, la décriminalisation de l’usage, comme au Canada, pourrait améliorer l’accès aux soins en réduisant la stigmatisation, mais à condition qu’elle s’accompagne de mesures sociales de substitution aux condamnations/peines d’incarcération (par exemple, remplacer les amendes par des orientations vers une consultation en CSAPA) et de mesures sanitaires (capacités suffisantes d’accueil et de traitement des personnes qui consomment) pour être efficace.
L’expertise invite donc à repenser la politique pénale en recentrant la répression sur les trafiquants de haut niveau, comme les importateurs (par exemple, avec la confiscation des patrimoines criminels pouvant servir à financer des campagnes de prévention ainsi que des structures d’accueil et de soin), avec une lutte contre l’offre tenant compte des nouvelles modalités d’approvisionnement – notamment en ligne –, et en choisissant une approche qui ne criminaliserait pas les personnes ayant des troubles de la consommation.
En conclusion, face au défi majeur de santé publique que représentent les conséquences de la consommation de cocaïne et ses nouveaux usages, l’analyse des données disponibles permet à l’expertise de recommander une approche globale et coordonnée, combinant prévention, réduction des risques, soins innovants et politique d’investigation pénale et financière. Elle identifie quatre grands leviers d’action prioritaires en France qui apparaissent comme indispensable pour réduire les dommages causés par la cocaïne à ses consommateurs et à l’ensemble de la société :
- une réduction des risques ciblée via les « haltes soins addictions » ;
- une répression ciblée sur les trafics et le haut du spectre des acteurs des réseaux criminels ;
- des campagnes de prévention ciblées ;
- la mise en place de programmes de logement et d’insertion.
Les expertes et experts qui ont travaillé sur l’expertise collective Cocaïne :
- Perrine Roux : directrice de recherche Inserm en santé publique au sein de l’unité Sciences économiques et sociales de la santé et traitement de l’information médicale (Sesstim, Inserm/IRD/Aix-Marseille Université)
- Clotilde Champeyrache : économiste, maîtresse de conférences et directrice de recherche au Conservatoire national des arts et métiers, directrice du PSDR3C (Pôle sécurité défense renseignement criminologie crises cybermenaces)
- Hélène Donnadieu : médecin hépatologue et addictologue, professeure d’addictologie à l’université de Montpellier et cheffe de service d’addictologie au CHU de Montpellier, unité Inserm Pathogenèse et contrôle des infections chroniques et émergentes (PCCEI, Inserm/Université de Montpellier/Université des Antilles/EFS)
- Émilie Jouanjus : pharmacologue et pharmacoépidémiologiste, maîtresse de conférences et praticienne hospitalière de pharmacologie à l’université de Toulouse et au CHU de Toulouse, Centre d’épidémiologie et de recherche en santé des populations de Toulouse (Inserm/Université de Toulouse), membre du Réseau français d’addictovigilance
- Yasser Khazaal : psychiatre et professeur de psychiatrie des addictions à l’université de Lausanne, médecin chef au service de psychiatrie du CHU de Lausanne
- Laurent Fleury : responsable du pôle Expertises collectives de l’Inserm
Les expertises collectives à l’Inserm
Développées par l’Inserm depuis 1993, les expertises collectives constituent une démarche d’évaluation et de synthèse des connaissances scientifiques existantes sur des thèmes de santé publique.
Ces expertises répondent aux demandes d’institutions souhaitant disposer des données récentes issues de la recherche. L’objectif est le partage de connaissances et l’apport d’un éclairage scientifique indépendant sur des questions précises de santé, dans une perspective d’aide à la décision publique dans le champ de la santé des populations.
Le cadrage scientifique, le support bibliographique, la coordination et la valorisation des expertises collectives sont assurés par le pôle Expertises collectives de l’Inserm, rattaché à l’institut thématique Santé publique. Pour en savoir plus : inserm.fr/expertise-collective
Les expertises collectives ciblées : un nouveau format
Il s’agit d’un nouveau format, plus agile, des expertises collectives de l’Inserm, qui s’inscrit dans un contexte d’urgence : elles permettent la remise des résultats d’expertise dans un délai plus restreint que les expertises collectives « classiques ». La méthodologie habituelle de l’expertise collective Inserm a ainsi été adaptée à un délai raccourci avec la constitution d’un groupe pluridisciplinaire plus restreint d’experts, et, selon la thématique abordée, une recherche bibliographique qui peut être soit approfondie (collecte des publications scientifiques), soit plus ciblée (sélection limitée aux revues et méta-analyses très récentes).
[1]Dans ce dossier de presse, l’utilisation du terme « cocaïne » seul désigne la substance dans sa globalité. Les adjectifs « poudre » ou « basée » seront utilisés pour désigner spécifiquement l’une ou l’autre des deux formes.
[2] Craving : impulsion véhiculant un besoin irrépressible de consommation d’un produit psychoactif.
[3]Escapad : enquête sur la santé et les consommations lors de la journée Défense et citoyenneté (JDC). Cette enquête est représentative des jeunes Français âgés de 17 ans.
[4]Le programme Tapaj offre un accompagnement médico-social aux jeunes de 16 à 25 ans en situation de précarité, facilitant leur réinsertion professionnelle.
[5]La prévention par les pairs dérive de l’éducation par les pairs, un principe qui repose sur un modèle de transmission horizontale d’informations et dans une logique de création de lien par des personnes de même âge, contexte social, fonction, éducation ou expérience.
[6]Stratégies auto-préventives : les personnes qui consomment développent elles-mêmes des stratégies auto-préventives à l’égard de leurs conduites addictives et des conséquences associées.
[7]Un drug checking ou services d’analyse de drogues comprend une analyse chimique de la substance à consommer et une consultation individuelle. Il a aussi pour objectif de permettre à la personne consommatrice de substances d’accéder aux offres de prévention et de réduction des risques et permet de mieux comprendre les tendances et les dynamiques du marché illégal de la drogue et de la consommation de substances illégales.
[8]https://presse.inserm.fr/vih-et-hepatite-c-chez-les-personnes-qui-consomment-des-substances-par-injection-les-salles-de-consommation-limitent-les-pratiques-a-risques/67517/#_ftn1
[9]L’intersectionnalité consiste à prendre en compte l’interdépendance et l’interconnexion d’identités sociales multiples (genre, origine ethnique, classe sociale, orientation sexuelle, usage de drogues…), à l’origine de rapports de pouvoir et d’inégalités structurelles et pouvant générer discrimination et marginalisation de groupes de personnes.
 © Unsplash
© Unsplash





 Activation d’une cellule dendritique après la capture d’exosomes tumoraux reprogrammés par la dendrogénine A. © Sandrine Silvente-Poirot.
Activation d’une cellule dendritique après la capture d’exosomes tumoraux reprogrammés par la dendrogénine A. © Sandrine Silvente-Poirot.
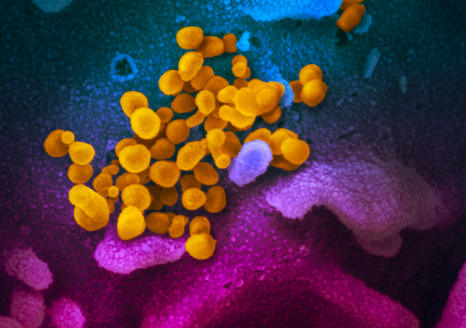 Cette image montre le virus du SARS-CoV-2 (en jaune). © National Institute of Allergy and Infectious Diseases – Rocky Mountain Laboratories, NIH
Cette image montre le virus du SARS-CoV-2 (en jaune). © National Institute of Allergy and Infectious Diseases – Rocky Mountain Laboratories, NIH