Illustration 3D du pancréas © Fotalia
Décrypter les relations entre les cellules cancéreuses et l’écosystème tumoral est un défi majeur pour comprendre le développement de la maladie et identifier des pistes thérapeutiques dans l’adénocarcinome pancréatiques (AdKP), l’un des cancers solides les plus agressifs, avec un taux de survie à 5 ans inférieur à 10%.
Dans cette étude, les équipes d’Olivier Soriani Professeur à Université Côte d’Azur (Nice, iBV, Institut de Biologie Valrose) et Richard Tomasini, Directeur de recherche Inserm (Marseille, CRCM, Centre de Recherches sur le Cancer) dévoilent comment un canal potassique (SK2) stimule la formation des métastases en sensibilisant les cellules cancéreuses aux signaux du microenvironnement tumoral. Ces travaux sont prochainement publiés dans la revue GUT.
Le cancer du pancréas ou adénocarcinome pancréatique (AdKP) est un cancer dont le pronostic demeure grave avec un taux de survie à 5 ans inférieur à 10%. C’est une tumeur solide dont la structure particulière est en partie responsable de la résistance aux traitements. Elle est en effet constituée de cellules cancéreuses peu nombreuses (<20% des cellules) dispersées au sein d’un compartiment très dense, peu vascularisé, le stroma, majoritairement constitué de cellules fibroblastiques associées au cancer (CAF).
Éléments clefs du stroma, les CAF sont issus de fibroblastes normaux, cellules de soutien naturellement présentes dans le pancréas. Sous l’influence des cellules tumorales, ces fibroblastes prolifèrent, sécrètent des signaux chimiques et des protéines qui forment un réseau, la matrice extracellulaire. Cet environnement très particulier contrôle en retour les cellules tumorales en stimulant leur fonctions pro-invasives. Plus agressives, les cellules cancéreuses forment des métastases qui vont coloniser des organes distants, et en particulier le foie.
La compréhension des voies de communication entre les cellules tumorales et les CAF représente un défi majeur pour permettre le développement de nouveaux traitements.
Quels sont donc les acteurs du dialogue entre les CAF et les cellules tumorales ?
L’équipe d’Olivier Soriani a focalisé ses recherches sur une famille de protéines encore peu étudiée dans le cadre de la recherche sur le cancer, celle des canaux ioniques, qui regroupe plus de 300 membres.
Un canal ionique est une protéine intégrée dans la membrane des cellules, autorisant le passage de petites molécules chargées électriquement, les ions. Le passage des ions à travers les canaux ioniques induit de petits courants qui déterminent un champ électrique à travers la membrane des cellules vivantes. Ce phénomène de « bioélectricité » est à la base de la transmission de l’information dans de nombreux organes tels que le système nerveux, le cœur, les muscles, ou encore le système endocrinien.
Trois questions sont au départ de cette étude : Les canaux ioniques sont-ils impliqués dans le dialogue entre les CAF et les cellules cancéreuses ? Si oui, sont-ils capables de contrôler le comportement des cellules cancéreuses ? Enfin, peut-on cibler ces canaux spécifiquement dans la tumeur à des fins thérapeutiques, sans altérer le fonctionnement normal des autres organes ?
Pour répondre à ces interrogations, les chercheurs de Nice de l’équipe d’Olivier Soriani, spécialistes des canaux ioniques, se sont associés à l’équipe marseillaise de Richard Tomasini, reconnue pour ses travaux sur le rôle des CAF dans le cancer du pancréas.
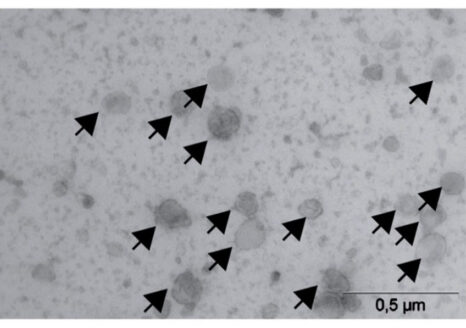
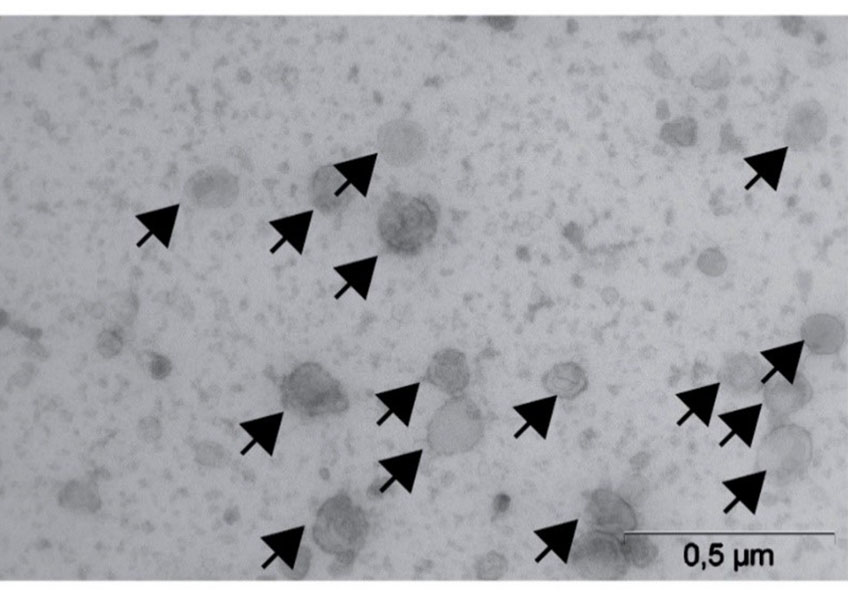
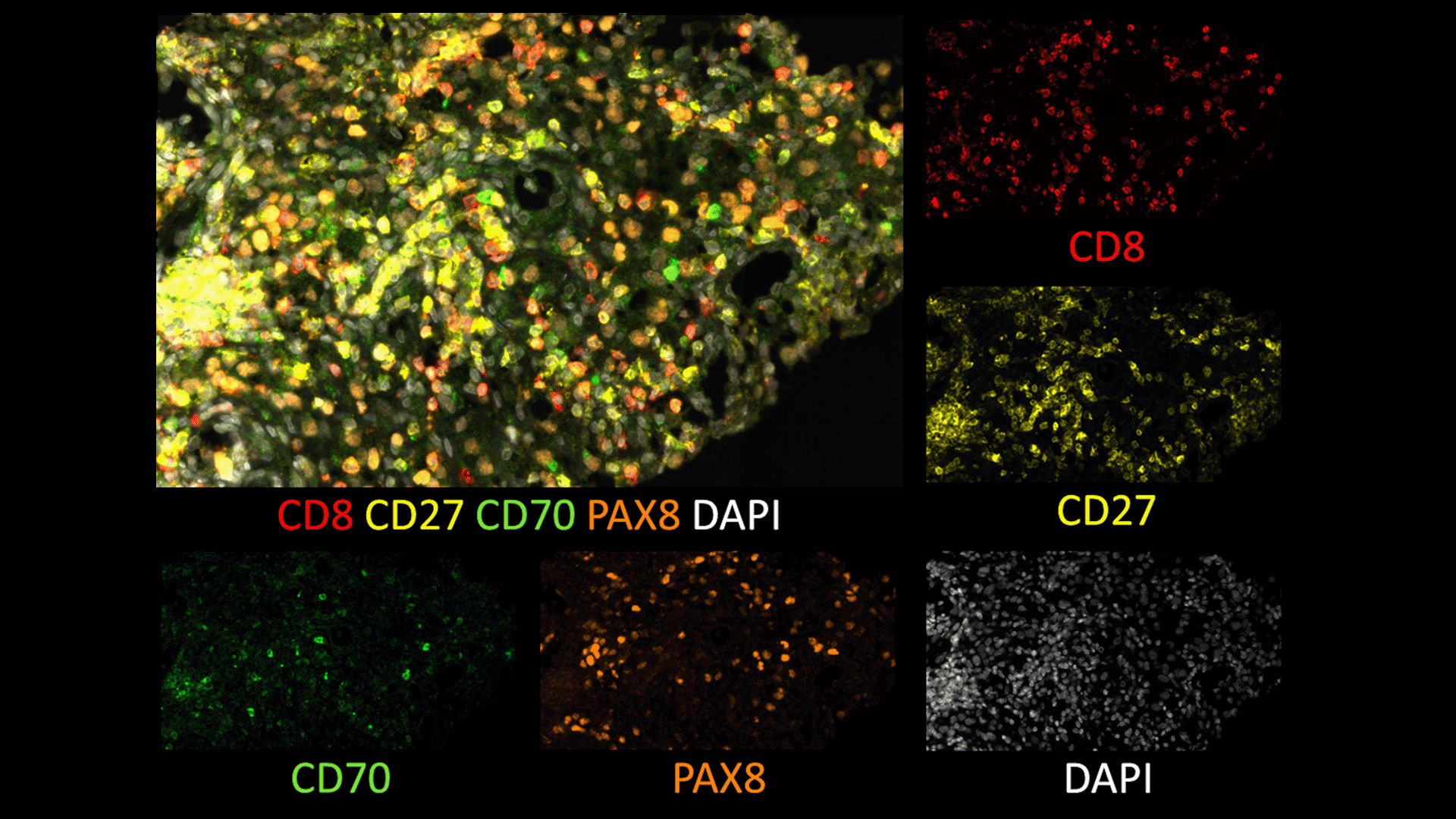
Dans un premier temps, ils ont montré que la stimulation des cellules cancéreuses par des CAF prélevés chez des patients, induit dans les cellules tumorales, un courant électrique généré par l’ouverture d’un canal ionique particulier, le canal potassique SK2. De plus, des expériences sur des cellules tumorales en culture indiquent que l’inhibition de l’activité du canal SK2 protège ces dernières de l’influence pro-invasive des CAF. Ces résultats sont confirmés in vivo, puisque les CAF ne sont plus capables d’induire la formation de métastases dans le foie de souris-modèles déficientes pour le canal SK2.
Enfin, l’analyse de banques de tumeurs du pancréas humaines montre que l’expression du canal SK2 est associée aux métastases hépatiques.
Par quel mécanisme le canal SK2 est-il capable d’augmenter la réponse des cellules tumorales à l’influence des CAF ?
Les chercheurs ont observé que les CAF, en sécrétant certaines protéines nécessaires à la formation de la matrice extracellulaire (collagène et fibronectine), stimulaient dans les cellules cancéreuses une voie de signalisation primordiale dans l’agressivité tumorale : la voie dépendante de l’AKT, une enzyme qui régule l’activité de nombreuses protéines cellulaires. L’exploration fine de cette voie par les chercheurs niçois a révélé deux faits majeurs : tout d’abord, le canal SK2 est une cible directe de l’AKT : c’est par cette voie que le canal est activé en présence des CAF. Ensuite, le canal se comporte comme un amplificateur de signal dont l’activité augmente considérablement l’efficacité de la voie AKT, et donc la sensibilité des cellules aux signaux pro-métastatiques émis par les CAF. L’utilisation de techniques de microscopie quantitative a d’ailleurs permis de montrer que la stimulation des cellules tumorales par les CAF provoquait le couplage physique entre SK2 et AKT.
Comment agir sur SK2 sans altérer la fonction du canal dans les tissus sains (cerveau, vaisseaux sanguins, cœur) ?
L’équipe d’Olivier Soriani s’intéresse depuis plusieurs années à une protéine auxiliaire de nombreux canaux ioniques : SigmaR1. SigmaR1 est une protéine intracellulaire exprimée dans tous les tissus. Silencieuse dans des conditions normales, elle s’active dans les tissus lésés pour accompagner des protéines –partenaires, contribuant ainsi à la survie des cellules en état de stress. De cette manière, SigmaR1 contribue à ralentir la progression ou à limiter la mort cellulaire dans des pathologies telles que les maladies neurodégénératives, les accidents vasculaires cérébraux, ou encore l’infarctus du myocarde.
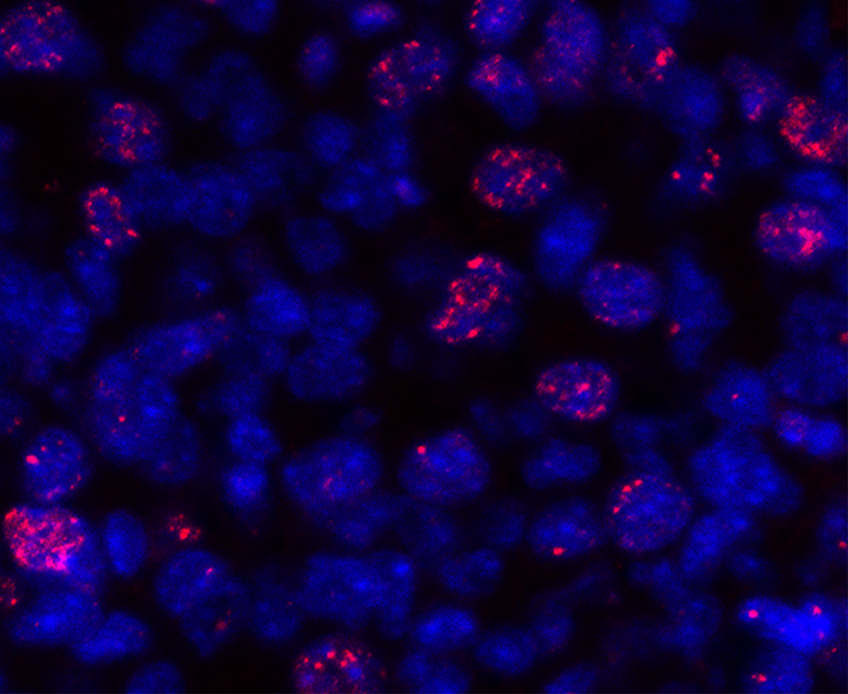
En analysant des tumeurs prélevées chez des patients atteints de cancer du pancréas, Olivier Soriani et Richard Tomasini ont remarqué que la distribution de SigmaR1 se superposait très exactement à celle de du canal SK2.
Dans cette configuration, SigmaR1 était-elle susceptible de contribuer à la mobilisation de SK2 dans les cellules cancéreuses du pancréas ? La réponse est positive : la présence de SigmaR1 est même absolument nécessaire à la stimulation de SK2 par les CAF, et pour cause : c’est SigmaR1 qui pilote l’association physique entre AKT et le canal SK2 !
Les chercheurs niçois et marseillais se sont alors tournés vers Patricia Melnyk, chimiste lilloise spécialisée dans la synthèse de petites molécules de type ligands pour des cibles impliquées dans les pathologies du SNC, parmi elles, SigmaR1. Les résultats obtenus avec l’un des ligands sigma qu’elle développe dans son laboratoire sont extrêmement prometteurs : cette molécule inhibe, dans les cellules cancéreuses, l’activation de SK2 par les CAF en empêchant l’association AKT/SK2 via SigmaR1.
Mais les résultats les plus spectaculaires ont été observés in vivo, dans un modèle de souris modifiées génétiquement pour développer spontanément des cancers du pancréas.
Les chercheurs ont constaté la disparition totale des lésions tumorales dans le pancréas des souris traitées avec le ligand sigma ; en parallèle, la survie des animaux traités progresse considérablement, et ceci même si le traitement est mis en place après l’apparition des premières tumeurs.
Ces travaux démontrent pour la première fois le rôle des canaux ioniques dans le dialogue entre les cellules tumorales et les acteurs de leur écosystème. Des études complémentaires permettront de préciser la place de cette nouvelle voie thérapeutique utilisant des ligands sigma comme adjuvant aux traitements de référence ou comme traitement de première ligne. Les perspectives offertes par ces résultats pourraient s’élargir à d’autres cancers dans lesquels le rôle du stroma est prédominent (cancer du sein ou du colon).

Schéma décrivant le mécanisme par lequel la Fibronectine (FN) et le Collagène 1 (Col1) sécrétés par les fibroblastes associés au cancer (CAFs) stimulent l’axe de signalisation β-1-intégrine-EGFR-AKT via le canal SK2.
Panneau supérieur : Cible directe de l’AKT, le canal exerce une boucle de rétroaction positive de l’axe de signalisation stimulé de façon paracrine par les CAFs. La présence du canal au sein du complexe augmente la sensibilité des cellules cancéreuses du pancréas (PCC) à la FN et au Col1, renforçant la transition épithélio-mésenchymateuse (EMT) et la formation des métastases.
Panneau inférieur : La protéine chaperon SigmaR1 conditionne l’association locale entre le canal et ses partenaires et peut être spécifiquement ciblée par de petites molécules exogènes (ligands sigma, 1(S)) pour inhiber la communication intercellulaire entre les CAFs et les PCC, ce qui abolit la formation des métastases et augmente la survie in vivo.