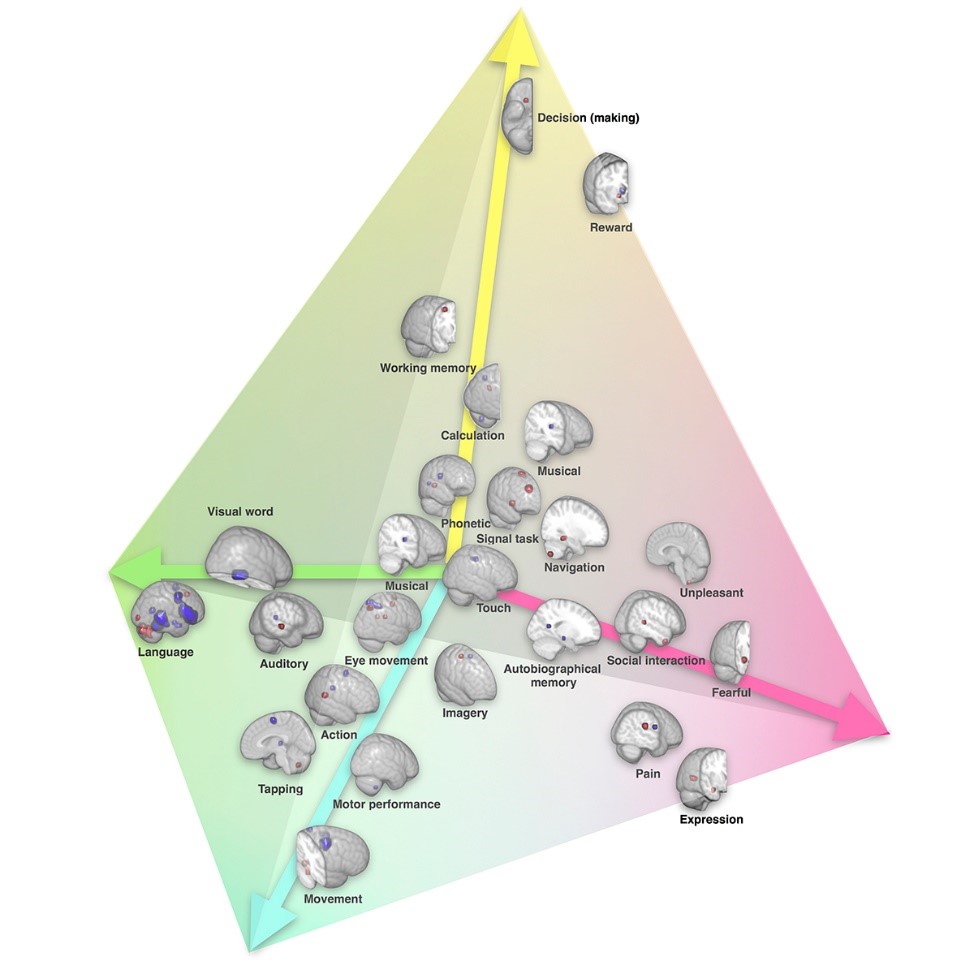
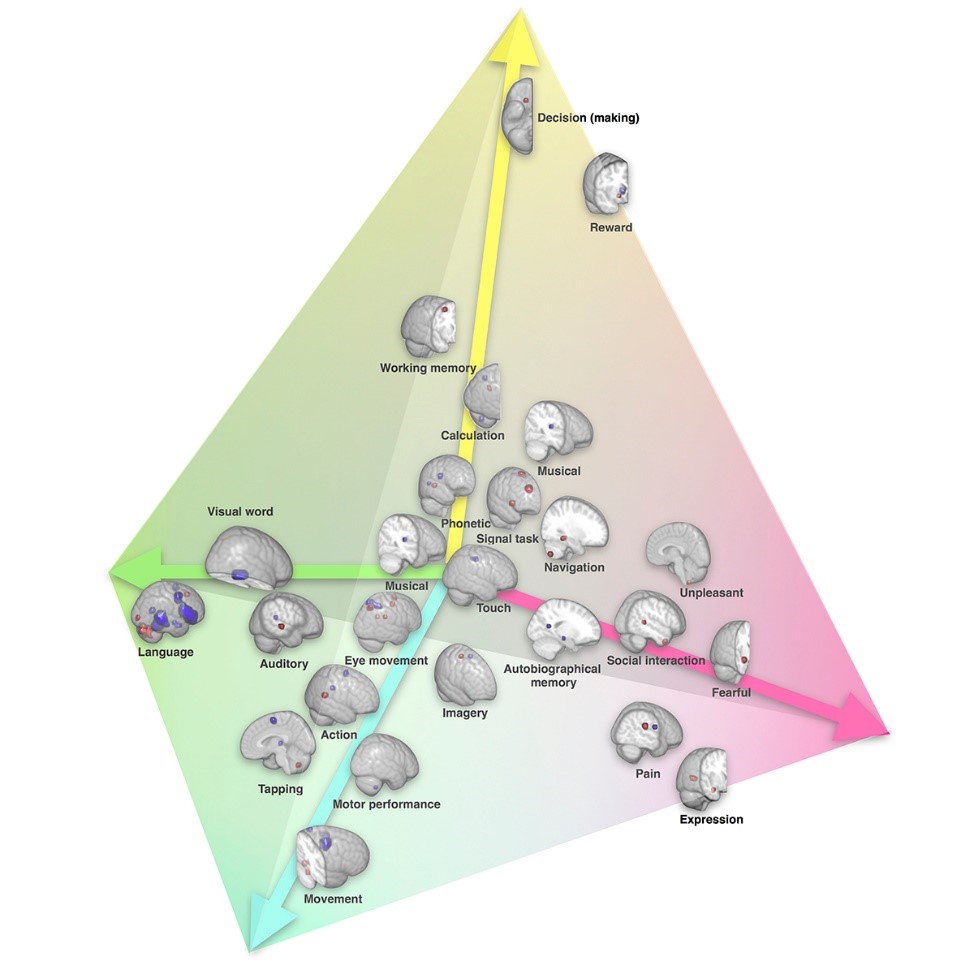
La latéralisation des fonctions cérébrales représentée dans un espace à 4 dimensions le long de l’axe de la communication symbolique (vert), l’axe de la « perception/action » (cyan), l’axe des émotions (rose) et l’axe de la prise de décision (jaune). ©Karoliset al./ Nature Communications
Certains processus cérébraux sont réalisés préférentiellement dans l’hémisphère droit ou l’hémisphère gauche du cerveau. Mais quelles fonctions et quel hémisphère ? Une équipe de recherche franco-italienne dirigée par un chercheur CNRS de l’Institut du cerveau et de la moelle épinière (AP-HP/CNRS/Inserm/Sorbonne Université) vient de répondre à cette question en livrant la première cartographie complète de la latéralisation des fonctions cérébrales, publiée le 29 mars 2019 dans la revue Nature Communications. Leurs résultats montrent pour la toute première fois que la prise de décision, comme la perception et l’action ainsi que les émotions, fait plus appel à l’hémisphère droit. Au contraire de la communication symbolique, qui repose plus sur l’hémisphère gauche.
En 1865, le médecin français Paul Broca notait que parmi les patients souffrant d’une lésion cérébrale, seuls ceux touchés au lobe frontal gauche rencontraient des difficultés pour parler. Pour la première fois, on observait une asymétrie fonctionnelle entre les deux hémisphères. De nombreuses recherches s’en sont suivies pour essayer d’identifier l’hémisphère « dominant » des différentes fonctions cérébrales, sans pour autant donner lieu à une investigation globale de cette latéralisation…
Jusqu’aux récents travaux de Michel Thiebaut de Schotten, chercheur CNRS de l’Institut du cerveau et de la moelle épinière (AP-HP/CNRS/Inserm/Sorbonne Université), et de ses collègues italiens de l’Université de Padoue. Grâce aux données d’IRM fonctionnelle collectées à l’échelle mondiale depuis plus de quinze ans, ils ont produit la première carte globale de la latéralisation des fonctions cérébrales.
Les chercheurs ont ainsi identifié quatre groupes de fonctions extrêmement latéralisées utilisant des régions cérébrales communes : la communication symbolique (où l’on retrouve le langage, la lecture et le calcul, par exemple) très latéralisée à gauche ; le groupe « perception/action » et les émotions latéralisés à droite et enfin la prise de décision, qui reposerait plutôt sur des régions du lobe frontal droit. Ce dernier point est tout à fait novateur, aucune équipe n’ayant encore décrit d’asymétrie entre les hémisphères lors de la prise de décision.
En outre, cette étude a permis de trancher une question épineuse quant aux connexions entre hémisphères: les régions très latéralisées sont-elles peu connectées avec l’autre hémisphère pour traiter plus rapidement l’information, ou au contraire sont-elles très connectées pour pouvoir s’influencer et prendre le dessus sur l’hémisphère opposé dans certains cas ? Grâce à leur carte, les chercheurs ont pu montrer que plus les fonctions sont latéralisées, moins elles établissent de connexions avec l’autre hémisphère, validant ainsi l’hypothèse qu’un hémisphère dominant pour une fonction est peu connecté à l’autre pour gagner en efficacité.
Aussi, cette découverte valide l’idée que les fonctions cérébrales se sont latéralisées avec l’augmentation de la taille du cerveau afin d’optimiser le traitement de l’information. Cette optimisation s’est néanmoins faite au dépend d’un autre avantage évolutif : la récupération fonctionnelle après une lésion cérébrale. À cause de la diminution des connexions entre les hémisphères, il est en effet plus difficile pour l’hémisphère non endommagé de pallier les fonctions perdues.
Les chercheurs souhaitent maintenant poursuivre ces travaux en étudiant les variations de latéralisation des fonctions entre individus, et tester par exemple si une forte latéralisation d’une fonction chez une personne entraîne une latéralisation différente d’autres fonctions.


 © AdobeStock
© AdobeStock