Certaines personnes se souviennent de leurs rêves tous les matins alors que d’autres s’en souviennent rarement. L’équipe de Perrine Ruby, chargée de recherche Inserm, au sein du centre de recherche en neurosciences de Lyon (Inserm / CNRS / Université Claude Bernard Lyon 1) a étudié l’activité cérébrale de ces rêveurs afin de comprendre ce qui les différencient. Dans une étude publiée dans la revue Neuropsychopharmacology, les chercheurs montrent que la jonction temporo-pariétale, un carrefour du traitement de l’information dans le cerveau, est plus active chez les grands rêveurs. Elle induirait une plus grande réactivité aux stimulations extérieures, faciliterait ainsi le réveil au cours du sommeil, ce qui favoriserait la mémorisation des rêves.
L’origine du rêve continue d’être un mystère pour les chercheurs qui étudient la différence entre les « grands rêveurs », qui parviennent à se souvenir de leurs rêves régulièrement, et les « petits rêveurs » pour lesquels cet événement est plus rare. En janvier 2013 (travaux publiés dans la revue Cérébral Cortex), l’équipe de Perrine Ruby, chargée de recherche à l’Inserm et ses collaborateurs du centre de recherche en neurosciences de Lyon, ont réalisé deux constats : les « grands rêveurs » comptabilisent 2 fois plus de phases de réveil pendant le sommeil que les « petits rêveurs » et leur cerveau est plus réactif aux stimuli de l’environnement. Cette sensibilité expliquerait une augmentation des éveils au cours de la nuit et permettrait ainsi une meilleure mémorisation des rêves lors de cette brève phase d’éveil. Dans cette nouvelle étude, l’équipe de recherche a cherché quelles régions du cerveau différencient les grands des petits rêveurs en mesurant l’activité cérébrale spontanée en Tomographie par Emission de Positons (TEP) à l’éveil et pendant le sommeil chez 41 rêveurs volontaires.
Les volontaires ont été classés en 2 groupes : 21 « grands rêveurs » se souvenant de leur rêve en moyenne 5.2 fois par semaine et 20 « petits rêveurs » rapportant en moyenne 2 rêves par mois.
Les chercheurs ont mesuré avec le scanner TEP l’activité cérébrale des grands et petits rêveurs pendant l’éveil et pendant le sommeil. (Voir vidéo).
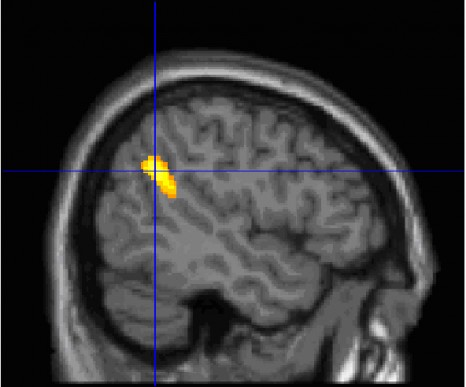
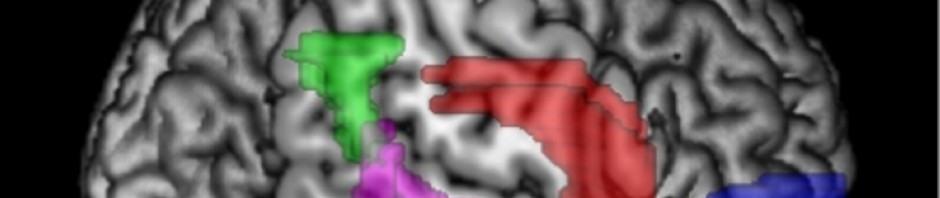
Les résultats révèlent que les grands rêveurs présentent une activité cérébrale spontanée plus forte pendant leur sommeil au niveau du cortex préfrontal médian (MPFC) et de la jonction temporo-pariétale (JTP), une zone cérébrale impliquée dans l’orientation de l’attention vers les stimuli extérieurs.
Jonction temporo-pariétale (JTP) © Perrine Ruby / Inserm
« Cela explique pourquoi les grands rêveurs réagissent plus aux stimuli de l’environnement et se réveillent plus au cours de leur sommeil que les petits rêveurs, et ainsi pourquoi ils mémorisent mieux leurs rêves. En effet le cerveau endormi n’est pas capable de mémoriser une nouvelle information en mémoire, il a besoin de se réveiller pour pouvoir faire ça »
explique Perrine Ruby, chargée de recherche à l’Inserm.
Le neuropsychologue sud-africain Mark Solms avait remarqué dans de précédents travaux que des lésions de ces deux zones conduisaient à une cessation des souvenirs de rêves. Les travaux de l’équipe lyonnaise ont pour originalité de mettre en évidence des différences d’activité cérébrale entre grands et petits rêveurs pendant le sommeil mais également à l’éveil.
« Ces résultats montrent que les grands et petits rêveurs se différencient en terme de mémorisation du rêve mais n’exclut pas qu’ils se différencient également en terme de production de rêve. En effet, il est possible que les grands rêveurs produisent une plus grande quantité de rêve » conclut l’équipe de recherche.