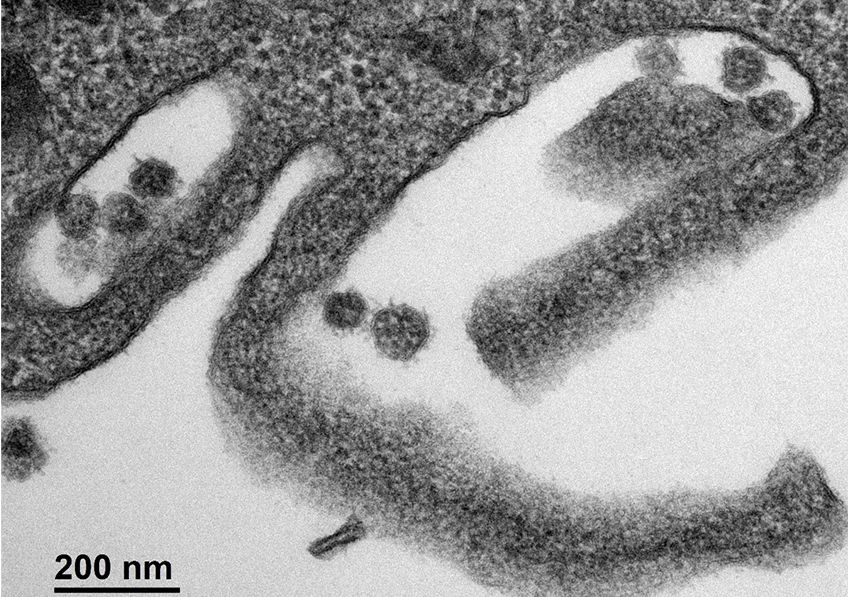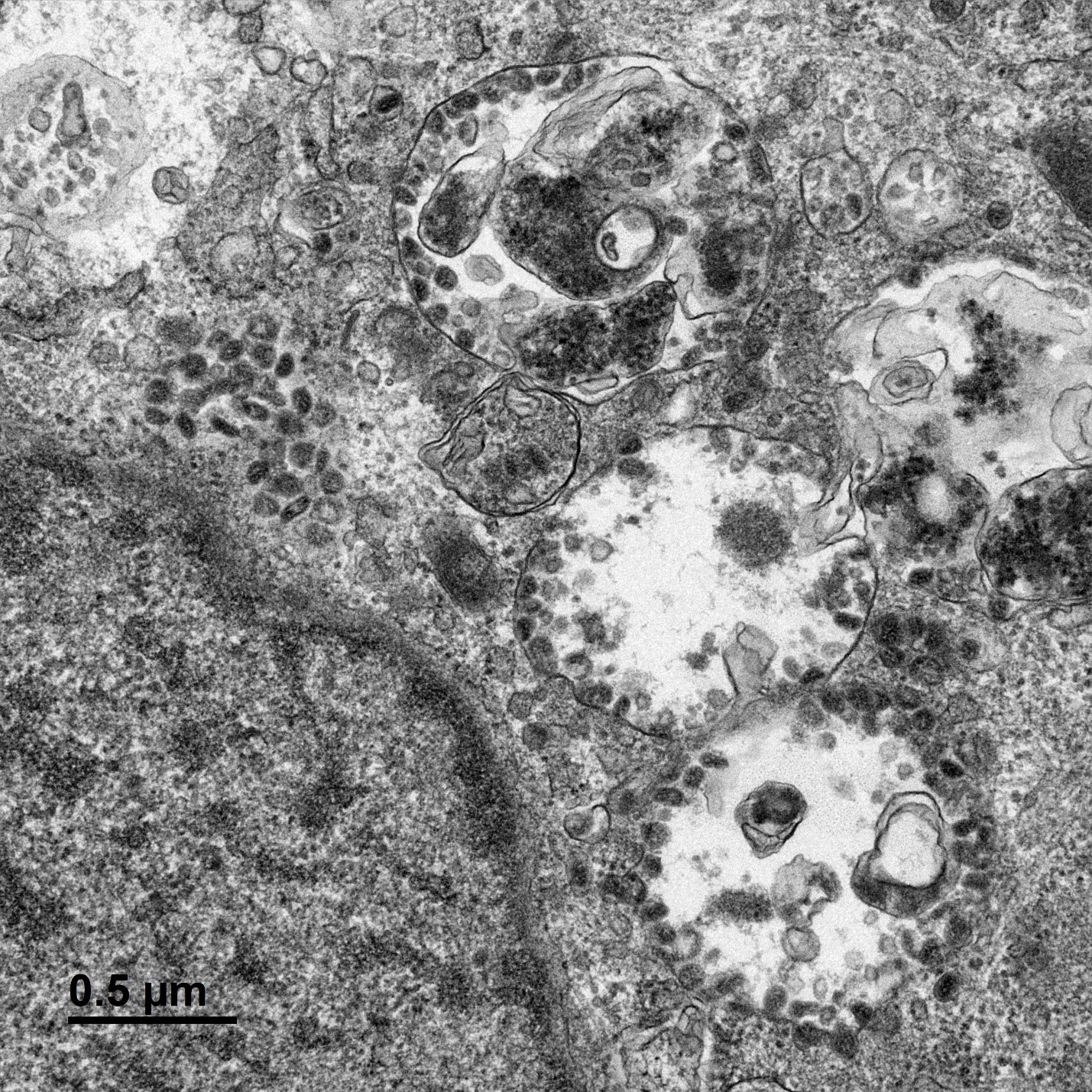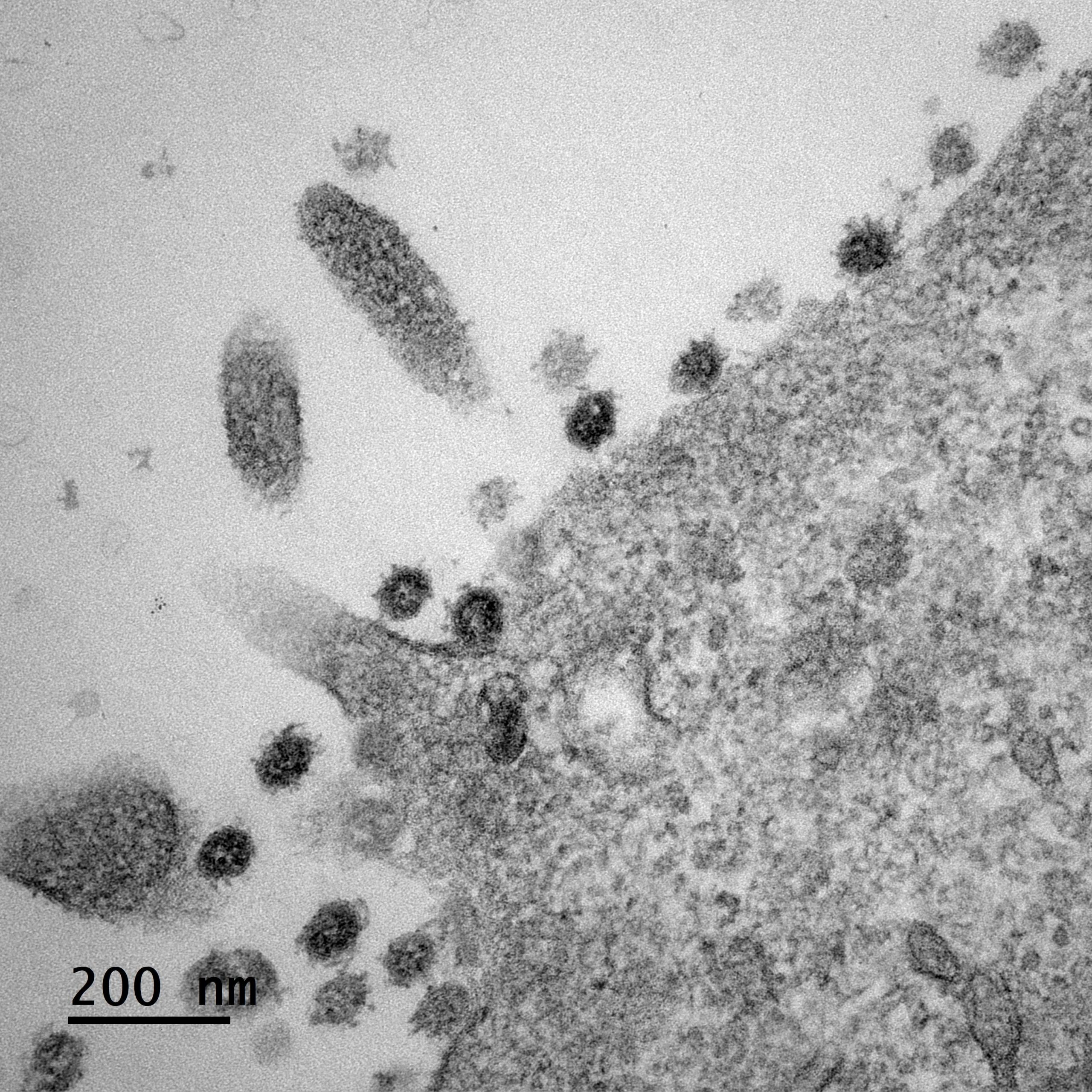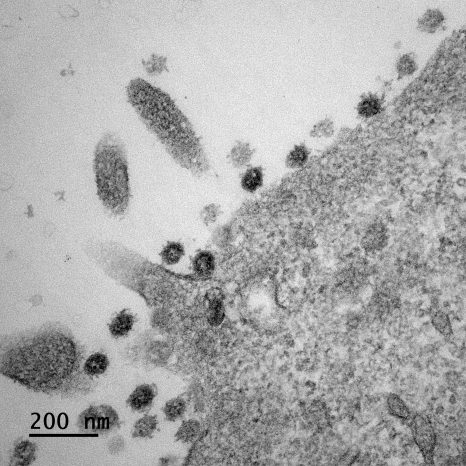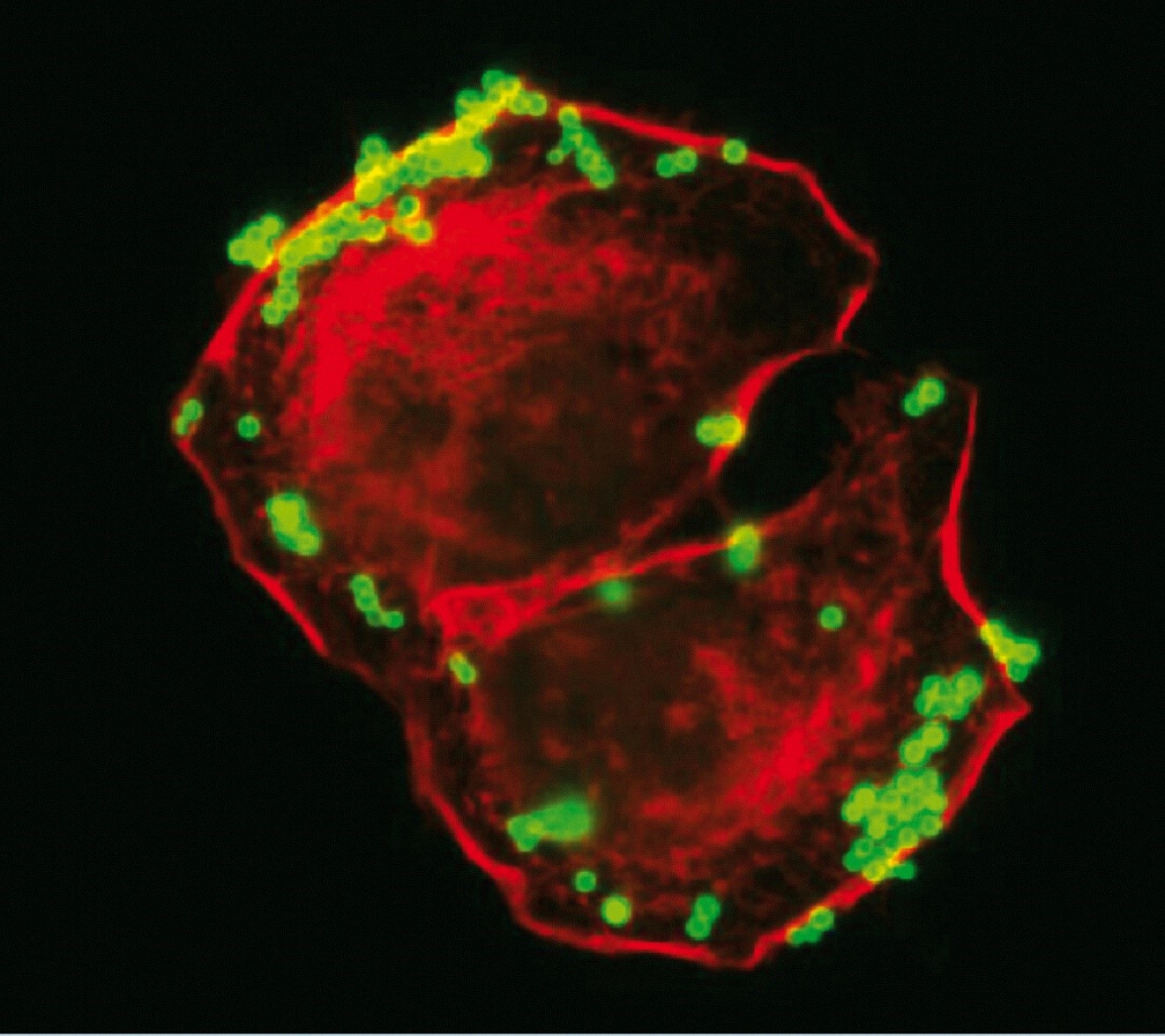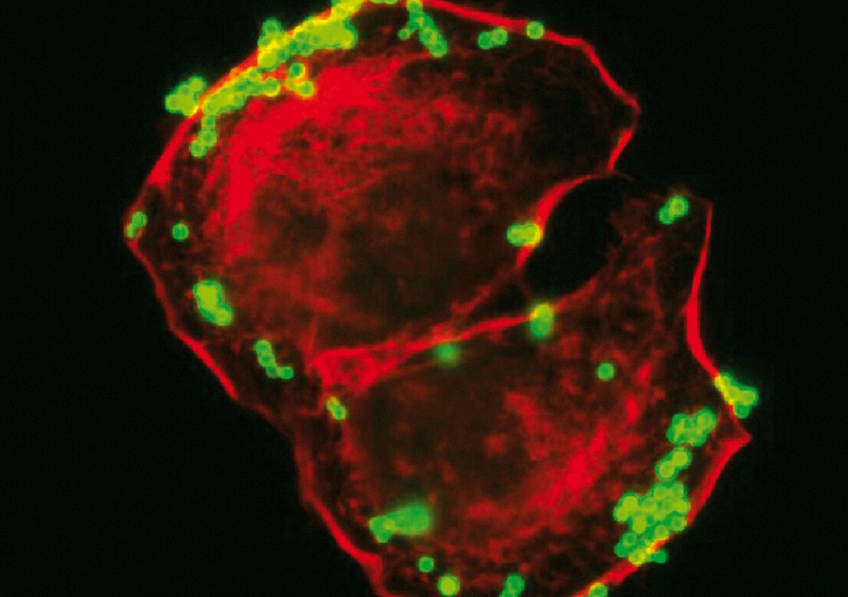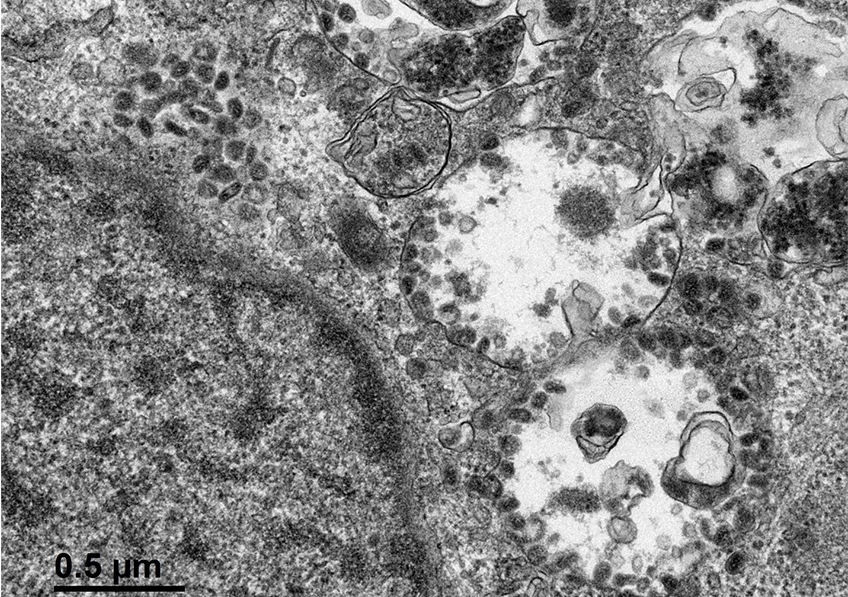
Cellules infectées par le SARS-CoV-2. ©Sébastien Eymieux et Philippe Roingeard, Inserm – Université de Tours
Apparu en décembre 2019 à Wuhan, au centre de la Chine, le nouveau coronavirus SARS-CoV-2 s’est très rapidement propagé à l’ensemble de la planète, entraînant la pandémie la plus grave de notre histoire récente. Dès le début de cette crise sanitaire mondiale, l’Inserm s’est mobilisé en tant qu’acteur de premier plan de la recherche biomédicale en France et à l’étranger, grâce à l’implication de ses nombreux experts sur des sujets liés aussi bien à la recherche fondamentale qu’à la thérapeutique ou à la modélisation de l’épidémie.
Un an après le début de la pandémie, alors que la plupart des pays initient leur campagne de vaccination et que l’émergence de variants ayant une incidence sur la transmission du virus marquent une nouvelle étape dans la lutte contre la Covid-19, les efforts de recherche à l’Inserm permettent chaque jour de nouvelles avancées dans la compréhension de la maladie, des facteurs de risque, de la dynamique de l’épidémie mais aussi une amélioration de la prise en charge et de la prévention.
La majorité des travaux publiés ont reçu un financement du fond d’amorçage du consortium REACTing, désormais intégré au sein de l’ANRS maladies infectieuses émergentes, la nouvelle agence créée au 1er janvier 2021. Ils concernent aussi bien la recherche fondamentale que la recherche thérapeutique et vaccinale, ou encore l’épidémiologie. De grandes cohortes ont par ailleurs été mises en place pour collecter des données de qualité permettant de répondre à des interrogations scientifiques capitales.
Jamais la mission portée par l’Inserm, la science pour la santé, n’a été aussi cruciale. Alors que de nombreuses questions restent en suspens, l’institution et ses chercheurs continuent à travailler, en collaboration avec leurs partenaires nationaux et internationaux, pour faire avancer les connaissances et éclairer les décisions publiques et la société en s’appuyant sur une recherche d’excellence alliant rigueur, transparence et éthique.
1. Les cohortes Covid-19, outil indispensable pour consolider les connaissances scientifiques en temps de pandémie
Les cohortes sont des groupes constitués d’un ensemble de personnes suivies individuellement dans le temps. Leur mise en place a pour objectif d’identifier la survenue d’événements de santé d’intérêt pour la recherche clinique ainsi que des facteurs de risque ou de protection. Elles constituent donc un instrument de référence pour la recherche épidémiologique et la santé publique.
En pleine pandémie, la constitution de larges cohortes de patients ou d’individus potentiellement à risque d’être exposés au virus permet aux scientifiques d’avoir accès rapidement à des données cliniques, biologiques et environnementales nombreuses, robustes et variées. Les équipe de recherche peuvent ainsi s’appuyer sur ces cohortes pour répondre à des interrogations scientifiques diverses, concernant aussi bien l’immunité, les facteurs de risque, l’efficacité des traitements, l’évolution et les symptômes de la maladie Covid-19 que l’impact socioéconomique ou encore psychologique de l’épidémie et des mesures de confinement sur les populations.
En France, plusieurs cohortes pilotées par l’Inserm ont été mises en place dès le début de la pandémie de Covid-19. En voici l’avancement sur quelques exemples non exhaustifs.
French Covid
Lancée fin janvier 2020, French Covid est une étude de cohorte française promue par l’Inserm. Elle repose sur le suivi d’un large groupe de patients ayant développé une forme clinique de la maladie qui nécessitait une hospitalisation, soit dans un service de médecine soit en réanimation. Au 20 janvier 2021, 4 300 patients avaient été inclus dans cette cohorte, la plus large cohorte française à l’heure actuelle de patients hospitalisés pour une infection par le SARS-CoV-2.
L’objectif est d’accumuler des connaissances sur la maladie Covid-19 et notamment sur les formes les plus graves, afin d’améliorer la prise en charge dans les cas où l’hospitalisation s’impose. La coordination de la cohorte est aujourd’hui confiée au Pr Jade Ghosn, chercheur au sein de l’unité 1137 IAME (Inserm/Université de Paris) et médecin infectiologue à l’hôpital Bichat AP-HP à Paris, en collaboration avec le Pr Catherine Chirouze, également infectiologue, au CHU de Besançon.
En plus des données cliniques et virologiques, des données immunologiques, génétiques, sérologiques, transcriptomiques sont collectées pour chaque participant afin de mieux caractériser la maladie et de définir le devenir des patients à court et à long terme (suivi jusqu’à 6 mois après le diagnostic).
Une étude fondée sur les données des premiers patients inclus avant le 15 mars 2020 a déjà été publiée en octobre 2020 dans The Journal of Medical Virology pour rendre compte de la mortalité dans la cohorte et des facteurs qui y étaient associés. Elle sera prochainement complétée par un article dans le journal PNAS portant sur le lien entre la dynamique de la charge virale et l’évolution de la maladie au cours du temps (mortalité).
Plusieurs groupes de recherche partenaires s’appuient également sur les données issues de French Covid pour mener leurs travaux, portant par exemple sur les facteurs génétiques associés aux formes graves de la maladie. Ainsi en septembre, deux publications dans la revue Science ont décrit les premières causes génétiques et immunologiques expliquant 15 % des formes graves de Covid-19. Elles soulignaient notamment que ces patients présentaient un défaut d’activité des interférons de type I (des protéines impliquées dans la réponse immunitaire).
D’autres travaux sont également menés à partir de la cohorte pour analyser l’impact de certains traitements (corticoïdes et hypertenseurs notamment) sur l’évolution des patients ou la persistance de séquelles. Enfin, les données de sérologie des participants ont aussi été utilisées afin de tester et de mettre au point de nouveaux tests de dépistage. Ainsi, une étude parue en décembre 2020 s’appuyant à la fois sur French Covid et sur la cohorte CoV-Contact (voir ci-après) a montré que l’identification d’un marqueur spécifique du virus dans les échantillons sanguins offrait une alternative intéressante de dépistage du virus.
Enfin, alors que les 1 000 premiers patients inclus dans la cohorte French Covid viennent d’atteindre les six mois de suivi, les chercheurs souhaitent désormais se pencher plus précisément sur la problématique de la persistance de certains symptômes à long terme.
French Covid est intégrée au consortium ISARIC basé à Oxford qui regroupe les données de plus de 100 000 patients à travers le monde et dont le but est de prévenir et de mieux comprendre les maladies infectieuses émergentes. À ce titre, ces données sont analysées dans le cadre de travaux de recherche internationaux publiés par ISARIC. Elle fait aussi partie du projet européen Orchestra (voir ci-après) et a reçu le label « priorité nationale de recherche » du comité CAPNET.
CoV-Contact
La cohorte CoV-Contact est une cohorte portant sur 300 à 350 personnes. Elle vise à mieux connaître les facteurs individuels associés au développement de la maladie Covid-19, après une exposition à risque de transmission du virus SARS-CoV-2. Dans ce but, des prélèvements à visée virologique et génétique sont réalisés sur les participants.
En septembre 2020, une étude parue dans Médecine et maladies infectieuses s’appuyant sur la cohorte CoV-Contact a évalué l’évolution clinique, virologique et immunologique à la suite d’un contact à risque non protégé avéré et daté parmi les professionnels de santé.
Elle a montré que la proportion des professionnels de santé infectés à la suite d’un contact professionnel à risque est très élevée et qu’un quart de ces infections sont asymptomatiques.
EpiCoV
La cohorte EpiCoV s’appuie sur un échantillon représentatif de 135 000 personnes sélectionnées par l’Insee pour représenter toute la diversité de la population vivant en France.
Porté par l’Inserm et la Direction de la recherche, des études, de l’évaluation et des statistiques (Drees) du ministère des Solidarités et de la Santé, en lien avec leurs partenaires (Insee, Santé publique France, CNRS, Ined, Université Paris-Saclay), le projet EpiCOV est une large étude épidémiologique, adossée à une grande enquête statistique, proposant de fournir une cartographie globale et scientifiquement fiable du statut immunitaire de la population et de sa dynamique, sur l’ensemble du territoire, via la collecte d’échantillons biologiques (auto-prélèvement d’une goutte de sang sur un papier buvard) couplée à des questionnaires.
L’objectif est de renseigner sur la diffusion du virus dans la population mais aussi sur les conséquences de l’épidémie sur le quotidien, les problématiques socioéconomiques et la santé des individus.
Les résultats de la première campagne d’interrogation, fondée sur 135 000 réponses aux questionnaires rempli en mai 2020 ainsi que sur 12 000 analyses sérologiques réalisées sur les prélèvements envoyés par les participants, témoignent de la situation en France au printemps.
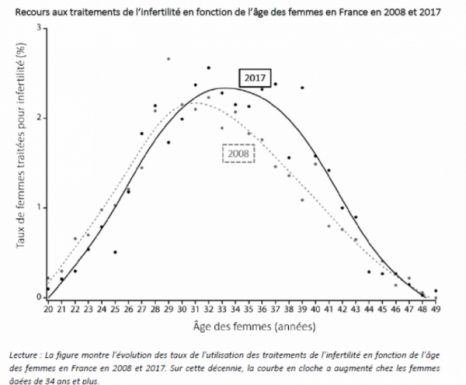
En France métropolitaine, 4,5 % des personnes de 15 ans ou plus avaient été en contact avec le virus en mai 2020. Cette part est plus importante parmi les 30-49 ans, dans les communes les plus densément peuplées et pour les personnes habitant dans des logements surpeuplés.
Une nouvelle campagne de questionnaires a été lancée à l’automne, afin d’assurer un suivi de l’évolution de la situation sanitaire au fil des mois.
Sapris
Sapris est une large enquête pilotée par l’Inserm qui s’appuie sur les grandes cohortes épidémiologiques françaises Constances, E3-E4N, NutriNet-Santé et Elfe-Epipage2. Elle vise là aussi à mieux comprendre la diffusion du virus dans la population et les conséquences de la pandémie sur la vie des individus.
Via un questionnaire en ligne, l’enquête coordonnée par Nathalie Bajos, sociologue-démographe et directrice de recherche Inserm, vise à évaluer l’évolution du nombre de personnes atteintes, les modes de transmission de la maladie, sa sévérité, les caractéristiques cliniques et les facteurs de risque d’infection et de complication, les conséquences sociales, économiques et psychologiques du confinement, mais aussi le recours au système de santé et la prise en charge.
Les grandes cohortes nationales sur lesquelles s’appuient les investigateurs de Sapris constituaient déjà une mine d’informations sur la santé, le mode de vie et le contexte social des participants. En s’appuyant sur toutes ces données déjà disponibles et en proposant des questionnaires axés sur la Covid-19 et son impact, ces cohortes françaises permettent de mieux appréhender l’évolution de l’épidémie.
L’étude Sapris comprend également un volet sérologique (le projet Sapris-Sero), s’intéressant aux échantillons biologiques de 14 600 participants interrogés pendant le premier confinement, sous la responsabilité de Fabrice Carrat, spécialiste en épidémiologie des virus, en coresponsabilité avec les responsables des cohortes participant à Sapris.
Les premiers résultats parus à l’automne 2020 suggèrent une proportion de tests positifs nettement plus élevée chez les personnes ayant présenté des symptômes évocateurs de Covid-19, comme les scientifiques en avaient fait l’hypothèse. Toutefois, 20 % des participants testés positifs n’ont présenté aucun symptôme.
Lancement de projets européens de grande ampleur s’appuyant sur des cohortes
Orchestra
Ce projet de recherche européen, lancé en décembre 2020 pour une durée de trois ans sous la direction de la chercheuse Evelina Taccinelli à l’université de Vérone, a pour objectif de créer une grande cohorte pan-européenne, regroupant des cohortes déjà existantes dans 15 pays, dont la France. Vingt-six institutions de recherche sont impliquées dont l’Inserm.
Bénéficiant d’un financement de plus 20 millions d’euros dans le cadre du programme de recherche et d’innovation européen Horizon 2020, le projet Orchestra vise à mettre en œuvre un suivi à long terme de milliers de personnes de tout âge, ayant été infectées ou non par le SARS-CoV-2, pour répondre à plusieurs questions de recherche qui persistent et pour guider les politiques publiques mises en place en réponse à la pandémie en Europe.
En s’appuyant sur les données collectées dans les cohortes des pays participants, la communauté scientifique souhaite en effet accroître les connaissances pour mieux protéger les populations les plus vulnérables et réduire les risques pour les soignants, étudier l’impact à long terme de la Covid-19 sur la santé et le bien-être des individus, mieux comprendre comment les populations répondent à la vaccination et enfin analyser l’influence de facteurs socioéconomiques et environnementaux sur la diffusion de l’épidémie.
Côté français, French Covid, Cov-Contact et Epicov sont incluses dans cette grande cohorte internationale : les informations collectées auprès des participants viendront donc alimenter cette grande base de données et soutenir les efforts de recherche à l’international, ainsi que la décision publique au niveau européen.
Respond
Il s’agit de l’un de quatre projets sélectionnés par l’Union européenne pour étudier les effets de la pandémie à long terme sur la santé et sur le comportement des personnes. Quatorze partenaires européens, dont l’Inserm via l’implication de la chercheuse Maria Melchior et de ses équipes, collaboreront avec l’OMS pour investiguer les effets des confinements sur le bien-être et la santé mentale des individus au cours des trois prochaines années.
Les chercheurs s’appuieront pour cela sur les données de grandes cohortes internationales ainsi que sur des registres de santé accessibles en Suède, en Italie et en Espagne. L’objectif est également d’étudier les liens qui existent entre respect des mesures de confinement et certaines caractéristiques spécifiques aux individus (par exemple le lien entre détresse psychologique et respect des mesures de restriction).
Par ailleurs, les équipes s’intéresseront à l’efficacité de programmes mis en place par l’OMS pour réduire les problèmes d’anxiété et de dépression pendant la crise sanitaire, en se penchant tout particulièrement sur certains groupes plus « vulnérables » comme les soignants, les jeunes, les migrants, les personnes ayant perdu leur emploi et/ou en situation précaire.
2. Actualités de la rentrée : de nouveaux travaux pour accroître les connaissances scientifiques
Alors que la lutte contre la pandémie se poursuit dans les laboratoires de recherche et dans les hôpitaux, de nombreux projets ont connu ces derniers mois des avancées significatives. En ce début d’année, plusieurs équipes Inserm dévoilent de nouveaux résultats, concernant des aspects de recherche fondamentale mais aussi de prise en charge des patients ou encore l’impact de la pandémie sur la société.
Évaluer l’impact de la pandémie de la Covid-19 sur la santé et la vie sociale des jeunes adultes
Au début de la pandémie de Covid-19, l’attention publique a été portée sur les personnes âgées, considérées comme plus vulnérables car plus à risque de développer des formes graves de la maladie. D’abord absents dans le débat public, les jeunes adultes ont été rapidement stigmatisés en raison de préjugés quant à leur irresponsabilité face à la pandémie durant l’été.
Afin de documenter la manière dont la pandémie de Covid-19 affecte la santé et la vie sociale des jeunes adultes (18-29 ans), un consortium de recherche regroupant des chercheurs français et canadiens s’est alors constitué entre l’Inserm (Marie Jauffret-Roustide, sociologue, PI) et l’université de Colombie-Britannique à Vancouver (Rod Knight, chercheur en santé publique PI ; Pierre-julien Coulaud, coordinateur scientifique ; et Naseeb Bolduc, coordinatrice opérationnelle).
Menée grâce à un premier financement de l’Institut de recherche en santé du Canada (IRSC), cette recherche intitulée Focus (pour France-Canada Observatory on Covid-19, Youth health and Social well-being) a été impulsée afin de documenter l’impact de la pandémie sur la santé mentale, les conduites addictives, la santé sexuelle et la vie sociale et économique des jeunes adultes.
L’enquête Focus s’articule autour de deux volets complémentaires impliquant la mise en place d’une enquête en ligne (volet quantitatif) et la réalisation d’entretiens semi-directifs auprès des jeunes (volet qualitatif). Le volet quantitatif de la recherche mené entre octobre et décembre 2020 a permis à près de 4 000 jeunes dans chaque pays de partager leurs expériences sur les six mois précédant l’enquête.

Cette enquête s’inscrit aussi dans une démarche de recherche participative par la mise en œuvre d’un conseil de jeunes adultes qui aide à mieux orienter et à adapter les travaux de recherche. Crédit : Adobe Stock
Les premières analyses montrent qu’une large majorité des jeunes adultes interrogés rapportent appliquer les gestes barrières (par exemple 86 % respectent le port du masque et 91 % se lavent régulièrement les mains) et viennent ainsi contredire les stéréotypes concernant leur irresponsabilité. Elles démontrent également que la pandémie affecte très fortement la santé des jeunes, et particulièrement leur santé mentale. Près de 3 jeunes sur 4 ont déclaré éprouver un sentiment de solitude, 66 % sont très anxieux et la moitié des jeunes interrogés (48 %) présentent des symptômes dépressifs modérés à sévères.
Ces données seront complétées par la réalisation d’entretiens sociologiques afin de mieux appréhender le vécu des jeunes et d’identifier les mesures urgentes à mettre en place pour améliorer leur bien-être et leur situation sociale et économique.
Cette enquête s’inscrit aussi dans une démarche de recherche participative par la mise en œuvre d’un conseil de jeunes adultes qui aide à mieux orienter et à adapter les travaux de recherche.
Une deuxième vague d’enquête est prévue au printemps 2021 et devrait permettre, grâce à des financements complémentaires, de construite une cohorte de jeunes adultes en France et au Canada afin d’étudier les effets à moyen et long terme de la pandémie de Covid-19 sur leurs trajectoires de vie et leur santé dans deux contextes sociopolitiques et économiques spécifiques. Elle est le reflet d’une collaboration internationale fructueuse entre l’Inserm et l’université de Colombie-Britannique.
Mieux comprendre le cycle infectieux du virus
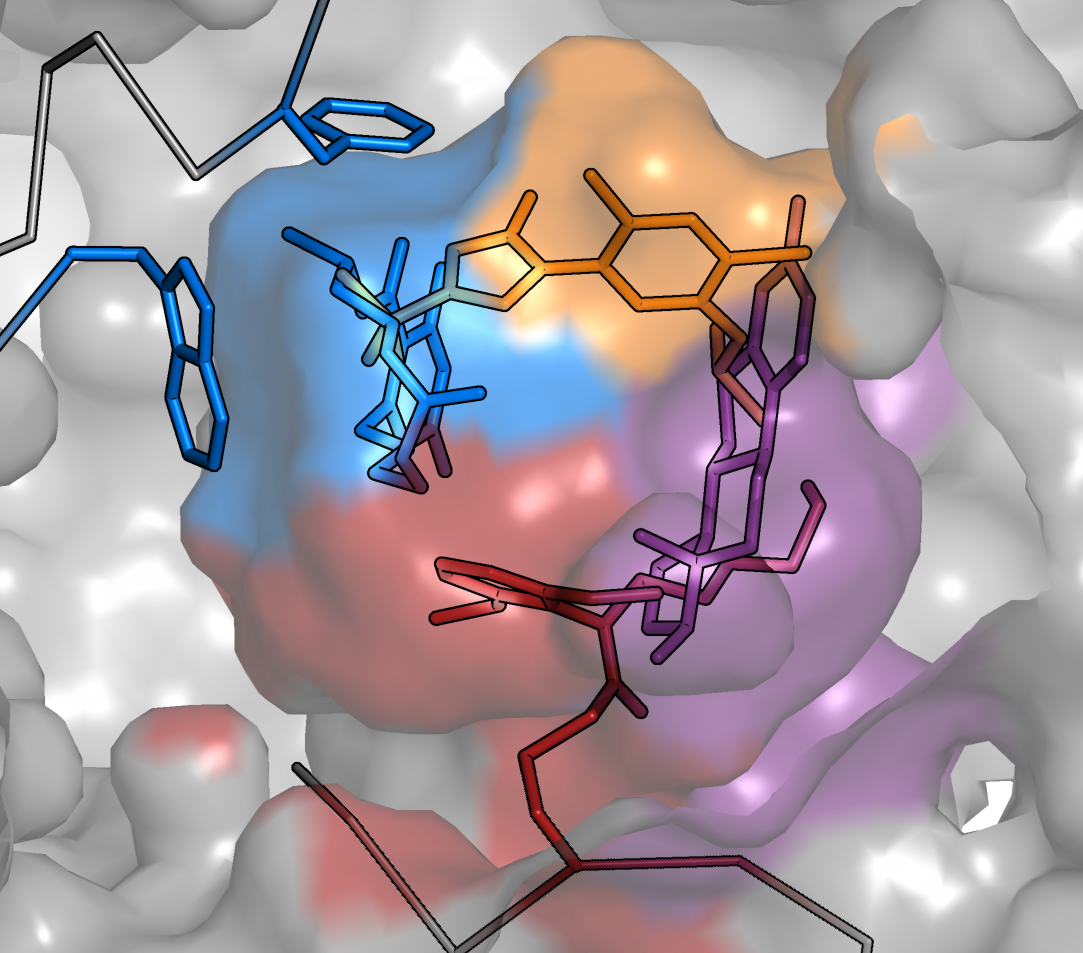
L’équipe de Philippe Roingeard à Tours s’attelle depuis le début de la pandémie à mieux comprendre la biologie fondamentale du SARS-CoV-2. À l’origine de photos du virus en microscopie électronique, les chercheurs se sont intéressés, dans une nouvelle étude parue dans Cellular and Molecular Life Science, aux étapes précoces et tardives du cycle infectieux.
Il s’agit de la première étude à se pencher de manière aussi minutieuse et détaillée sur le comportement du virus dans les cellules au cours du temps, en s’appuyant sur des techniques de microscopie électronique.
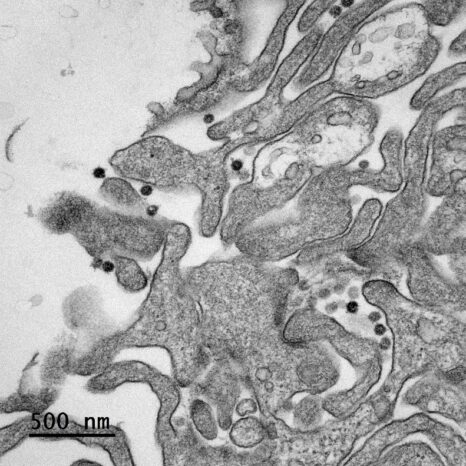
Cellule infectée par le SARS-CoV-2. Crédit : Sébastien Eymieux, Philippe Roingeard, Inserm/Université de Tours
L’étude, réalisée en collaboration avec l’institut Pasteur de Lille et le CIRI à Lyon, ouvre des pistes pour mieux comprendre les interactions entre le virus et les cellules. S’il était déjà clair que le SARS-CoV-2 induit des remaniements membranaires qui lui servent à ancrer ses complexes de réplication[1] dans les membranes afin de se protéger de la réponse immunitaire cellulaire, les chercheurs montrent comment ces remaniements s’opèrent. L’équipe rend compte de ces modifications structurales de la cellule qui interviennent à un stade très précoce de l’infection par le virus pour mieux comprendre comment le cycle infectieux se met en place, et à plus long terme pour identifier des stratégies permettant de bloquer ce processus.
L’étude montre aussi, pour la première fois, que lors des étapes tardives du cycle infectieux, des virus s’accumulent dans des grandes vacuoles intracellulaires. Les conséquences de ce phénomène ne sont pas encore bien comprises, mais cette accumulation pourrait être associée à la pathogénicité de la maladie.
Les chercheurs souhaiteraient désormais étudier le cycle infectieux dans d’autres types cellulaires, par exemple des cellules du tractus respiratoire, plus pertinentes pour la physiologie de l’infection, afin de confirmer leurs observations.
[1] Complexes enzymatiques intervenant dans la réplication du virus
Contact chercheur
Philippe Roingeard
U1259 MAVIVH
Université de Tours
rf.sruot-vinu.dem@draegnior
Le SARS-CoV-2 à l’assaut des neurones
L’infection par le virus SARS-CoV-2 est connue pour être caractérisée par des atteintes respiratoires importantes. Toutefois, des symptômes neurologiques ont également très rapidement et régulièrement été rapportés chez les patients. Ces symptômes vont des maux de tête aux pertes de mémoire et à la perte d’odorat en passant par des manifestations cliniques plus sévères comme des pertes de conscience et des AVC.
Dès le printemps 2020, Karen Richie, directrice de recherche émérite à l’Inserm, alertait sur les risques posés par le virus sur le cerveau et la moelle épinière dans une revue de littérature publiée dans Brain Communications. Elle et ses collègues y apportaient des pistes pour mieux appréhender le lien entre cerveau, difficultés psychiatriques et neurologiques, et épidémie de coronavirus.
Néanmoins, si des travaux expérimentaux ont souligné que des traces d’ARN du virus ont été retrouvées dans le cerveau de patients décédés de la Covid-19 et des protéines virales dans certaines cellules de leur bulbe olfactif, la capacité du virus à infecter les cellules du cerveau et les conséquences possibles n’avaient pas été démontrées jusqu’alors.
C’est l’objet d’une nouvelle étude publiée le 12 janvier 2021 dans le Journal of Experimental Medicine. En collaboration avec l’université de Yale aux États-Unis, des chercheurs de l’Inserm, de Sorbonne université et du CNRS à l’Institut du cerveau ainsi que de l’hôpital de la Pitié-Salpêtrière AP-HP ont utilisé trois approches différentes pour étudier l’infection dans le cerveau : des cultures de cellules cérébrales en 3D, un modèle murin d’infection au SARS-CoV-2 et des tissus cérébraux de patients décédés de la Covid-19.
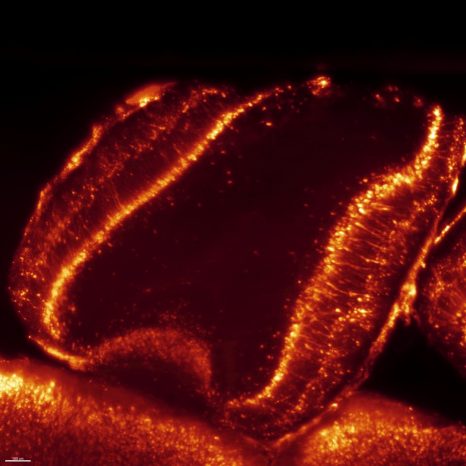
Photo en 3D par imagerie en feuillet de lumière de la présence du virus dans les neurones du bulbe olfactif. Crédit : Inserm/Nicolas Renier
Leurs résultats confirment le tropisme cérébral du SARS-CoV-2 et sa capacité à infecter les neurones. Ils suggèrent également que les symptômes neurologiques observés dans la Covid-19 pourraient être une conséquence de cette atteinte directe du système nerveux central.
Ces recherches doivent à présent se poursuivre pour identifier précisément la voie empruntée par le virus pour entrer dans le cerveau et confirmer le lien entre les changements cellulaires observés au niveau des neurones et les symptômes neurologiques rapportés.
Un meilleur pronostic vital des patients en réanimation
Parmi les facteurs associés à un risque plus élevé de décès chez les patients infectés par le SARS-CoV-2 figurent l’âge et un faible nombre de lymphocytes circulants. Une lymphopénie[1] importante causée par l’infection virale est en effet fréquemment observée chez les patients atteints de Covid-19 sévère et des modifications des lymphocytes T antiviraux ont été corrélées avec la sévérité de la Covid-19.
Dans une étude publiée début janvier dans la revue Critical Care, l’équipe des chercheurs Inserm Rémi Cheynier et Stefano Marullo à l’institut Cochin (Paris) en collaboration avec des cliniciens de la clinique Ambroise-Paré (Neuilly-sur-Seine) ont mené une étude chez des patients hospitalisés en réanimation pour forme grave de Covid-19 avec atteinte pulmonaire. Ils se sont intéressés au thymus, l’organe producteur des lymphocytes T (un type de globule blanc), dont le rôle dans ces formes sévères de Covid-19 n’avait pas encore bien été documenté.
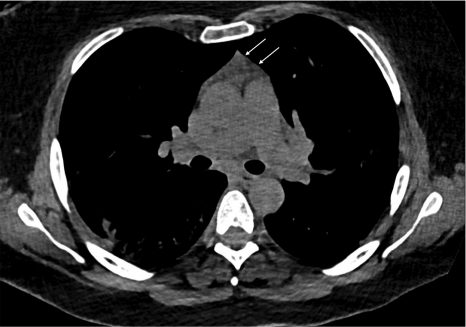
Une réactivation de la fonction du thymus est observée chez une majorité des patients survivant d’une Covid-19 sévère. Crédits : Rémi Cheynier.
En utilisant des scans pulmonaires sur 88 patients (dont 50 patients Covid et 37 patients témoins), les scientifiques ont systématiquement cherché à caractériser le degré d’hypertrophie du thymus[2]. Ils ont identifié une hypertrophie de cet organe chez de nombreux patients. Celle-ci s’accompagnait d’une production accrue de lymphocytes T, permettant de compenser la lymphopénie engendrée par le virus. Grâce à sa capacité à se réactiver et à produire massivement de nouvelles cellules T lors d’infections systémiques comme l’infection par le SARS-CoV-2, le thymus participe donc à la réponse immune antivirale. Un thymus hypertrophié est associé à un meilleur pronostic chez les patients hospitalisés en unité de soins intensifs pour Covid-19.
Une analyse scanner systématique du thymus permettrait de mieux évaluer les risques de développement d’une forme sévère de la maladie chez les patients hospitalisés pour Covid-19.
[1] Nombre anormalement faible de lymphocytes dans le sang
[2] L’hypertrophie thymique correspond à un développement anormal du thymus qui le fait enfler.
Les engelures, dommages collatéraux d’une immunité performante
Les engelures sont des atteintes cutanées douloureuses qui apparaissent en réaction au froid. Dues à des troubles de la microvascularisation cutanée, elles se manifestent par des doigts rouges ou violacés, avec parfois la présence de petites cloques pouvant prendre un aspect nécrotique. Une fréquence inédite de consultations pour engelures a été rapportée en Italie puis en France dès le début de la pandémie de Covid-19.
Afin d’évaluer leurs liens avec l’infection par le SARS-CoV-2, une équipe de chercheurs menée par Thierry Passeron (unité 1065 Inserm/Université de Nice Sophia Antipolis) a mis en place une étude auprès des personnes reçues par la cellule Covid du CHU de Nice entre le 9 et le 17 avril et qui présentaient ce type de lésions. Au cours de cette période, 40 patients souffrant d’engelures ont été accueillis. Aucun d’entre eux n’avait présenté une forme grave de Covid-19 et la plupart étaient jeunes (âge médian de 22 ans). S’ils avaient tous été cas contacts ou suspectés d’être infectés par le SARS-CoV-2 dans les 3 semaines précédant la consultation, le résultat de la recherche du virus au niveau nasopharyngé (PCR) était négatif pour l’ensemble de ces patients, et une sérologie positive n’a été retrouvée que chez un tiers d’entre eux.
En analysant ces chiffres, si la causalité entre les lésions cutanées et le SARS-CoV-2 n’est pas démontrée, elle est malgré tout fortement suspectée par les scientifiques, notamment parce que le nombre de patients présentant des engelures à cette époque de l’année dans cette région du sud de la France est particulièrement surprenant.
Se fondant sur les données biologiques et cliniques des patients concernés – leur âge plutôt jeune, la rareté de leurs symptômes associés à la Covid-19 ou encore la négativité des tests PCR et sérologiques –, les chercheurs estiment que les engelures sont la conséquence d’une immunité innée particulièrement efficace. Si les formes graves de Covid-19 semblent liées à un défaut de l’immunité adaptative, qui rend impossible une production suffisante de cellules et d’anticorps spécifiques du SARS-CoV-2, les engelures seraient à l’inverse l’illustration d’une surréaction de l’immunité innée. Cette diversité de réponses reposerait sur des variants génétiques associés à l’activité des médiateurs de l’immunité. Plus d’informations sur cette étude sur le site Inserm.fr.
Repositionnement thérapeutique d’un hypertenseur
Dans le cadre du consortium REACTing coordonné par l’Inserm, l’équipe Virpath, codirigée par les chercheurs Inserm Manuel Rosa-Calatrava et Bruno Lina au Centre international de recherche en infectiologie (Inserm/CNRS/Université Claude-Bernard-Lyon 1/ENS Lyon), travaille au repositionnement de médicaments déjà disponibles sur le marché en vue de nouvelles indications thérapeutiques contre les infections virales. Pour tester l’efficacité thérapeutique de ces molécules contre le SARS-CoV-2, l’équipe a développé et caractérisé des modèles précliniques prédictifs d’infections virales.
Pour être au plus proche de la physiologie humaine, elle utilise des épithéliums respiratoires humains d’origine nasale, bronchique ou alvéolaire cultivés en interface air-liquide. Elle a déjà montré dans ces modèles l’intérêt du diltiazem, un antihypertenseur utilisé dans le traitement de l’angine de poitrine. Celui-ci a déjà été caractérisé et repositionné par les chercheurs de VirPath afin de stimuler fortement la réponse immunitaire innée des épithéliums respiratoires, notamment contre les virus influenza, les pneumovirus et le SARS-CoV-2.
Plus récemment, à partir de modèles animaux, les chercheurs en collaboration avec les équipes de l’IDMIT ont pu confirmer le mode d’action de ce traitement sur le SARS-CoV-2 : le diltiazem stimule l’expression des gènes des interférons de type 3, des protéines impliquées dans la réponse immunitaire et qui ne sont pas associées à de hauts niveaux d’inflammation. Fort de ces résultats encourageants, une nouvelle étude préclinique devrait démarrer en février avec l’objectif de confirmer l’intérêt du diltiazem et de caractériser les doses efficaces optimales dans l’optique de mettre en place un éventuel essai chez l’Homme.
Contact chercheur
Manuel Rosa-Calatrava
Chercheur Inserm au CIRI
rf.1noyl-vinu@avartalac-asor.leunam