Des chercheurs de l’Inserm au sein de l’Unité mixte de recherche Inserm/Université Paris Descartes (Unité 970 « Paris Centre de recherche cardiovasculaire ») en collaboration avec l’AP-HP (Hôpital Européen Georges Pompidou, hôpital Saint-Louis et hôpital Necker) viennent de montrer que la présence d’anticorps chez des patients ayant subi une greffe de rein provoquait le rétrécissement accéléré des artères de petit et moyen calibre qui fournissent le sang au nouveau rein. Les résultats à paraître ce jour dans The Journal of the American Society Nephrology démontrent que le rétrécissement progressif des vaisseaux du rein appelé artériosclérose est particulièrement fréquent en cas de rejet lié aux anticorps.
© Fotolia
Deux à trois millions de Français souffrent de maladies rénales chroniques. Organes vitaux, les reins permettent d’épurer le sang de ses différents déchets et leur bon fonctionnement est nécessaire à la vie. En cas de non fonctionnement, un traitement de substitution est nécessaire. La transplantation d’un nouvel organe issu d’un donneur vivant ou décédé s’impose aujourd’hui comme le traitement de choix.
Une des problématiques majeures de la greffe rénale est la nécessité d’une compatibilité immunologique entre le donneur et le receveur. Néanmoins, la greffe peut être compromise lorsque les receveurs développent des anticorps contre leur greffon, provoquant un rejet sévère de l’organe transplanté. Malgré les avancées considérables dans le domaine des traitements immunosuppresseurs, le rejet lié aux anticorps est aujourd’hui une problématique majeure.
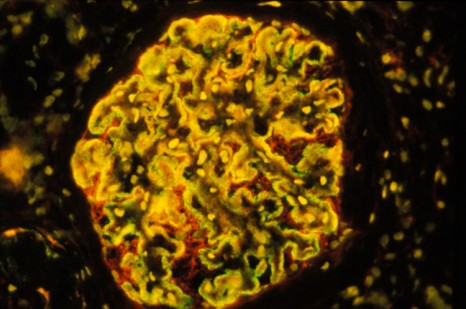
Dans cette étude, les chercheurs de l’Inserm ont analysé les caractéristiques des reins des patients transplantés en fonction de la présence d’anticorps dirigés contre leur donneur. Ils ont également comparé le vieillissement des vaisseaux de l’organe greffé au vieillissement vasculaire rénal physiologique.
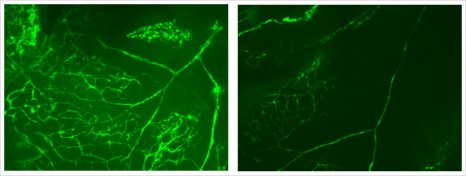
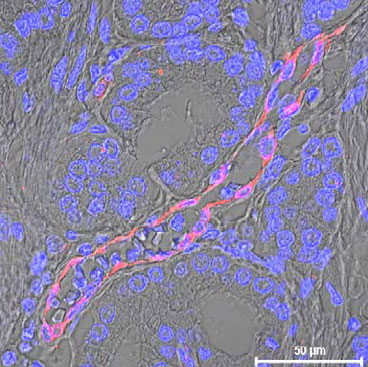
Leurs travaux démontrent que la présence d’anticorps dirigés contre le donneur induit un vieillissement prématuré de l’organe transplanté. Ce vieillissement se caractérise par un rétrécissement significatif du calibre des petites et moyennes artères du greffon appelé artériosclérose.
Les chercheurs ont constaté que le rétrécissement des artères progresse significativement entre trois et douze mois après la greffe chez les patients développant des anticorps comparativement à la progression classique de l’artériosclérose lié au vieillissement. Ainsi, en un an, le vieillissement observé en présence d’anticorps correspond au vieillissement normal s’étalant sur 28 ans pour une personne en bonne santé. Cette diminution du calibre de ces vaisseaux a potentiellement un impact délétère sur la fonction du greffon et in fine sur sa durée de vie.
Du rein au cœur
Cette étude à l’échelle humaine est concordante avec les résultats publiés issus de modèles murins qui soulignaient l’importance particulière de mécanismes immuns dans la survenue de l’artériosclérose.
« Nos résultats confortent l’intérêt de dépister ces anticorps précocement après la transplantation rénale et de développer des stratégies thérapeutiques ciblées afin de prévenir cette artériosclérose accélérée » déclarent Gary Hill et Alexandre Loupy, les principaux auteurs de cette étude.
Compte tenu du rôle majeur de l’artériosclérose dans le développement des maladies cardiovasculaires, nos résultats suggèrent par ailleurs que les sujets greffés représentent une population particulièrement à risque de morbidité et mortalité cardiovasculaire.
Le vieillissement normal des artères se nomme artériosclérose. Il se caractérise par une perte d’élasticité des vaisseaux et par une diminution de leur diamètre. Il arrive fréquemment que cette artériosclérose s’accompagne de dépôt de plaques graisseuses sur la paroi interne des vaisseaux. Lorsque ces fameuses plaques d’athérome se forment, elles obstruent encore plus la lumière des vaisseaux. On parle alors d’athérosclérose.