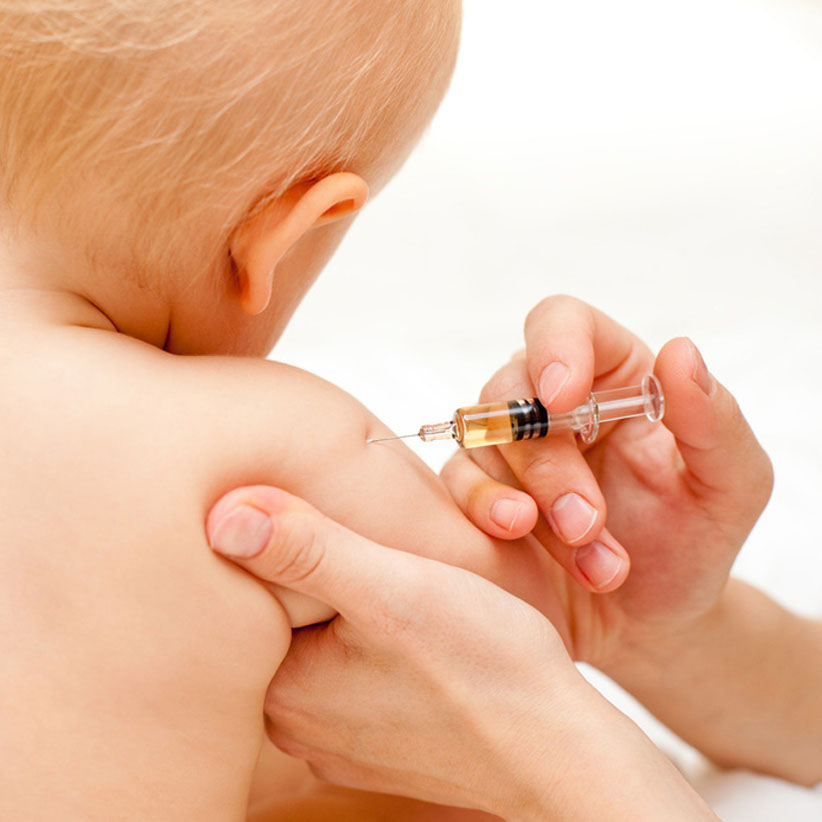
 Le nirsévimab est un anticorps ciblant le virus respiratoire syncytial (VRS). Mis à disposition en France depuis septembre 2023, il est indiqué chez les nouveau-nés et nourrissons dans la prévention des bronchiolites causées par le VRS. © AdobeStock.
Le nirsévimab est un anticorps ciblant le virus respiratoire syncytial (VRS). Mis à disposition en France depuis septembre 2023, il est indiqué chez les nouveau-nés et nourrissons dans la prévention des bronchiolites causées par le VRS. © AdobeStock.
Le nirsévimab est un anticorps ciblant le virus respiratoire syncytial (VRS). Mis à disposition en France depuis septembre 2023, il est indiqué chez les nouveau-nés et nourrissons dans la prévention des bronchiolites causées par le VRS. Sa large diffusion soulève cependant la question de l’apparition de mutations de résistance. La plus grande étude de surveillance prospective de la sensibilité au nirsévimab menée à ce jour, l’étude POLYRES, vient de livrer ses conclusions. Ces travaux coordonnés par les Pr. Slim Fourati et Marie-Anne Rameix-Welti[1] ont bénéficié d’un financement de l’ANRS MIE grâce au soutien du ministère de l’Enseignement supérieur et de la Recherche dans le cadre du Consortium EMERGEN.[2] Les scientifiques de l’AP-HP (dont ceux des Hôpitaux Universitaires Henri Mondor), de l’Inserm, de l’Institut Pasteur et des Université Paris-Est-Créteil et Université de Versailles-Saint-Quentin-en-Yvelines, membres des équipes du réseau de virologie de l’ANRS MIE, ont montré que les mutations de résistance au nirsévimab étaient très rares chez le VRS. Les résultats de l’étude viennent de paraître dans la revue Lancet Infectious Diseases du 15 octobre 2024.
Le virus respiratoire syncytial (VRS) est le principal virus responsable de la bronchiolite, une infection des voies respiratoires basses affectant le nourrisson. On distingue deux groupes de VRS (le VRS-A et le VRS-B) qui peuvent circuler en alternance ou ensemble. Chaque année, le VRS est responsable de plus de 33 millions de cas de bronchiolites dans le monde, conduisant au décès de 100 000 enfants essentiellement dans les pays à bas revenus. En France, cette pathologie est responsable d’environ 480 000 cas par an. Elle est de loin la première cause d’hospitalisation chez l’enfant, entrainant chaque année plus de 26 000 hospitalisations en pédiatrie. Le nirsévimab, un nouvel anticorps neutralisant* contre le virus, avait été mis à disposition en France en septembre 2023. Cet anticorps monoclonal** cible un site antigénique spécifique (l’épitope*** Ø) sur une protéine située à la surface du VRS impliquée dans la multiplication virale, la protéine de fusion F, et bloque ainsi le virus. Il existe un risque théorique d’émergence de variants du VRS portant des mutations de résistance à la neutralisation par le nirsévimab, même en absence de pression de sélection par l’anticorps. Le VRS est, en effet, un virus variable. Ce risque pourrait augmenter avec l’utilisation préventive généralisée du nirsévimab.
Lors des essais cliniques de phase IIb/III, seuls 48 VRS ayant infecté des enfants sous traitement par le nirsévimab avaient pu être étudiés, et des mutations d’échappement# avaient été retrouvées chez deux d’entre eux. L’étude POLYRES avait pour objectif d’évaluer le risque d’échappement virologique au nirsévimab sur un plus vaste échantillon grâce à une étude observationnelle, multicentrique, de grande envergure se déroulant en vie réelle au cours de la saison hivernale 2023-2024.
Dans cette étude, ont été inclus 695 nourrissons ayant une infection par le VRS, parmi lesquels 349 avaient reçu une prophylaxie par nirsévimab. Le VRS-A était majoritaire cette saison et a été retrouvé chez 86,6 % des enfants infectés. Les équipes ont analysé les caractéristiques des VRS-A et VRS-B présents dans les prélèvements nasopharyngés réalisés dans le cadre de la prise en charge habituelle des enfants. La séquence complète du génome viral a été déterminée pour rechercher en particulier des mutations dans le site de liaison (le site Ø) du nirsévimab (analyse génotypique§). La capacité du nirsévimab à inhiber la multiplication des virus en culture cellulaire a également été étudiée (analyse phénotypique¥). L’analyse de 472 VRS-A (dont la moitié provenant d’enfants traités) n’a révélé aucune mutation de résistance au nirsévimab dans le site Ø de la protéine F. Parmi les 73 enfants infectés par le VRS-B, 24 avaient reçus du nirsévimab en prophylaxie. Chez ces 24 enfants, deux isolats de VRS-B présentaient des mutations de résistance à l’anticorps, une déjà connue, l’autre inconnue et décrite ici pour la première fois.
« Cette étude est la plus vaste concernant des analyses virologiques d’échecs au nirsévimab à ce jour. Elle a pu être réalisée grâce à un travail synergique et collaboratif avec le consortium des virologues de l’ANRS MIE, et constitue un projet d’ampleur nationale qui permet d’identifier les phénomènes de résistance liés à la diffusion du médicament. Ce type d’études est essentiel pour analyser la dynamique d’évolution des virus, à la lumière de solutions médicales existantes » précise le Pr Marie-Anne Rameix-Welti, responsable du Centre national de référence des Virus des infections respiratoires à l’Institut Pasteur, et responsable de l’unité M3P (Institut Pasteur, Inserm U1173).
« La faible prévalence des mutations de résistance au nirsévimab chez des patients traités est rassurante. Toutefois quelques VRS-B issus de patients traités analysés à ce jour présentaient des mutations d’échappement, ce qui invite à la prudence et souligne l’importance d’une surveillance moléculaire active dans le contexte d’une future utilisation du nirsévimab à l’échelle mondiale. Ces résultats sont essentiels dans la lutte contre cette maladie et pour anticiper toute forme de résistance », ajoute le Pr Slim Fourati, responsable de l’unité de Virologie- Virus Respiratoires, CHU Henri Mondor, Inserm U955.
En conclusion, les résultats de l’étude POLYRES sont en faveur de la poursuite de l’utilisation du nirsévimab en prophylaxie pour tous les nouveau-nés dans le monde.
* Les anticorps neutralisants sont des anticorps particuliers empêchant l’infection en bloquant l’entrée du virus dans les cellules cibles. Ils le font en formant un complexe antigène-anticorps qui inhibe l’activité biologique de l’antigène (substance étrangère à l’organisme capable de déclencher une réponse immunitaire visant à l’éliminer).
** Les anticorps monoclonaux regroupent un seul type d’anticorps (les polyclonaux, plusieurs). Ils sont utilisés en médecine.
*** Partie d’une molécule reconnue par un anticorps.
# Les mutations d’échappement permettent au virus de déjouer l’action des anticorps du système immunitaire humain
- Les tests génotypiques sont basés sur l’identification de mutations conférant au virus un caractère de résistance.
¥ Le phénotypage, effectué par des tests phénotypiques, permet de définir le caractère sensible ou résistant du virus. Ceci se fait par culture du virus en présence de l’antiviral étudié.
[1] Responsable du Centre national de référence des Virus des infections respiratoires à l’Institut Pasteur et responsable de l’unité M3P (Institut Pasteur, Inserm U1173)
[2] Coordonné par Santé publique France et l’ANRS MIE


 © Photo de
© Photo de 

 © Adobe stock
© Adobe stock