La mise en œuvre généralisée du dépistage universel du VIH pendant la grossesse et de la thérapie antirétrovirale maternelle immédiate au cours de la dernière décennie a permis de réduire de manière significative les nouvelles infections pédiatriques par le VIH, sans toutefois les éliminer. Les infections pédiatriques au VIH restent à un niveau très élevé : l’ONUSIDA estiment à 130 000 le nombre de nouveaux cas en 2022, dont la plupart surviennent pendant l’allaitement. Pour améliorer la prévention de la transmission postnatale du VIH, le consortium PROMISE, composé de chercheurs du Centre hospitalier universitaire de Lusaka (Zambie), du Centre Muraz (Burkina Faso), de l’Université de Bergen (Norvège), de l’Inserm / Université de Montpellier (France), a évalué une stratégie innovante combinant des outils existants, notamment le dépistage chez le nourrisson et le contrôle de la charge virale maternelle à l’aide de tests sur le lieu de soins, et une prophylaxie post-natale prolongée. Les résultats de cette étude, financée par le European & Developing Countries Clinical Trials Partnership (EDCTP) et promue par l’ANRS MIE, ont été publiés dans le Lancet le 11 mars 2024.
Pendant la période postnatale, une proportion importante de mères vivant avec le VIH ne sont pas traitées efficacement par une trithérapie antirétrovirale (c’est-à-dire que leur charge virale est ≥ 1000 copies/mL, en raison d’une résistance ou d’une mauvaise observance au traitement). À l’époque où les antirétroviraux n’étaient prescrits qu’à partir d’un certain stade de l’infection VIH, le consortium PROMISE avait montré en 2016 qu’une prophylaxie postnatale pour les nourrissons, grâce au médicament appelé névirapine ou lamivudine, est efficace pour prévenir la transmission lorsque les mères n’étaient pas sous traitement antirétroviral[1]. Alors que le traitement antirétroviral maternel universel est aujourd’hui disponible, la valeur ajoutée de cette prophylaxie pour réduire la transmission postnatale, n’est pas connue. La prophylaxie infantile est actuellement donnée jusqu’à 6 à 12 semaines après la naissance, pour couvrir le risque périnatal. Étant donné que le risque de transmission persiste en fait tout au long de la période d’allaitement, il pourrait être important d’étendre la prophylaxie au-delà des 6 à 12 semaines actuelles, avec un maximum de 24 semaines, pour couvrir cette période d’exposition au VIH liée à l’allaitement.
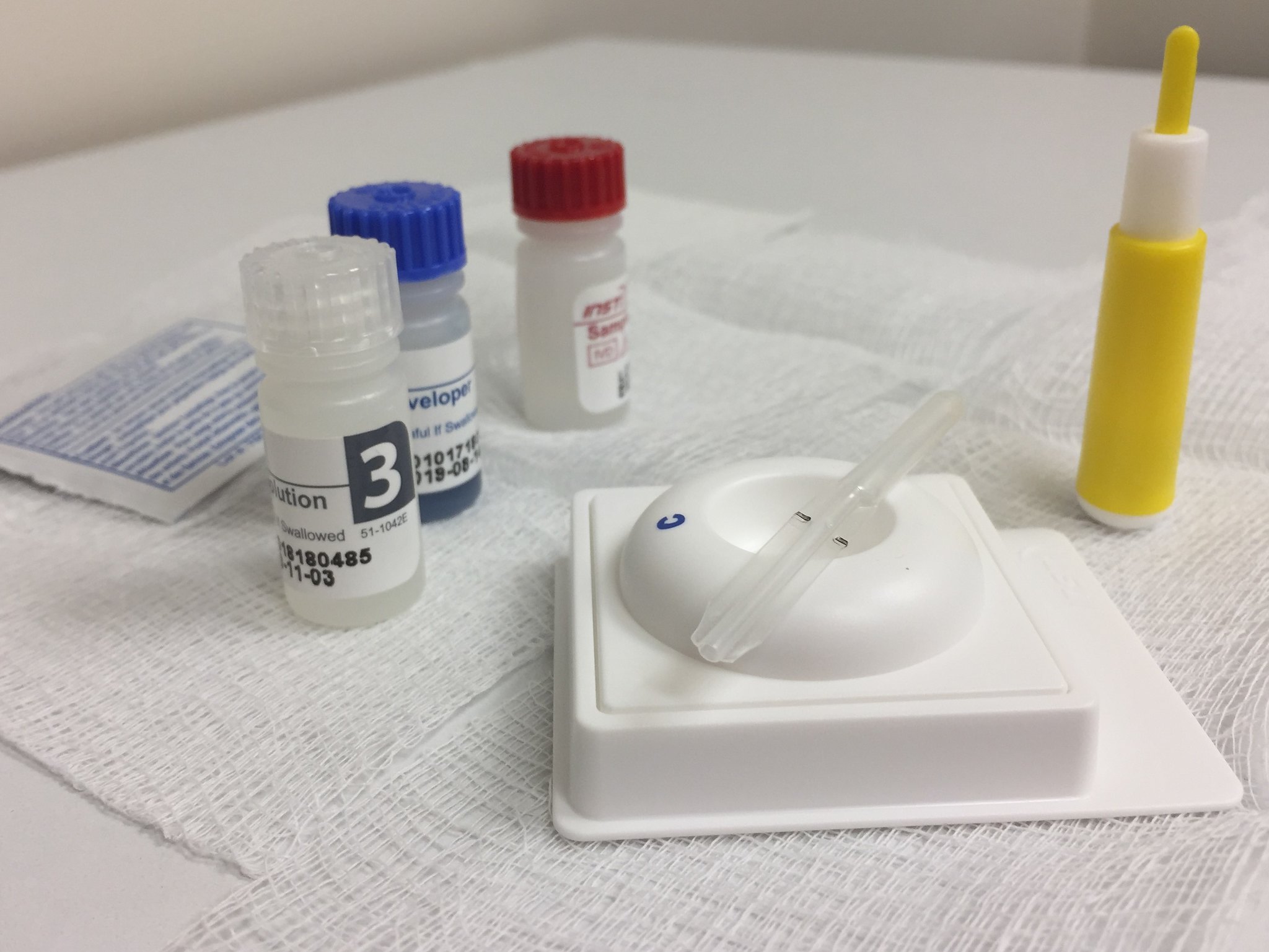
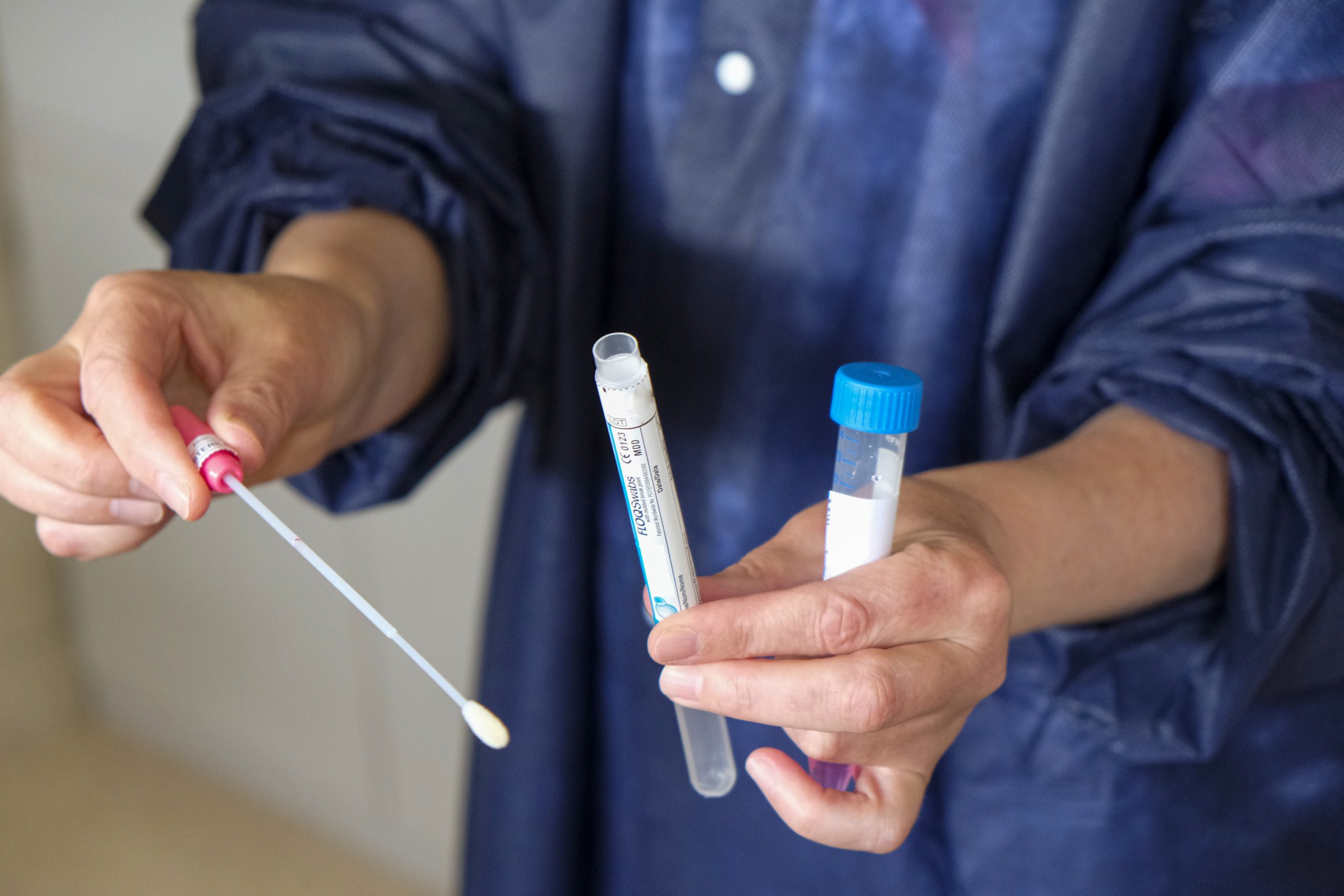
Le consortium de recherche PROMISE a donc conçu une stratégie d’interventions visant à appliquer les meilleures technologies disponibles, au moment le plus approprié, dans le système de santé. Cette intervention a été évaluée dans le cadre de l’essai contrôlé randomisé PROMISE-EPI mené au Burkina Faso et en Zambie. Lors de la deuxième visite de vaccination de l’enfant, le statut VIH des mères a été systématiquement réévalué et, pour les mères séropositives, le statut de leur enfant également. La vérification du statut VIH des mères a encore été répétée six mois après. Si la charge virale des mères était trop élevée (soit lors de la deuxième visite de vaccination, soit à 6 mois) après mesure par un appareil permettant le rendu immédiat du résultat, une prophylaxie par lamivudine en suspension orale était prescrite à leurs enfants non-infectés jusqu’à la fin de l’allaitement. L’efficacité de l’intervention a été évaluée par la proportion d’enfants séropositifs à 12 mois, en comparaison aux programmes locaux de prévention de la transmission postnatale au Burkina Faso et en Zambie, dérivés des recommandations de l’OMS. Ces derniers reposent sur une prophylaxie infantile de 6 à 12 semaines dès la naissance, en utilisant soit la névirapine au Burkina Faso), soit une trithérapie antirétrovirale en Zambie, arrêtée lorsque la charge virale de la mère était < 1000 copies/mL, avec mesure tous les 3 mois.
Entre décembre 2019 et septembre 2021, 34 054 mères (25 093 au Burkina Faso et 8 961 en Zambie) ont été dépistées pour le VIH lors de la deuxième visite de vaccination, et 1 526 (201 au Burkina Faso et 1 491 en Zambie) sur 1 692 mères vivant avec le VIH ont été incluses dans l’étude. L’âge médian des mères était de 30,6 ans, 98,4 % d’entre elles étaient sous traitement antirétroviral, et 11,5 % avaient une charge virale ≥ 1000 copies/mL. À la fin du suivi des enfants à 12 mois, un seul nourrisson du groupe intervention était infecté par le VIH, contre six dans le groupe contrôle, soit un taux de transmission de 0,19 % dans le groupe d’intervention et de 1,16 % dans le groupe contrôle. La durée moyenne de risque élevé de transmission (défini par une charge virale maternelle > 1000 copies/mL et l’absence de prophylaxie infantile) était 10 fois plus faible dans le groupe intervention que dans le groupe contrôle, ce qui confirme l’efficacité de l’intervention. Cette différence importante de l’incidence du VIH n’a cependant pas atteint exactement la signification statistique, en raison de la fermeture de certains sites d’étude pendant l’épidémie de COVID-19, qui n’a pas permis d’inclure autant de nourrissons qu’initialement prévu.
Ces résultats suggèrent fortement que la transmission du VIH par l’allaitement peut être réduite quasiment à zéro par une stratégie combinant les outils existants, incluant le dépistage chez le nourrisson et le contrôle de la charge virale chez la mère par une technique rapide, ainsi qu’une prophylaxie infantile prolongée chez les mères avec un traitement antirétroviral non efficace. Bien que l’étude n’ait pas été réalisée en milieu rural, où la faisabilité de cette intervention devrait être évaluée, cette stratégie innovante s’est avérée efficace dans des systèmes de santé et des pays aussi divers que la Zambie et le Burkina Faso, ce qui plaide en faveur de sa généralisation à d’autres pays d’Afrique subsaharienne.
L’étude PROMISE-EPI (numéro de subvention RIA2016MC-1617) fait partie du programme EDCTP2 soutenu par l’Union européenne et financé par le National Institute for Health and Care Research (NIHR) du Royaume-Uni. Le NIHR est financé par le département britanique de la santé et de la protection sociale (Department of Health and Social Care). Le programme NIHR Global Health Research soutient la recherche appliquée en santé de très haut niveau pour le bénéfice direct des populations des pays à revenu faible et intermédiaire, grâce au financement du gouvernement britannique.
[1] essai ANRS 12174, Nagot N. et al, Lancet 2016