© vege/fotolia
Et si méditer améliorait le vieillissement ? C’est ce que suggèrent les résultats d’une étude pilote menée par des chercheurs de l’Inserm basés à Caen et Lyon. 73 personnes âgées de 65 ans en moyenne ont passé des examens d’imagerie cérébrale. Parmi elles, les « experts en méditation » (avec 15 000 à 30 000 heures de méditation à leur actif) présentaient des différences significatives au niveau de certaines régions du cerveau. En permettant une réduction du stress, de l’anxiété, des émotions négatives et des problèmes de sommeil qui ont tendance à s’accentuer avec l’âge, la méditation pourrait réduire les effets néfastes de ces facteurs et avoir un effet positif sur le vieillissement cérébral. Ces résultats ont été publiés dans la revue Scientific Reports.
Avec l’âge, une diminution progressive du volume cérébral et du métabolisme du glucose apparaissent avec, pour conséquence, un déclin des fonctions cognitives. Ces changements physiologiques peuvent être exacerbés par le stress et une mauvaise qualité du sommeil. Ces deux derniers paramètres sont considérés comme des facteurs de risque de la maladie d’Alzheimer. Agir sur le stress et le sommeil pourrait donc faire partie de la panoplie d’outils utiles pour retarder le plus possible l’apparition de la maladie. Une des pistes de recherche, menée notamment à l’Inserm, se focalise sur l’aide de la méditation pour y parvenir.
C’est ainsi qu’une étude pilote menée par des chercheurs Inserm de Caen et Lyon a exploré la possibilité que la méditation puisse décaler de quelques années l’âge auquel les changements cérébraux favorables au développement d’Alzheimer apparaissaient. Pour cela, ils ont étudié le fonctionnement du cerveau de 6 personnes pratiquant la méditation. « Les « experts » ayant participé à l’étude sont âgés de 65 ans en moyenne et ont entre 15 000 et 30 000 heures de méditation derrière eux. Nous les avons sélectionnés car ils pratiquent la méditation selon différents courants traditionnels bouddhistes ce qui nous permet d’avoir un panel représentatif », explique Gaël Chételat, chercheuse Inserm et première auteure de ces travaux. Puis les chercheurs ont comparé le fonctionnement de leur cerveau à celui de 67 témoins non-méditants eux aussi âgés en moyenne de 65 ans. Un groupe plus large de 186 personnes âgées de 20 à 87 ans a également été inclus pour évaluer les effets classiques du vieillissement sur le cerveau et mieux comprendre les effets particuliers de la méditation.
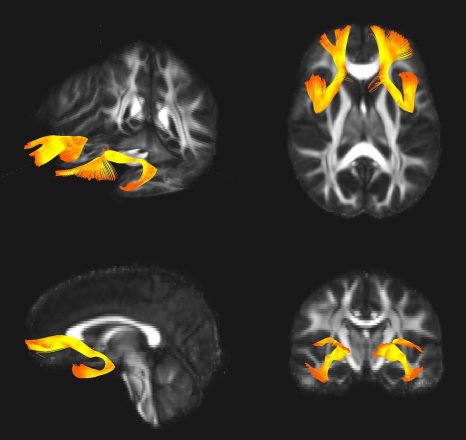
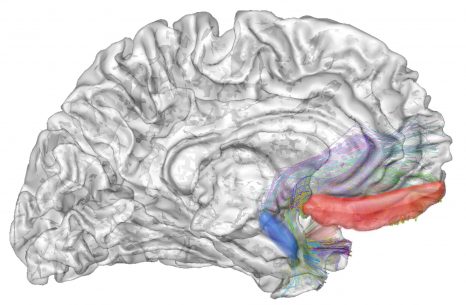
L’ensemble des personnes ayant participé à cette étude ont été soumises à des examens neurologiques par IRM et TEP au sein de la plateforme d’imagerie biomédicale Cyceron à Caen. Des différences significatives ont été mises en évidence au niveau du volume de la matière grise et du métabolisme du glucose. Dans le détail, les résultats d’examens montrent que le cortex frontal et cingulaire et l’insula des personnes pratiquant la méditation étaient plus volumineux et/ou avaient un métabolisme plus élevé que celui des témoins, et ce, même lorsque les différences de niveau d’éducation ou de style de vie étaient prises en compte. « Les régions cérébrales détectées avec un plus grand volume ou métabolisme chez les personnes pratiquant la méditation sont spécifiquement celles qui déclinent le plus avec l’âge », explique Gaël Chételat. Les effets de l’âge évalués dans cette même étude chez les personnes non-méditantes âgées de 20 à 87 ans se concentraient effectivement sur certaines régions bien particulières – les mêmes que celles qui étaient préservées chez les méditants âgés.
Ces premiers résultats suggèrent que la méditation pourrait réduire les effets néfastes de ces facteurs sur le cerveau et avoir un effet positif sur le vieillissement cérébral, possiblement en permettant une réduction du stress, de l’anxiété, des émotions négatives et des problèmes de sommeil qui ont tendance à s’accentuer avec l’âge.
Bien entendu, il s’agit d’une étude pilote donc il faudra réitérer ces observations sur des échantillons de personnes plus grands afin d’obtenir des résultats plus robustes. Par ailleurs, les chercheurs s’attellent aussi à comprendre quels sont les mécanismes qui permettraient à la médiation d’avoir cet impact positif sur le vieillissement cérébral.
Les chercheurs auteurs de cette étude se sont vus attribuer un financement de 6 millions d’euros par la Commission européenne pour mener à bien un projet de plus grande envergure sur le bien vieillir nommé silver santé study. Ce projet permettra de mieux comprendre les facteurs de vie qui déterminent le bien vieillir, et de tester les bienfaits d’entraînements mentaux à la méditation ou à l’apprentissage de l’anglais sur le bien-être et la santé mentale des seniors. Il est coordonné par l’Inserm (Gaël Chételat, U1237, Caen) et regroupe dix partenaires dans 6 pays européens (la France, la Suisse, l’Angleterre, l’Allemagne, la Belgique et l’Espagne). Les premiers résultats devraient être connus en 2019.