Darragh Duffy et Alba Libre, unité d’Immunobiologie des cellules dendritiques, Institut Pasteur / Inserm, utilisant le test Genedrive de diagnostic du HCV. ©Institut Pasteur
Pour l’éradication du virus de l’hépatite C (HCV), un des enjeux émis par l’OMS est le diagnostic des cas chroniques qui sont la plupart du temps asymptomatiques. Les progrès doivent donc porter sur le diagnostic précoce et « décentralisé », c’est-à-dire accessible aux populations des pays aux ressources limitées. Des chercheurs de l’Institut Pasteur et de l’Inserm, en collaboration avec la société Genedrive, ont développé un test de dépistage HCV, transportable au chevet du patient, rapide et fiable. Ce nouveau test de détection permet donc une prise en charge immédiate du patient suite au diagnostic, et une mise en place sans tarder d’un traitement contre la maladie. Ces résultats ont été publiés dans la revue Gut, le 04 avril 2018.
L’hépatite C est une inflammation du foie causée par le virus HCV. Le virus peut conduire à un état de portage chronique, pouvant entrainer de nombreuses années plus tard des complications graves : cirrhose et cancer du foie. L’infection chronique au virus de l’hépatite C concerne environ 1% de la population mondiale (71 millions de personnes) et est responsable de 400 000 décès par an dus à l’évolution sévère de la maladie.
Actuellement, les récents antiviraux d’action directe permettent de traiter les hépatites C chroniques à 95% s’ils sont pris à temps. Par conséquent, l’OMS a publié en 2016 un plan pour éliminer cette menace pour la santé publique d’ici 2030. Le défi majeur pour répondre à cet ambitieux objectif, reste cependant le dépistage des patients asymptomatiques, notamment dans les pays à revenus faibles ou intermédiaires, où l’accès aux tests classiques reste limité.
Le diagnostic actuel se fait, dans un premier temps, par la mesure des anticorps spécifiques au VHC. Mais ce test ne permet pas d’indiquer si le patient a été infecté par le passé (et qu’il y a eu une rémission spontanée) ou, s’il est encore infecté de façon chronique. Dans un deuxième temps, une recherche d’ARN du virus dans le sang doit être réalisée par PCR1 pour confirmer ou non l’infection chronique.
Il existe des tests sérologiques des anticorps au HCV rapides mais les tests par PCR demandent des infrastructures dédiées et du personnel qualifié. Dans les pays à ressources limitées, ce type de test n’est disponible que dans des laboratoires centralisés. Ce qui a pour effet que moins de 1% des personnes infectées dans ces régions savent qu’ils le sont. De plus, ces tests demandent plusieurs visites et du temps entre chaque résultat ce qui augmente le risque de perdre les patients en cours de diagnostic. Pour améliorer la prise en charge du patient, depuis le diagnostic jusqu’au traitement, il était urgent de disposer d’un test de détection de l’ARN du virus, qui puisse être décentralisé dans les milieux ruraux, ou à faibles ressources.
L’équipe de chercheurs menée par Darragh Duffy (unité d’Immunobiologie des cellules dendritiques, Institut Pasteur / Inserm) a développé un test, en collaboration avec la société Genedrive, capable de détecter l’ARN du virus HCV, tout en étant aussi fiable que les tests existants, plus rapide et transportable auprès du patient. Les opérations de PCR peuvent se faire dans le kit miniaturisé grâce à un ventilateur qui permet la succession des 40 cycles nécessaires. L’analyse peut être réalisée en une heure environ. Au final, ce type d’appareil est moins cher que les tests actuels qui demandent des infrastructures conséquentes.
Les chercheurs ont d’abord validé cliniquement le test sur des cohortes de l’Institut Pasteur en France et du National Health Service de Nottingham au Royaume-Uni, puis avec les données du Lancet Laboratories de Johannesburg avec des échantillons provenant d’Afrique du Sud, du Kenya, du Ghana, du Nigeria, et d’Uganda.
L’étude démontre que le test a une spécificité de 100%, c’est-à-dire qu’il ne fournit aucun faux positif, et a une sensibilité de 98,6%, ce qui répond aux exigences de l’OMS pour ce type de test.
Le kit a obtenu une certification CE pour une distribution en Europe, et sera disponible à la vente au Moyen-Orient, en Afrique, en Asie du Sud-Est, et en Inde une fois que l’autorisation réglementaire locale aura été obtenue.
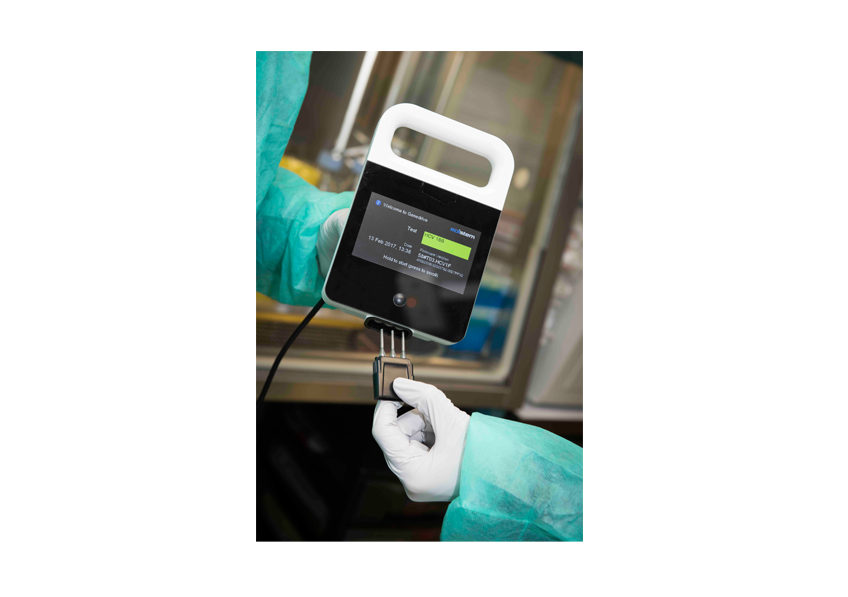
Test de diagnostic Genedrive de détection du HCV. ©Institut Pasteur
1