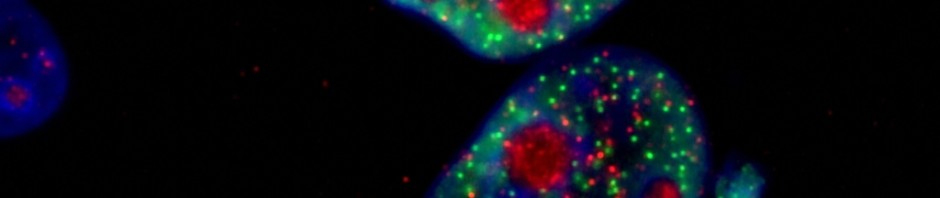
Cellules cancéreuses. Expression de la protéine PML en rouge et du gène ZNF703 en vert dans des cellules de la lignée de cancer du sein MCF7. ©Inserm/Ginestier, Christophe
Une analyse de la cohorte CANTO publiée aujourd’hui dans la revue Annals of Oncology vient bousculer les idées reçues sur l’impact que peuvent avoir l’hormonothérapie et la chimiothérapie sur la qualité de vie des femmes atteintes d’un cancer du sein. Contrairement à ce qui est communément admis, à deux ans du diagnostic, l’hormonothérapie, traitement extrêmement efficace contre le cancer du sein, a un impact plus long et plus délétère sur la qualité de vie notamment celle des femmes ménopausées ; les effets négatifs de la chimiothérapie étant plus transitoires. À l’heure où les recommandations internationales sont de prescrire une hormonothérapie pendant 5 à 10 ans, il est important de proposer une prise en charge aux femmes qui développent des symptômes sévères liés aux traitements antihormonaux et d’identifier celles qui pourraient bénéficier d’une désescalade thérapeutique.
Ces travaux ont été dirigés par le Dr Inès Vaz-Luis, oncologue spécialiste du cancer du sein et chercheur à Gustave Roussy au sein du laboratoire « Identification de nouvelles cibles thérapeutiques en cancérologie » (Inserm/Université Paris-Sud/Gustave Roussy).
« Cette analyse de la cohorte CANTO démontre pour la première fois que les traitements antihormonaux n’ont pas un impact plus faible que la chimiothérapie sur la qualité de vie des femmes. Bien au contraire, la détérioration de la qualité de vie, qui se déclare au diagnostic, persiste deux ans après alors que l’impact de la chimiothérapie est plus transitoire » détaille le Dr Vaz-Luis.
Dans cette étude, les chercheurs ont mesuré au moment du diagnostic, à un an puis à deux ans la qualité de vie de 4 262 patientes atteintes d’un cancer du sein localisé (stade I à III). Le traitement de ces patientes était composé de chirurgie et pour certaines de chimiothérapie et/ou de radiothérapie. Environ 75-80 % d’entre elles prenaient ensuite une hormonothérapie pendant au moins 5 ans. L’équipe de recherche a utilisé un outil qui évalue la qualité de vie générale des patients atteints de tout type de cancer (EORTC QLQ-C30) couplé à un outil de mesure plus spécifique de la qualité de vie dans le cadre du cancer du sein (QLQ-BR23).
Il est observé pour l’ensemble de la population étudiée une dégradation globale de la qualité de vie deux ans après le diagnostic. Cette détérioration est plus importante chez les patientes ayant reçu de l’hormonothérapie, surtout après la ménopause. A contrario, l’impact de la chimiothérapie est plus important sur la qualité de vie des femmes non-ménopausées, particulièrement sur la détérioration des fonctions cognitives.
« Il est primordial à l’avenir que nous puissions prédire quelles femmes vont développer des symptômes sévères avec les traitements antihormonaux afin de pouvoir mieux les accompagner » ajoute le Dr Vaz-Luis. Alors qu’il a été prouvé que l’hormonothérapie apporte un réel bénéfice pour éviter les rechutes des cancers hormono-dépendants[1] − qui représentent 75 % de la totalité des cancers du sein − la dégradation de la qualité de vie peut aussi avoir un effet négatif sur l’observance des femmes au traitement. Il est donc important de leur proposer une prise en charge des symptômes les plus impactants, notamment ceux liées à la ménopause, les douleurs musculo-squelettiques, la dépression, la fatigue sévère, ou encore les dysfonctions cognitives, et d’y associer des soins de support comme l’exercice physique et les thérapies cognitivo-comportementales.
« À l’avenir, il sera aussi important de parvenir à identifier avant traitement les patientes à haut risque de rechute de celles à plus faible risque. Cela permettra d’éviter l’escalade des traitements antihormonaux » conclut le Dr Vaz-Luis qui rappelle que « l’hormonothérapie est extrêmement efficace contre le cancer du sein. Elle permet une réduction d’environ 50 % du risque de rechute. La description d’une mauvaise tolérance ne remet en aucun cas en cause l’excellent rapport bénéfice/risque de ce traitement ».
Promue par Unicancer et dirigée par le Pr Fabrice André, oncologue spécialisé dans le cancer du sein à Gustave Roussy, directeur de recherche Inserm et responsable du laboratoire « Identification de nouvelles cibles thérapeutiques en cancérologie » (Inserm/Université Paris-Sud/Gustave Roussy), la cohorte CANTO pour CANcer TOxicities est composée de 12 000 femmes atteintes d’un cancer du sein prises en charge dans 26 centres français. Elle a pour objectif de décrire les toxicités associées aux traitements, d’identifier les populations susceptibles de les développer et d’adapter les traitements en conséquence pour garantir une meilleure qualité de vie dans l’après-cancer.
[1] J Clin Oncol. 2019 Feb 10;37(5):423-438 : https://doi.org/10.1200/JCO.18.01160https://doi.org/10.1200/JCO.18.01160