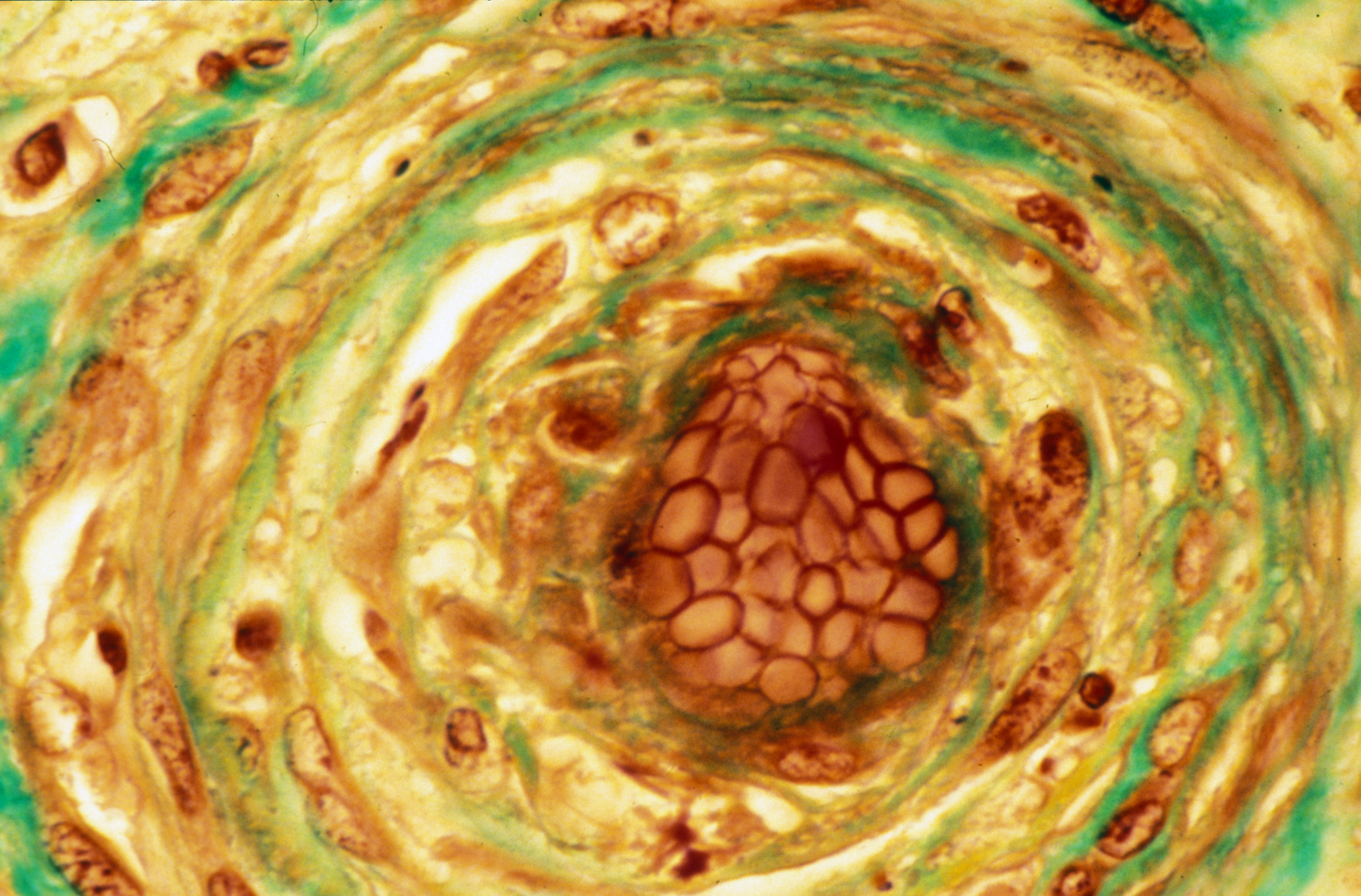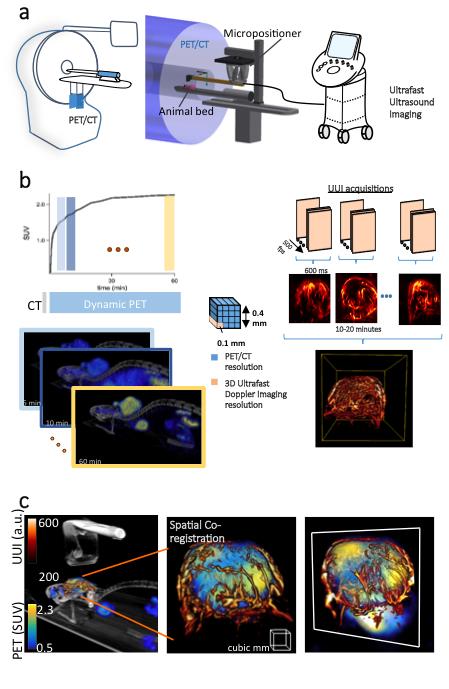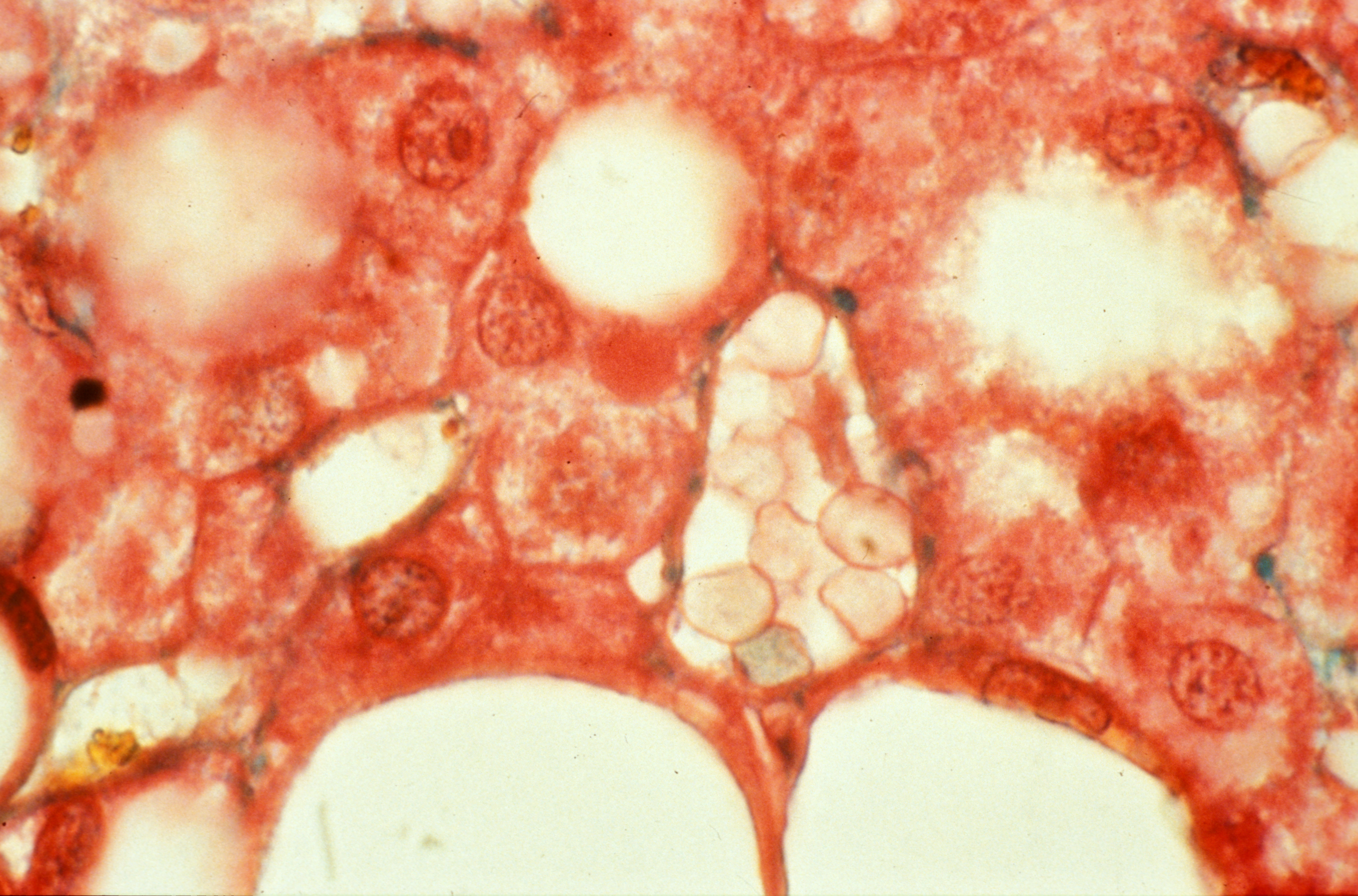
Détail d’une stéatose, accumulation d’une graisse, triglycéride, dans la cellule hépatique. Crédits: Inserm/Hadchouel, Michelle
Le microbiote continue jour après jour de livrer ses secrets. Dans une nouvelle étude publiée dans la revue Nature Medicine, Rémy Burcelin, directeur de recherche Inserm au sein de l’Institut des maladies métaboliques et cardiovasculaires (Inserm/UPS) avec des chercheurs de l’Imperial College de Londres, de l’hôpital de Girone et de l’Université Tor Vergata de Rome, montrent comment certaines bactéries intestinales provoquent l’accumulation de graisse dans le foie et jouent un rôle majeur dans la maladie dite du « foie gras » (stéatose hépatique). Ces travaux pourraient permettre à terme de disposer de biomarqueurs prédictifs de la maladie et de proposer des solutions thérapeutiques fondées sur des approches pharmacologiques et une nouvelle génération de probiotiques.
70 à 80 % des personnes souffrant d’obésité et de diabète possèdent un « foie gras ». L’accumulation de graisse dans cet organe conduit rapidement au développement d’une insuffisance hépatique avec pour conséquences un risque de développement de cancer et une capacité réduite à filtrer les toxines environnementales et alimentaires.
Aujourd’hui, il n’existe pas de médicament pour combattre ces altérations hépatiques. Les seules solutions résident dans un contrôle strict du régime alimentaire et, dans les cas les plus extrêmes, consistent à proposer une greffe de foie.
Face à cette impasse thérapeutique, un consortium européen (FLORINASH) réunissant des chercheurs français de l’Inserm, italiens et anglais, a décidé de créer puis de colliger les données issues de deux grandes cohortes de 800 hommes et femmes souffrant d’obésité, en séparant les groupes en fonction de la présence ou non d’un « foie gras ». Chez ces personnes, de nombreuses données médicales ont pu être collectées. Puis, dans un sous-groupe plus réduit de femmes obèses (environ une centaine) des analyses moléculaires ont pu être réalisées à partir de biopsies du foie, de prélèvements d’urine et de plasma et de la collection de selles.
Le but de cette nouvelle étude était de découvrir le chemin biologique par lequel l’insuffisance hépatique se déclarait, de révéler des marqueurs biologiques permettant de prédire le risque de développer la maladie chez les personnes obèses et de trouver des solutions thérapeutiques.
Des résultats antérieurs (publiés en 2007 et 2011) avaient permis d’expliquer le processus par lequel les bactéries de l’intestin (microbiote) devenaient délétères et entrainaient le diabète et l’obésité. Les chercheurs se sont donc posé la question de savoir si le microbiote pouvait, là encore, jouer un rôle dans la survenue des complications hépatiques du diabète et de l’obésité.
À partir des biopsies réalisées et des données cliniques des patientes, les chercheurs ont utilisé une approche de big data. Une immense base de données contenant tous les détails moléculaires de la composition du microbiote, des gènes du foie, des protéines plasmatiques et des protéines urinaires a été constituée. Puis, les chercheurs ont développé des algorithmes capables d’identifier un lien logique entre ces données.
En d’autres termes, explique Rémy Burcelin, directeur de recherche Inserm et coordinateur de ce travail : » Nous voulions voir si nous pouvions identifier, étape par étape, depuis le microbiote, la succession de mécanismes responsables de la maladie hépatique. »
Grâce à ce travail à grande échelle (plus de 3 millions de gènes bactériens ont été passés au crible par les algorithmes), les chercheurs ont pu aboutir à deux constats. Premièrement, plus la maladie progresse, plus la diversité des gènes microbiens retrouvés diminue ; ce qui suggère une réduction de la composition du microbiote avant même que les premiers symptômes n’apparaissent. Deuxièmement, un des composés spécifiques du microbiote, l’acide phénylacétique, potentialise l’accumulation de graisses dans le foie.
Afin de prouver le lien de cause à effet, les chercheurs ont poursuivi leurs travaux chez l’animal et sur des cellules du foie humain. Pour cela, ils ont transféré chez des souris saines le microbiote de donneurs humains présentant une maladie du foie gras. Le taux de triglycérides a alors augmenté drastiquement dans le foie de ces souris. Ils ont également montré que l’acide phénylacétique administré aux souris déclenchait l’accumulation de graisses dans leur foie.
D’après l’équipe, il serait possible à terme, en manipulant des bactéries du microbiote, d’empêcher les complications hépatiques liées à l’obésité. L’idée est également de pouvoir aboutir au développement d’une nouvelle génération de probiotiques et à une stratégie pharmacologique interférant avec les mécanismes bactériens responsables de l’affection hépatique.