Madame Liliane Bettencourt, Présidente de la Fondation Bettencourt Schueller, a remis, mardi 25 janvier à l’Institut de France, en présence d’éminents représentants de la communauté scientifiques française, les Prix de la 11e édition des Coups d’élan pour la Recherche française.
Ces prix sont attribués chaque année à des laboratoires français de recherche renommés pour la qualité de leurs équipes et le caractère prometteur de leurs recherches afin de leur permettre d’optimiser leurs infrastructures (locaux, matériel) et de bénéficier d’une aide ponctuelle au fonctionnement.
Au total, à ce jour, 34 laboratoires (soit près de 1000 chercheurs) ont déjà bénéficié des Coups d’élan pour la Recherche française de la Fondation Bettencourt Schueller.
© S. Compoint
Cette année, la Fondation Bettencourt Schueller a décidé d’attribuer 1 000 000 € à 4 équipes de l’Inserm. Les lauréats sont :
Équipe dirigée par le Pr. François Goffinet, Unité Inserm 953 « Recherche épidémiologique en santé périnatale et santé des femmes et des enfants », Hôpital Cochin-Saint-Vincent de Paul, Paris
L’objectif des recherches du laboratoire de François Goffinet est d’accroître les connaissances nécessaires à une meilleure définition et une meilleure mise en application de pratiques et de politiques efficaces concernant la santé de la femme et de l’enfant dans la période qui entoure la grossesse et l’accouchement. Son équipe évalue les pratiques cliniques et les modes d’organisation des soins et met au point des indicateurs en santé périnatale dans le but de développer les connaissances permettant de définir de nouveaux protocoles de soins ou d’adapter des mesures réglementaires.
L’installation de l’unité dans un nouveau bâtiment de la maternité Port-Royal, soutenue par le Prix Coups d’élan, permettra de regrouper des services cliniques et des équipes de recherche, facilitant ainsi les interactions entre cliniciens et chercheurs dans le domaine de la santé périnatale et maternelle.
Équipe dirigée par le Pr. Michel Haïssaguerre, Unité Inserm 1045, Laboratoire « Electrophysiologie et stimulation cardiaque », Hôpital Haut-Lévêque, Bordeaux
a fonction cardiaque est, dans l’esprit de tous, associée à la contraction du muscle cardiaque. Cette action mécanique n’est cependant possible qu’après l’activation électrique des cellules cardiaques, s’exprimant par l’électrocardiogramme. Près de la moitié des décès d’origine cardiaque sont des dysfonctionnements électriques se traduisant par des morts subites, très largement liées à une arythmie instantanément mortelle (fibrillation ventriculaire), correspondant à une « tornade » électrique. Michel Haïssaguerre a montré que ces tornades électriques sont initiées par les cellules de Purkinje, provenant d’une fraction infime de la masse cardiaque. Ces travaux ont eu un impact considérable dans la compréhension et le traitement des troubles du rythme cardiaque. Le défi majeur reste l’identification des sujets menacés.
Le Prix Coups d’élan permettra à cette équipe de s’installer dans le nouveau Centre de recherche cardio-thoracique situé à Bordeaux.
Équipe dirigée par le Pr. Guido Kroemer, Unité Inserm 872, laboratoire « Apoptose, Cancer et immunité », Centre de Recherche des Cordeliers, Paris
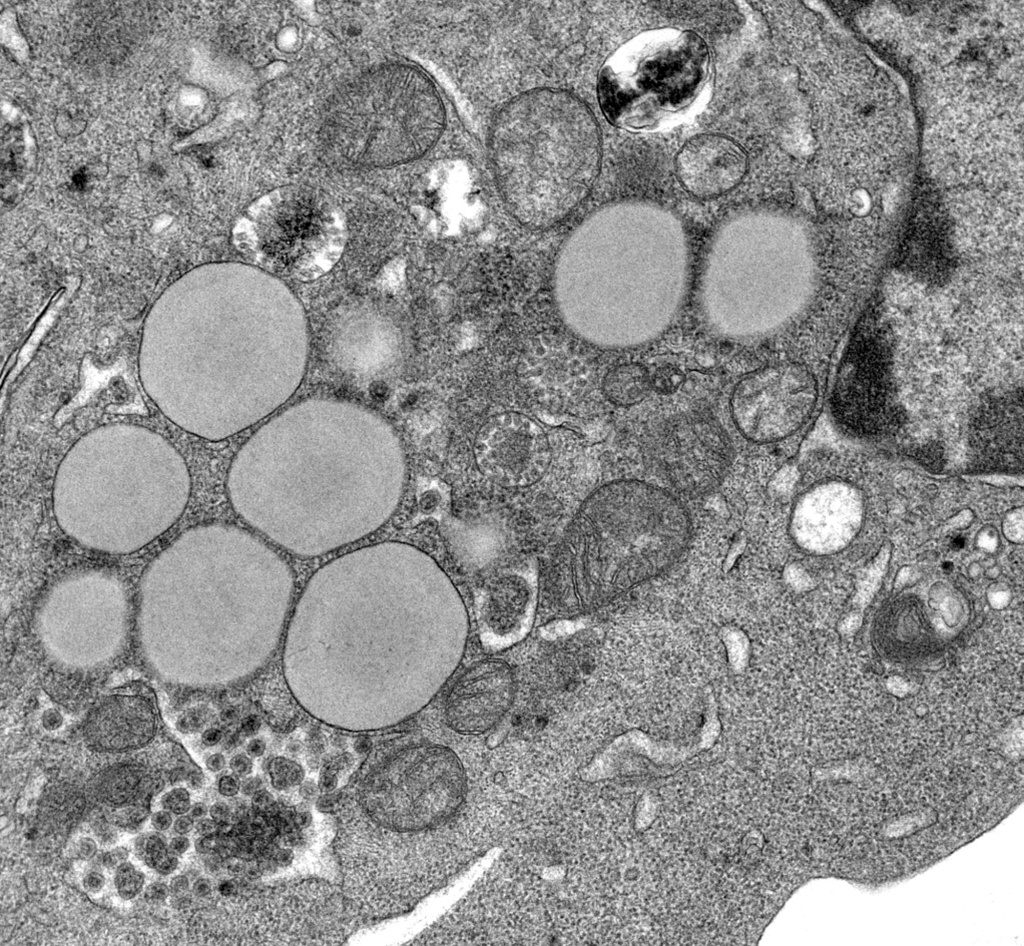
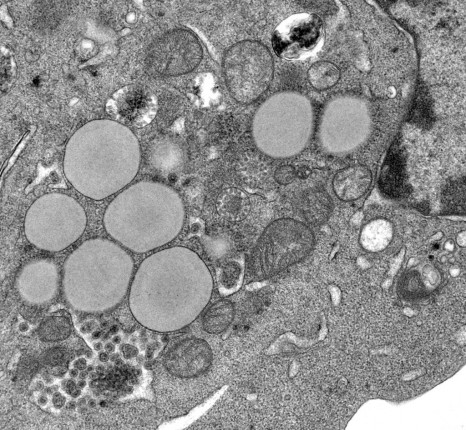
Guido Kroemer s’intéresse aux interactions entre médicament, cellule cancéreuse et système immunitaire, et plus particulièrement aux mécanismes de l’apoptose, processus de mort cellulaire programmée. Ces recherches ont permis de démontrer que la chimiothérapie anticancéreuse est particulièrement efficace lorsqu’elle induit une mort cellulaire immunogénique et déclenche une réponse immunitaire contre le cancer. L’objectif ultime de ce projet de recherche est d’isoler les signaux émis par les cellules tumorales succombant à une mort cellulaire immunogénique et de définir quels médicaments anticancéreux seraient capables de déclencher ce processus apoptotique.
Le Prix Coups d’élan va permettre de rénover des locaux du Centre de Recherche des Cordeliers (Paris) où s’installera le l’équipe de Guido Kroemer, ainsi que d’équiper son laboratoire de matériel pour la culture cellulaire.
Équipe dirigée par le Dr. Julien Marie, Unité Inserm 1052, Centre de Recherche en Cancérologie de Lyon, laboratoire « TGF-beta et échappement immunitaire », Centre Léon Bérard, Lyon
Parmi les cellules qui composent notre système immunitaire, les lymphocytes T présentent une activité spécifique et accrue contre les cellules cancéreuses et sont ainsi capables de les tuer efficacement in vitro. Cependant, au sein de l’organisme, cette activité antitumorale des lymphocytes T est moins efficace car elle est réprimée par l’action d’une protéine, le TGF-ß, produite par les cellules tumorales. Julien Marie s’intéresse au rôle joué par le TGF-ß dans le contrôle des lymphocytes T et cherche à élucider les mécanismes qui bloquent leur activation au moyen d’approches physiopathologiques nécessitant des investigations à l’échelle de l’organisme.
Le Prix Coups d’élan va permettre à ce laboratoire d’aménager, d’équiper et de mettre aux normes une animalerie pour souris dépourvues de germes pathogènes.
Coups élan Bettencourt Schueller © S. Compoint
De gauche à droite : Dr. Julien Marie (Lauréat des Prix Coups d’élan 2010), Gabriel de Broglie (Chancelier de l’Institut de France), Pr. Hugues de Thé (Membre du Comité Scientifique de la Fondation Bettencourt Schueller), Pr. François Goffinet (Lauréat des Prix Coups d’élan 2010), Dr. Sebastian Amigorena (Membre du Comité Scientifique de la Fondation Bettencourt Schueller), Liliane Bettencourt (Présidente de la Fondation Bettencourt Schueller), Pr. Guido Kroemer (Lauréat des Prix Coups d’élan 2010), Pr. André Syrota (PDG de l’Inserm), Pr. Pierre Corvol (Président du Comité Scientifique de la Fondation Bettencourt Schueller).