©Brooke Lark on Unsplash
Et si l’efficacité du système immunitaire contre les cellules cancéreuses pouvait être renforcée par un régime alimentaire sans réduction calorique mais avec des nutriments précisément dosés ? C’est sur cette question que se sont penchés des chercheurs de l’Inserm de l’Université Côte d’Azur, à travers l’étude des effets de régimes alimentaires restrictifs, sur la croissance tumorale chez la souris. Ils ont observé qu’un régime diminué en protéines, permettait de limiter le développement des tumeurs par accroissement de la réponse immunitaire. Les résultats, à paraître dans Cell metabolism, s’avèrent prometteurs pour la compréhension de l’immunité anti-tumorale chez la souris et ouvrent la voie à de nouvelles études chez l’homme.
Si le jeûne a acquis une récente popularité dans la prévention de l’occurrence de cancers, dans le renforcement de la chimiothérapie et dans la prolongation de l’espérance de vie chez les patients atteints de tumeurs, aucune preuve scientifique solide ne vient à ce jour étayer l’efficacité de cette pratique. Les essais cliniques sont en réalité quasi inexistants chez l’homme et les résultats obtenus à partir de modèles animaux sont très débattus. Une réduction calorique prolongée peut en outre s’avérer être un facteur aggravant de la dénutrition et de la perte de masse musculaire (sarcopénie) fréquemment associées aux chimiothérapies.
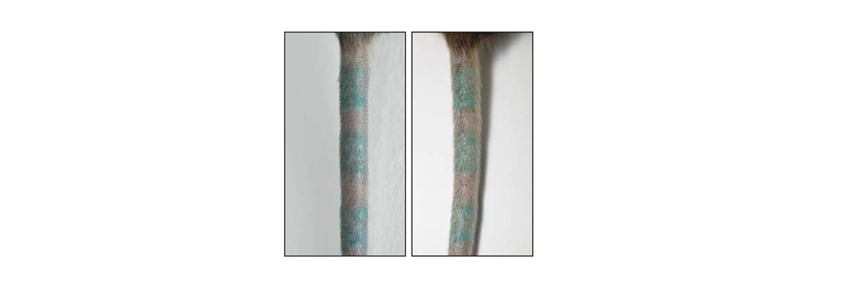
Une équipe de l’Inserm au sein de l’Université Côte d’Azur s’est intéressée à l’hypothèse selon laquelle une modulation de l’apport en macronutriments (glucides, lipides et protéines), plutôt que de l’apport calorique, pouvait avoir un impact restrictif sur la croissance tumorale. Les chercheurs ont comparé l’effet sur la croissance des tumeurs chez la souris de plusieurs régimes alimentaires, plus ou moins appauvris en glucides ou en protéines, mais de même apport calorique. Les résultats ont montré qu’un régime appauvri en protéines mais pas en glucides avait un impact positif sur la limitation de la croissance tumorale et l’allongement de la durée de vie des souris.
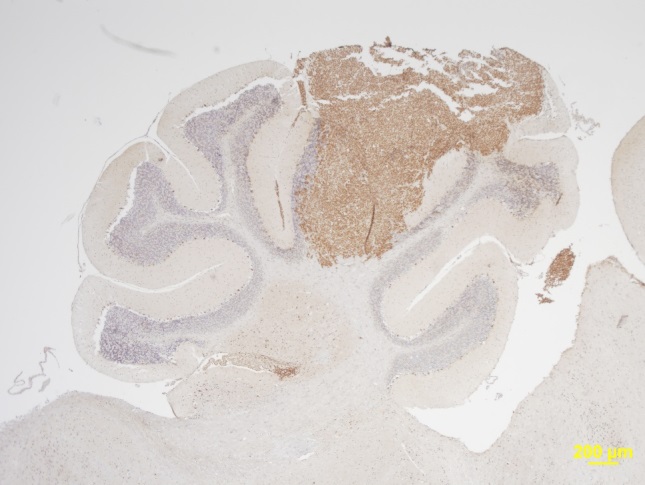
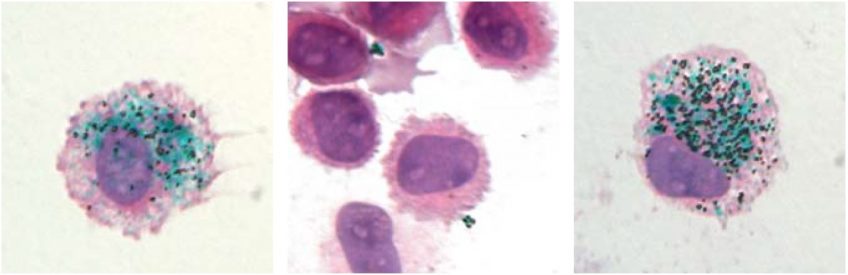
L’analyse du contenu cellulaire des tumeurs des souris sous régime appauvri en protéines, a montré une quantité accrue et une activité plus intense des cellules anti-tumorales spécifiques du système immunitaire.
Les chercheurs ont constatés que la limitation de la croissance tumorale était due non pas à une inhibition de la prolifération des cellules cancéreuses comme on pouvait le croire, mais à un accroissement de l’efficacité de la réponse immunitaire, aussi appelée immunosurveillance, pour détruire les cellules cancéreuses.
En se penchant sur les mécanismes moléculaires liés à ce phénomène, les chercheurs ont constaté que ce renforcement de l’immunosurveillance était lié à la sécrétion par les cellules tumorales de protéines d’alerte du système immunitaire : les cytokines. Selon l’étude, la diminution en protéines dans le régime alimentaire rendrait insuffisante la quantité disponible de certains acides aminés (constituants des protéines) auxquels les cellules cancéreuses sont très sensibles. Une diminution de l’accès aux acides aminés provoquerait un stress chez les cellules tumorales, qui libèreraient alors des cytokines, activant ainsi une forte réponse immunitaire au niveau de la tumeur.