Fotolia
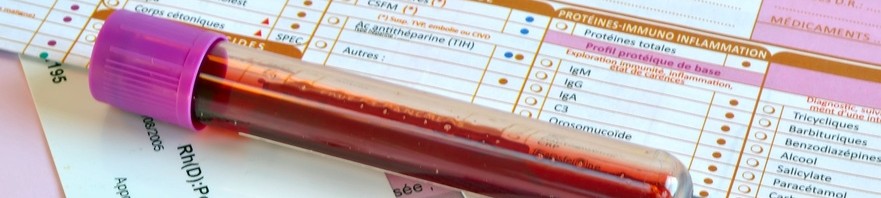
Des équipes de l’AP-HP en collaboration avec des chercheurs de l’ICM (Inserm/CNRS/UPMC), et la start-up Metafora Biosystems, issue du CNRS, viennent de développer un test de diagnostic sanguin d’une maladie neurologique rare mais traitable, la maladie de De Vivo.
Il a été testé sur 30 patients atteints de cette maladie qui induit des déficits neurologiques tels qu’une épilepsie ou des troubles de la marche par exemple.
Le nouveau test[1], dont les résultats sont publiés dans la revue Annals of Neurology, permettra d’identifier rapidement (en moins de 48h) et facilement les enfants et les adultes touchés comparativement aux tests diagnostiques actuels qui reposent sur un geste invasif, la ponction lombaire ou des analyses ADN complexes.
La maladie de De Vivo ou syndrome du déficit en transporteur cérébral de glucose de type 1 (GLUT-1) se caractérise le plus souvent par un retard du développement, une épilepsie et/ou des troubles moteurs chez l’enfant. Des formes frustres[2] ont été décrites chez les enfants (accès de mouvements anormaux) mais aussi les adultes. On estime, sur la base d’une prévalence estimée à 1/83 000 dans la population danoise, à 800 le nombre de patients en France[3], dont un peu plus d’une centaine serait diagnostiquée. Dès lors qu’ils sont diagnostiqués, les patients peuvent bénéficier de traitements métaboliques qui diminuent les symptômes.
Le Dr Fanny Mochel à l’hôpital Pitié-Salpêtrière AP-HP, en lien avec les équipes de plusieurs hôpitaux de l’AP-HP (Bichat, Raymond-Poincaré et Robert-Debré) et de l’Institut du cerveau et de la moelle épinière (Inserm/CNRS/UPMC), ont développé avec la start-up Metafora Biosystems, un test de diagnostic sanguin simple et rapide (moins de 48h) de la maladie de De Vivo. Le diagnostic actuel est contraignant puisqu’il repose sur un geste invasif, la ponction lombaire, et des analyses génétiques complexes.
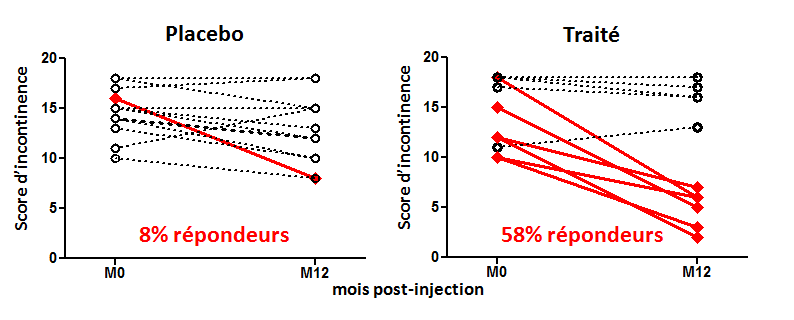
Dans cette étude, les prélèvements sanguins de 30 patients atteints de la maladie avec des profils différents, en fonction de l’âge et des symptômes, ont été analysés. Comparés à 346 prélèvements d’individus témoins, les résultats montrent que le test est significativement concluant avec 78% de diagnostic, incluant des patients pour lesquels les analyses génétiques n’avaient pas permis d’établir le diagnostic.
Forts de ces résultats, les chercheurs recommandent l’utilisation de ce test en routine clinique dans tous les services de neuropédiatrie et de neurologie. Ils suggèrent que la simplicité de ce nouveau test devrait augmenter le nombre de patients identifiés en France.
Grâce à ce nouveau test sanguin innovant, la maladie va pouvoir être recherchée chez tout patient présentant une déficience intellectuelle et/ou une épilepsie et/ou un trouble de la marche. Les traitements que l’on peut mettre en œuvre améliorent considérablement les symptômes, avec par exemple la disparition des crises d’épilepsie, et sont d’autant efficaces qu’ils sont débutés tôt, d’où l’importance d’un diagnostic précoce.
[1] Protégé par le brevet CNRS WO2004/096841.
[2] Quand les patients ne présentent pas tous les symptômes caractéristiques d’une maladie ou que ces symptômes sont légers.
[3] [1] Larsen J, et al. The role of SLC2A1 mutations in myoclonic astatic epilepsy and absence epilepsy, and the estimated frequency of GLUT1 deficiency syndrome. Epilepsia. 2015 Dec;56(12):e203-8.